
银氨溶液可用于检测CO气体。实验室研究该反应的装置图如下: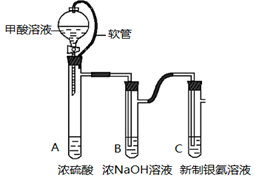
(1)甲酸在浓硫酸条件下能分解生成CO和H2O,体现浓硫酸具有 (填“氧化性”或脱水性)。
(2)软管的作用是 。
(3)浓NaOH溶液的作用是 。
(4)反应结束后试管C底部有黑色沉淀,为验证产物,分离出上层清液和底部黑色固体,并进行实验。
a.测得上层清液pH为10。
b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体。
c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。
d.将黑色沉淀用蒸馏水洗净。
① 实验c的目的是 。
② 根据上述实验现象证明上层清液中含有 。
③ 已知银可溶于浓硝酸,设计实验证明黑色固体是Ag单质:
④ CO与银氨溶液反应中有氨气生成,根据实验现象写出该反应的化学方程式: 。
(1)脱水性 (2)保证分液漏斗和试管A内气压相同使甲酸溶液可以顺利滴下。
(3)洗气,吸收酸性气体
(4)①对比试验,证明Ba(OH)2溶液不能与银氨溶液反应,证明实验b中的现象是产物与Ba(OH)2溶液反应导致的。②(NH4)2CO3或NH4+、CO32—。③取少量黑色固体,向其中滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl 溶液,能产生白色沉淀,说明黑色固体为单质银。CO+ 2Ag(NH3)2OH=(NH4)2CO3+2Ag↓+2NH3↑
解析试题分析:(1)甲酸与浓硫酸共热发生反应:HCOOH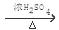 CO↑+H2O。在该反应中浓硫酸的作用是脱水性。(2)软管的作用是使分液漏斗的上下气体压强相同,这样分液漏斗中的液体在重力的作用下就可以顺利滴下。(3)甲酸在加热时会挥发,也可能部分CO被氧化为CO2,所以浓NaOH溶液的作用是洗气,吸收酸性气体。(4)a.测得上层清液pH为10,证明溶液为碱性;b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体。证明含有NH4+;同时证明在溶液中含有的离子能与Ba(OH)2电离产生的离子结合形成白色难溶性物质。根据反应物及所含元素可确定产生的白色沉淀为BaCO3。c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。d.CO被银氨溶液氧化为CO32—,它本身则被还原为Ag单质。疏松的Ag颗粒在室温下为黑色固体。将黑色沉淀用蒸馏水洗净就得到单质Ag。① 实验c的目的是是为了与b形成对照,证明Ba(OH)2溶液不能与银氨溶液反应,实验b中的现象是产物与Ba(OH)2溶液反应导致的。② 根据上述实验现象证明上层清液中含有(NH4)2CO3或NH4+、CO32—。③证明黑色固体是Ag单质实验方案是取少量黑色固体,向其中滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl 溶液,能产生白色沉淀,说明黑色固体为单质银。④根据实验现象可知CO与银氨溶液反应的化学方程式为CO+ 2Ag(NH3)2OH=(NH4)2CO3+2Ag↓+2NH3↑。
CO↑+H2O。在该反应中浓硫酸的作用是脱水性。(2)软管的作用是使分液漏斗的上下气体压强相同,这样分液漏斗中的液体在重力的作用下就可以顺利滴下。(3)甲酸在加热时会挥发,也可能部分CO被氧化为CO2,所以浓NaOH溶液的作用是洗气,吸收酸性气体。(4)a.测得上层清液pH为10,证明溶液为碱性;b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体。证明含有NH4+;同时证明在溶液中含有的离子能与Ba(OH)2电离产生的离子结合形成白色难溶性物质。根据反应物及所含元素可确定产生的白色沉淀为BaCO3。c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。d.CO被银氨溶液氧化为CO32—,它本身则被还原为Ag单质。疏松的Ag颗粒在室温下为黑色固体。将黑色沉淀用蒸馏水洗净就得到单质Ag。① 实验c的目的是是为了与b形成对照,证明Ba(OH)2溶液不能与银氨溶液反应,实验b中的现象是产物与Ba(OH)2溶液反应导致的。② 根据上述实验现象证明上层清液中含有(NH4)2CO3或NH4+、CO32—。③证明黑色固体是Ag单质实验方案是取少量黑色固体,向其中滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl 溶液,能产生白色沉淀,说明黑色固体为单质银。④根据实验现象可知CO与银氨溶液反应的化学方程式为CO+ 2Ag(NH3)2OH=(NH4)2CO3+2Ag↓+2NH3↑。
考点:考查银氨溶液在检测CO气体的应用的实验操作、反应原理及化学方程式的书写的知识。


科目:高中化学 来源: 题型:填空题
海水是巨大的资源宝库。下图是人类从海水资源获取某些重要化工原料的流程示意图。

回答下列问题:
(1)操作A是_________________(填实验基本操作名称)。用何种方法知道海水晒盐的过程中溶液里食盐含量在逐渐提高?________
a.分析氯化钠含量 b.测定溶液密度 c.观察是否有沉淀析出
(2)操作B需加入下列试剂中的一种,最合适的是______(选填编号)。
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳 d.碳酸钠溶液
(3)向苦卤中通入Cl2,发生反应的离子方程式是____________________________,操作C是_______________________________。
(4)上图中虚线框内流程的主要作用是_______________________;与之目的相同的流程在上图中还有几处,试指出其中一处________________________。
(5)将MgCl2转化为Mg时获得的副产品是_____________,用化学方程式表示该物质的某种用途______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(12分)高纯硝酸锶[化学式:Sr(NO3)2]用于制造信号灯、光学玻璃等。
⑴工业级硝酸锶中常含有硝酸钙、硝酸钡等杂质,其中硝酸钙可溶于浓硝酸,而硝酸锶、硝酸钡不溶于浓硝酸。请结合相关信息,补充完整提纯硝酸锶的下列实验步骤:
①取含杂质的硝酸锶样品, ,搅拌。
② 。
③将滤渣溶于水中,加略过量铬酸使Ba2+沉淀,静置后加入肼(N2H4)将过量铬酸还原,调节pH=7~8,过滤。
④将滤液用硝酸调节pH=2~3, ,过滤,洗涤。
⑤将得到的Sr(NO3)2·2H2O晶体在100 ℃条件下干燥,得到高纯硝酸锶。
⑵Sr(NO3)2受热易分解,生成Sr(NO2)2和O2;在500 ℃时Sr(NO2)2进一步分解生成SrO及氮氧化物。取一定质量含Sr(NO2)2的Sr(NO3)2样品,加热至完全分解,得到5.20 g SrO固体和5.08 g混合气体。计算该样品中Sr(NO3)2的质量分数(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(12分)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式:
(2)观察到A中的现象是 _______________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
(4)C中盛放CCl4的作用是 。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入 ,现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(15分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验:
现称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
(1)称量样品所用的仪器为_____(填“托盘天平”或“电子天平”),将样品研细后再反应,其目的是_______ 。
(2)装置a和c的作用分别是____和____(填标号)。
| A.除去SO2气体 | B.除去空气中的水蒸气 | C.有利于气体混合 |
| D.有利于观察空气流速 E.除去反应后多余的氧气 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
制备水杨酸对正辛基苯基酯( )如下:
)如下:
步骤一:将水杨酸晶体投入三颈烧瓶中,再加入氯苯,搅拌溶解后,加入无水三氯化铝。
步骤二:按图12所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2,反应制得水杨酰氯,该反应为: (水杨酸)+SOCl2→
(水杨酸)+SOCl2→ (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑
步骤三:将三颈烧瓶中的混合液升温至80℃,再加入对正辛苯酚( ),温度控制在100℃左右,不断搅拌。
),温度控制在100℃左右,不断搅拌。
步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥。
(1)步骤一中加入三氯化铝的作用是 。
(2)实验时,冷凝管中的水应从 进 出(选填“a”或“b”);装置c的作用是 。
(3)步骤三??发生反应的化学方程式为 。
(4)步骤四减压过滤操作中,除烧杯、玻璃棒外,还必须使用的硅酸盐材料的仪器有 。
(5)步骤四减压过滤时,有时滤纸会穿孔,避免滤纸穿孔的措施是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
牙膏中的摩擦剂一般由CaCO3、Al(OH)3或SiO2组成。某小组对几种牙膏中摩擦剂成分及其含量进行探究:
(1)根据上述信息,推测摩擦剂应具备的性质有
A.易溶于水 B.难溶于水 C.颗粒较大 D.颗粒较小
(2)已知A牌牙膏的摩擦剂是Al(OH)3,取少量牙膏样品,加水充分搅拌、过滤:
①往滤渣中加入过量NaOH溶液,Al(OH)3与NaOH溶液反应的离子方程式____ __。
②往①所得滤液先通入过量CO2,再加入过量稀盐酸,观察到的现象是 。
(3)已知B牌牙膏中摩擦剂可能含有一或两种物质,将此牙膏的摩擦剂溶于盐酸时,发现有不溶性物质。
① 对B品牌牙膏摩擦剂的成分提出合理假设:
假设1:只有SiO2 假设2:可能有SiO2和CaCO3
假设3:可能有________________。
② 请设计方案对B品牌牙膏摩擦剂的成分进行验证。填写下表。限选试剂:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量牙膏样品,加水成分搅拌、过滤,得滤液A和沉淀B。 | |
| 步骤2: | |
| 步骤3: | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
Na2SO3、SO2是中学常见的物质。
(1)某同学用下图示装置制取干燥纯净的SO2。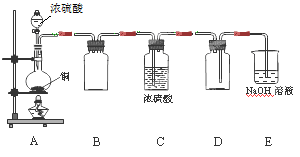
写出制取SO2气体的化学方程式 。请指出D装置中的错误 。若实验过程中不慎在皮肤上沾少量浓硫酸,处理的方法是 。
(2)向烧碱和Na2SO3的混合溶液中加入少量溴水,振荡后溶液变为无色。反应后的溶液中含有大量的SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO32-、SO42-和Br-的实验报告。限选试剂:2 mol/LHCl,1 mol/L H2SO4,l mol/LBaCl2,l mol/LBa(NO3)2,0.1 mol/LAgNO3,CCl4,新制饱和溴水,新制饱和氯水。
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 在试管A中加入少量待测液,加入足量氯水,再加入四氯化碳,振荡,静置后观察颜色。 | ,证明待测液中含Br-。 |
| 步骤② | 在试管B中加入少量待测液, | 有白色沉淀生成, 证明待测液中含SO42-。 |
| 步骤③ | 在试管C中加入少量待测液,滴加2 mol/LHCl至溶液呈酸性,加入几滴______(填试剂),振荡。 | , 证明待测液中含SO32-。 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
乙酰水杨酸俗称阿司匹林(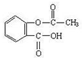 ),是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,其制备原理为:
),是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,其制备原理为:


制备基本操作流程如下:
主要试剂和产品的物理常数如下表:
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |


 ),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为 (百分数精确到0.1)。
),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为 (百分数精确到0.1)。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com