

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题



查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
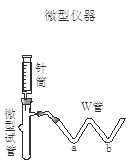
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量固体样品于微型试管中;在W管a处滴入 、b处滴入 ;用胶管将W管与微型试管连接好 | |
| 步骤2:用针筒吸入 ,将针头穿过微型试管的胶塞,向固体样品中注入该溶液。 | 。 |
| 步骤3:拨出针筒,吸入蒸馏水洗净;再吸入 注入微型试管中 | 。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.上下移动①中铜丝可控制SO2的量 |
| B.②中品红溶液不褪色 |
| C.③中石蕊溶液变蓝色 |
| D.为确认CuSO4生成,向①中加水,观察溶液颜色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向盛有1mL 0.01mol·L-1AgNO3溶液的试管中滴加0.01mol·L-1NaCl溶液,至不再有沉淀生成,再向其中滴加 0.01mol·L-1NaI溶液,产生黄色沉淀。 | 常温下,Ksp(AgCl)>Ksp(AgI) |
| B | 常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小 | NH4Cl溶液显酸性 |
| C | 向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色 | 说明溶液中一定含有Fe2+ |
| D | 将少量某物质滴加到新制的氢氧化铜悬浊液中,加热后有红色沉淀生成 | 说明该物质一定是醛 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
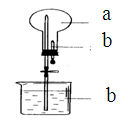
| A.a为HCl,b为H2O |
| B.a为CO2,b为浓NaOH溶液 |
| C.a为Cl2,b为饱和NaCl溶液 |
| D.a为NH3,b为浓NH4Cl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com