
【题目】运用元素周期律分析下面的推断,其中错误的是
A. 氢氧化铯(CsOH)为强碱
B. 砹单质(At2)为有色固体,HAt不稳定
C. 碳酸锶(SrCO3)是难溶于水的固体
D. 硒化氢(H2Se)比硫化氢稳定
科目:高中化学 来源: 题型:
【题目】下列物质结构图中,●代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表除形成共价键外的其他最外层电子,短线代表共价键,如F2:![]() 。
。


⑴试写出四种图示所代表的化学式:
A___________,B___________,C___________,D___________。
⑵将上述四种物质的液体呈细流流下,用带静电的玻璃棒靠近细流,细流发生偏转的是_____________(填“A”“B”“C”“D”)。
⑶B分子中有__________个δ键,___________个π键。
⑷C分子中,中心原子杂化类型____________其分子空间构型是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.AlCl3溶液和NaAlO2溶液分别加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同
B.配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度
C.用加热的方法可除去KNO3溶液中混有的Fe3+
D.泡沫灭火器中常使用的原料是碳酸钠和硫酸铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生反应的原理,用如图装置进行实验。

根据相关知识回答下列问题:
(1)实验开始时,关闭K2,开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。过一会儿,在Ⅲ中可能观察的现象是_________________。(至少答2点)
(2)整套实验装置中能防止倒吸的装置有________(填装置序号)。
(3)烧杯Ⅰ中盛装的溶液为___________,结束后关闭K1,打开K2,,使装置Ⅰ中的溶液倒吸入装置Ⅱ中。这样操作的目的是_____________________。
(4)苯与溴反应的原理__________________。(用方程式表达)
Ⅱ、海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:

(1)指出提取碘的过程中有关的实验操作名称:① ______,③ ________;过程②中还可以选择一种绿色氧化剂_____________代替氯气。写出该氧化剂与含碘离子溶液在酸性条件下反应的离子方程式_________________________________ 。
(2)提取碘的过程中,可供选择的有机试剂是__________________。
A 甲苯、酒精 B 四氯化碳、苯 C 汽油、乙酸 D 汽油、甘油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铁片和浓硫酸混合加热,充分应后得到溶液X,X中除Fe3+外还可能含有Fe2+.若要确认其中的Fe2+,应选用
A. KSCN溶液和氯水
B. 铁粉和KSCN溶液
C. 浓氨水
D. 酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢溶液可作为采矿业废液消毒剂,如消除采矿废液中剧毒的氰化钾,反应方程式为KCN+H2O2+H2O![]() A+NH3↑(已配平),请回答:(提示:
A+NH3↑(已配平),请回答:(提示:![]() 、
、![]() )
)
(1)生成物A的化学式是_____________________________。
(2)该反应是否是氧化还原反应?________(填写“是”或“否”),其理由是_____________________。若是,则被还原的元素是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物X、Y和高聚物Z,可以用烃A为主要原料,采用以下路线合成。
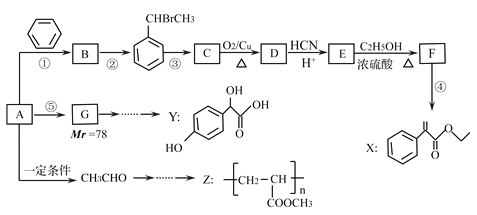
已知:Ⅰ.反应①、反应②的原子利用率均为100%.
Ⅱ.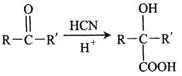 (R或R可以是烃基或氢原子)
(R或R可以是烃基或氢原子)
请回答下列问题:
(1)A的结构简式为____________。
(2)Z中的官能团名称为__________,反应③的条件为___________。
(3)关于药物Y(![]() )的说法正确的是______________。
)的说法正确的是______________。
A.1mol药物Y与足量的钠反应可以生成33.6L氢气。
B.药物Y的分子式为C8H8O4,能使酸性高锰酸钾溶液褪色
C.药物Y中⑥、⑦、⑧三个-OH的酸性由强到弱的顺序是⑧>⑥>⑦
D.1mol药物Y与H2、浓溴水中的Br2反应,最多消耗H2、Br2分别为4mol和2mol
(4)写出反应E→F的化学方程式_________________,F→X的化学方程式______________________。
(5)写出符合下列条件的E的一种同分异构体的结构简式____________。
①遇FeCl3溶液可以发生显色反应,且是苯的对位二元取代物;②能发生银镜反应和水解反应;③核磁共振氢谱有6个峰。
(6)参考上述流程以CH3CHO和CH3OH为起始原料,其它无机试剂任选,设计合成Z的线路。_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,pH=2的HA和HB各1 mL分别加水稀释,pH随溶液体积变化如图所示。下列叙述正确的是

A. Kw的数值:a点大于c点
B. 溶液中的总酸量:a点大于b点
C. HB的电离程度:b点大于c点
D. 将a点与b点两溶液同时升高温度,则![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如右图转化关系(部分生成物和反应条件略去)

下列推断不正确的是( )
A. 若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
B. 若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,E一定能还原Fe2O3
C. 若D为CO,C能和E反应,则A一定为Na2O2,其电子式是![]()
D. 若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com