
| A、氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
| B、2L 0.5 mol?L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C、1mol Na2O2固体中含离子总数为4NA |
| D、5NH4NO3═2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA |
| 1 |
| 4 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、KMnO4酸性溶液 |
| B、溴水 |
| C、NaOH溶液 |
| D、FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、在核电站厂区,较多使用的安全标识是图2 |
| B、在垃圾分类中,废电池属于图4 |
C、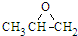 和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物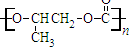 ,反应符合绿色化学的原则 ,反应符合绿色化学的原则 |
| D、图5 装置内发生的反应有化合、分解和置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
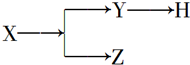 如图表示一些物质间的从属关系,不正确的是( )
如图表示一些物质间的从属关系,不正确的是( )
| X | Y | Z | H | |
| A | 分散系 | 胶体 | 溶液 | 烟 |
| B | 元素周期表的纵行 | 主族 | 副族 | 卤族 |
| C | 电解质 | 酸 | 碱 | 盐 |
| D | 化合物 | 共价化合物 | 离子化合物 | 酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.8克乙烯和丙烯的混合气体中所含碳原子数为0.2 NA |
| B、0.1mol CnH2n+2含有C-C数为0.1nNA个 |
| C、标准状况下,22.4L CCl4含有NA个CCl4分子 |
| D、1mol苯乙烯含有的C=C数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com