
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是( )

A. 反应的化学方程式为:2M![]() N
N
B. t2时,正逆反应速率相等,达到平衡
C. t3时,正反应速率大于逆反应速率
D. t1时,N的浓度是M浓度的2倍
科目:高中化学 来源: 题型:
【题目】有机物的结构简式如图: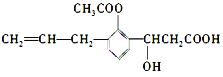 。则此有机物可发生的反应类型有 ( )
。则此有机物可发生的反应类型有 ( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和 ⑧加聚
A. ①②③⑤⑥ B. ②③④⑤⑥⑧ C. ②③④⑤⑥⑦ D. ①②③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是K的合成路线。

(1)按官能团分类,A的类别是__________。
(2)A→B的化学方程式是____________________。
(3)C→D所需的试剂a是__________。
(4)检验F存在的试剂及现象是__________。
(5)F→G的反应类型是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的比较顺序中,不正确的是![]()
A. 热稳定性:HF<HCl<HBr<HI B. 微粒半径:K+>Na+>Mg2+>Al3+
C. 酸性:HClO4>H2SO4>H3PO4>H2SiO3 D. 最外层电子数:Li<Mg<Si<Ar
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有资料显示过量的NH3和Cl2在常温下可合成岩脑砂(主要成分为NH4Cl),某实验小组对该反应进行探究,并对岩脑砂进行元素测定,回答下列问题:

(1)岩脑砂的制备
①利用装置A制取实验所需的NH3,写出反应的化学方程式:______。
②已知该实验中用浓盐酸与MnO2反应制取所需Cl2,装罝F中的试剂是饱和食盐水,则F装置的作用是___。
③为了使NH3和Cl2在D中充分混合,请确定上述装置的合理连接顺序:___→e f←h←g←j←i←b(用小写字母和箭头表示,箭头方向与气流方向一致)。
④证明NH3和Cl2反应生成的岩脑砂中含有NH4+,需要用到的实验用品中除了蒸馏水、稀HNO3、红色石蕊试纸外,还需要用到的试剂有___。(填试剂的化学式也可以)
(2)岩脑砂中元素的测定:准确称取a g岩脑砂,与足量的氧化铜混合加热,利用下列装置测定岩脑砂中氮元素和氯元素的物质的量之比。
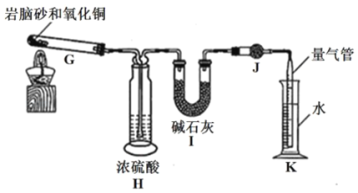
(已知该过程发生的反应为:2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O)
3Cu+N2↑+2HCl↑+3H2O)
⑤设置装置H的目的是___。
⑥若装置I增重b g,利用装置K测得气体体积为V L(已知常温常压下的气体摩尔体积为24.5Lmol﹣1),则岩脑砂中n(N):n(Cl)=___(用含b、V的代数式表示,不必化简)。
⑦若测量体积时气体温度高于常温(其他操作均正确),则n(N)比正常值____(“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性。
【制备FeBr2固体】
实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时,先将干燥、纯净的CO2气流通入D中,再将铁粉加热至600—700℃,E管中铁粉开始反应。不断将d中液溴滴入温度为100—120℃的D中,经过一段时间的连续反应,在不锈钢管内产生黄绿色鳞片状溴化亚铁。

(1)若在A中盛固体CaCO3,a中盛有6 mol/L的盐酸。为使导入D中的CO2为干燥纯净的气体,则图中B、C处的洗气瓶中装有的试剂分别是:B中为____________,C中为_________________。
若进入E装置中的CO2未干燥,则可能发生的副反应的化学方程式为_____________________。
(2)E管中的反应开始前通入CO2的主要作用是__________________________________;
E管中的反应开后持续通入CO2的主要作用是______________________________________。
【探究FeBr2的还原性】
(3)现实验需要90 mL 0.1 mol/L FeBr2溶液,取上述反应制得的FeBr2固体配制该溶液,所需仪器除烧杯、量筒、玻璃棒外,还需要的玻璃仪器是_______________________________。
(4)已知:Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色。Cl2既能氧化Br-,也能氧化Fe2+。
取10 mL上述FeBr2溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为血红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。
以上实验结论表明还原性:Fe2+__________Br-(填“>”或“<”)。
(5)若在40 mL上述FeBr2溶液中通入标准状况下67.2 mL的 C12,取少量反应后的溶液加入CCl4,振荡后下层液体呈______色,写出该反应的离子方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:HmD>HmC;②Cm-、E(m-1)-具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式_________。
(2)Cm-、E(m-1)-的还原性强弱顺序为:___,(用离子符号表示)能证明其还原性强弱的离子方程式为______。
(3)将E的单质通入A与D形成的化合物的水溶液中,在常温下反应的离子方程式为:_______。
(4)常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液按体积比1:2混合,写出该反应的离子方程式_____。该溶液的溶质含有的化学键类型是_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有下列几组物质,请将序号填入下列空格内:
A、CH2=CH-COOH和油酸(C17H33COOH) B、12C60和石墨
C、![]() 和
和![]()
D、35Cl和37Cl E、乙醇和乙二醇
①互为同位素的是__________;
②互为同系物的是______________;
③互为同素异形体的是______;
④互为同分异构体的是__________;
(2)请写出下列反应的化学方程式:
①由丙烯制取聚丙烯:_____________________________________
②丙氨酸缩聚形成多肽:___________________________________
③淀粉水解:_____________________________________________
④丙醛与新制的氢氧化铜悬浊液反应:_______________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com