
【题目】钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图所示。下列说法不正确的是( )

A.盐酸的浓度越大,腐蚀速率越快
B.碳素钢的腐蚀速率不随硫酸的浓度增大而增大,说明反应速率不与c(H+)成正比
C.钼酸钠和月桂酰肌氨酸的浓度相等时,腐蚀速率最小
D.对比盐酸和硫酸两条曲线,可知Cl-也可能会影响碳素钢的腐蚀速率
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
【题目】中学化学常见物质存在转化关系:A+B→C+D+H2O,其中C属于盐类,下列推断不正确的是
A.若A为黄绿色气体,则D可能有漂白性
B.若A为红色金属单质,则D一定是红棕色气体
C.若A为纯碱,则D一定能使澄清石灰水变浑浊
D.若A为氯化铵,则D一定是具有刺激性气味的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑色冶金工业中除了铁、锰、铬、钒、钛以及这些金属的黑色金属合金以外,其他的金属,都算是有色金属。
![]() 基态钛原子的结构示意图为________;基态铬原子的价层电子排布式为________。
基态钛原子的结构示意图为________;基态铬原子的价层电子排布式为________。
![]() 中C、N的电负性关系为C________
中C、N的电负性关系为C________![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() ;
;![]() 的沸点比
的沸点比![]() 的沸点低,其原因是________。
的沸点低,其原因是________。
![]() 中C原子的杂化方式为________;
中C原子的杂化方式为________;![]() 分子是________
分子是________![]() 填“极性”或“非极性”
填“极性”或“非极性”![]() 分子;
分子;![]() 分子中
分子中![]() 键与
键与![]() 键的数目之比为________。
键的数目之比为________。
![]() 金属锰的一种晶体为面心立方最密堆积,其晶胞中有________个锰原子,每个锰原子周围紧邻的锰原子有________个。
金属锰的一种晶体为面心立方最密堆积,其晶胞中有________个锰原子,每个锰原子周围紧邻的锰原子有________个。
![]() 因
因![]() 和
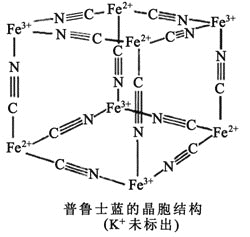
和![]() 外围有较多能量相近的空轨道,故能与一些分子或离子形成配合物。如图为普鲁士蓝配合物晶体结构的示意图
外围有较多能量相近的空轨道,故能与一些分子或离子形成配合物。如图为普鲁士蓝配合物晶体结构的示意图![]() 每两个立方体中,一个
每两个立方体中,一个![]() 在其中一个立方体中心,另一个则无
在其中一个立方体中心,另一个则无![]() ,其化学式是________。
,其化学式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl22H2O的流程如下:

(1)毒重石用盐酸浸取前需充分研磨,目的是____________________。实验室用37%的盐酸配制15%的盐酸,除量筒外还需使用下列仪器中的______________。
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)加入NH3H2O调节pH=8可除去_____(填离子符号),滤渣Ⅱ中含______(填化学式)。加入H2C2O4时应避免过量,原因是_________________。
已知:Ksp(BaC2O4)=1.6×10﹣7,Ksp(CaC2O4)=2.3×10﹣9
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42﹣+2H+═Cr2O72﹣+H2O Ba2++CrO42﹣═BaCrO4↓
步骤Ⅰ:移取x ml一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b molL﹣1盐酸标准液滴定至终点,测得滴加的盐酸体积为V0 mL。
步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b molL﹣1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL。
滴加盐酸标准液时应使用酸式滴定管,“0”刻度位于滴定管的______________(填“上方”或“下方”)。BaCl2溶液的浓度为______________ molL-1,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将______________(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是
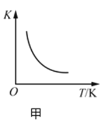
A.图甲表示反应![]() 的平衡常数K与温度的关系,说明该反应的
的平衡常数K与温度的关系,说明该反应的![]()
B.图乙表示Cu与过量浓硝酸反应生成的![]() 气体体积随时间的变化关系,说明该反应在
气体体积随时间的变化关系,说明该反应在![]() 时间段内反应速率最快
时间段内反应速率最快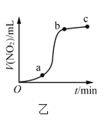
C.图丙表示一定温度下![]() 和NiS的沉淀溶解平衡曲线,说明该温度下,
和NiS的沉淀溶解平衡曲线,说明该温度下,![]() 时,两者的
时,两者的![]() 相等
相等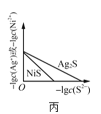
D.图丁表示相同温度下,![]() 的HF和
的HF和![]() 溶液分别加水稀释时pH的变化曲线,说明加水稀释前HF的电离程度大于
溶液分别加水稀释时pH的变化曲线,说明加水稀释前HF的电离程度大于![]() 的电离程度
的电离程度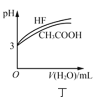
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化如图所示,则下列说法中正确的是
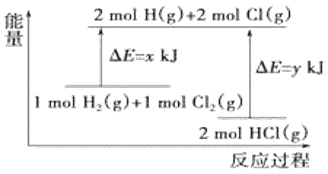
A.该反应是吸热反应
B.断裂1molH-H键和1molCl-Cl键时能放出x kJ的能量
C.断裂2molH-Cl键时需要吸收y kJ的能量
D.2molHCl(g)的总能量高于1molH2(g)和1molCl2(g)的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组进行下列实验:
①将0.1mol·L-1MgCl2溶液和0.5mol·L-1NaOH溶液等体积混合得到浊液
②取少量①中浊液,滴加0.1mol·L-1FeCl3溶液,出现红褐色沉淀
③将①中浊液过滤,取少量白色沉淀,滴加0.1mol·L-1FeCl3溶液,白色沉淀变为红褐色沉淀
④另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解
下列说法中不正确的是( )
A.将①中所得浊液过滤,所得滤液中含少量Mg2+
B.①中浊液中存在沉淀溶解平衡:Mg(OH)2(s)![]() Mg2+(aq)+2OH-(aq)
Mg2+(aq)+2OH-(aq)
C.实验②和③均能说明Fe(OH)3比Mg(OH)2难溶
D.NH4Cl溶液中的NH![]() 可能是④中沉淀溶解的原因
可能是④中沉淀溶解的原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国亚利桑那州大学和阿贡国家实验室的科学家最近设计出生产氢气的人造树叶,原理为2H2O(g) ![]() 2H2(g)+O2(g)。有关该反应的说法错误的是( )
2H2(g)+O2(g)。有关该反应的说法错误的是( )
A.没有人造树叶和太阳能的作用该反应不能自发进行
B.该反应最终是将太阳能转化为电能
C.该反应为充分利用太阳能开辟了广阔前景
D.氢能是理想的绿色能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是A、B、C、D四种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色;②比例模型为 |
B | ①由C.H两种元素组成;②球棍模型为 |
C | ①由C.H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与D反应生成相对分子质量为88的酯 |
D | ①由C.H、O三种元素组成;②球棍模型为 |
回答下列问题:
(1)A与溴的四氯化碳溶液反应的化学方程式为:___;反应类型___。
(2)B具有的性质是___(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
(3)C所含官能团的名称是___,D所含官能团的名称是___,C和D发生酯化的反应方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com