
【题目】美国亚利桑那州大学和阿贡国家实验室的科学家最近设计出生产氢气的人造树叶,原理为2H2O(g) ![]() 2H2(g)+O2(g)。有关该反应的说法错误的是( )
2H2(g)+O2(g)。有关该反应的说法错误的是( )
A.没有人造树叶和太阳能的作用该反应不能自发进行
B.该反应最终是将太阳能转化为电能
C.该反应为充分利用太阳能开辟了广阔前景
D.氢能是理想的绿色能源
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】香草酸广泛用于食品调味剂, 作香精、 香料, 合成线路如下:
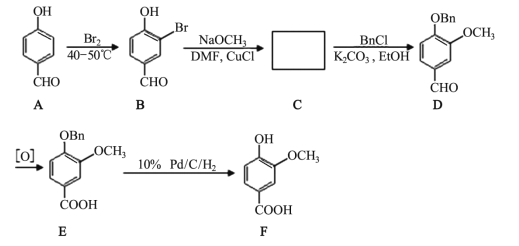
(1)C 的结构简式是_____, B 转化为 C 的反应类型为_____。
(2)A 中含有的官能团名称是_____。
(3)B 的分子式是_____。
(4)在 B 中滴入 FeCl3溶液, 其现象是_____。
(5)与 F 官能团相同的芳香族化合物的同分异构体有_____种。
(6)写出 F 与乙醇进行酯化反应的方程式_____。
(7)写出由 的合成线路图_____。
的合成线路图_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图所示。下列说法不正确的是( )

A.盐酸的浓度越大,腐蚀速率越快
B.碳素钢的腐蚀速率不随硫酸的浓度增大而增大,说明反应速率不与c(H+)成正比
C.钼酸钠和月桂酰肌氨酸的浓度相等时,腐蚀速率最小
D.对比盐酸和硫酸两条曲线,可知Cl-也可能会影响碳素钢的腐蚀速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个绝热定容的密闭容器中,1molA与2molB发生反应A(g)+2B(g) ![]() xC(g)+2D(g) △H=bkJ·mol1(b<0),下列说法不正确的是
xC(g)+2D(g) △H=bkJ·mol1(b<0),下列说法不正确的是
A.平衡时,A和B的转化率相等
B.若 x=1,容器中压强不变时不能判断反应达到平衡
C.当B和D的物质的量之比1:1不变时,表明该反应已达到平衡
D.达到平衡过程中,正反应速率可能是先增大再减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钠(Na2Cr2O7·2H2O)俗称红矾钠,在工业方面有广泛用途。我国目前主要是以铬铁矿(主要成份为FeO、Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下:
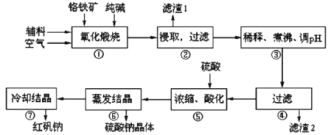
①中涉及的主要反应有:
主反应:4FeO·Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3![]() Na2SiO3+CO2↑、Al2O3+Na2CO3
Na2SiO3+CO2↑、Al2O3+Na2CO3![]() 2NaAlO2+CO2↑
2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
试回答下列问题:
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是________。
(2)“③”中调节pH至4.7,目的是________。
(3)“⑤”中加硫酸酸化的目的是使![]() 转化为
转化为![]() ,请写出该平衡转化的离子方程式:________。
,请写出该平衡转化的离子方程式:________。
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶(锥形瓶)中,加入10mL2mol·L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol·L-1Na2S2O3标准溶液滴定(I2+2![]() =2I-+
=2I-+![]() )。
)。
①判断达到滴定终点的依据是:________;
②若实验中共用去Na2S2O3标准溶液40.00mL,所得产品的中Na2Cr2O7的纯度(设整个过程中其它杂质不参与反应)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,体积为2L的密闭容器中,1molX和3molY进行反应:X(g)+3Y(g)![]() 2Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是( )
2Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是( )
A.以X浓度变化表示的反应速率为1/8mol/(L·S)
B.12s后将容器体积扩大为10L,Z的平衡浓度变为原来的1/5
C.若增大X的浓度,则物质Y的转化率减小
D.若该反应的△H<0 ,升高温度,平衡常数K减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S16O2与18O2在高温条件下发生反应2SO2+O2![]() 2SO3,达到化学平衡后,平衡混合物中含18O的微粒( )
2SO3,达到化学平衡后,平衡混合物中含18O的微粒( )
A. 只有SO3 B. 只有SO2、SO3 C. 有SO2、SO3、O2 D. 只有O2、SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li/Li2O体系的能量循环图如图所示。已知,△H4>0。下列说法正确的是
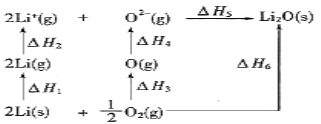
A. △H3<0
B. △H3+△H4+△H5=△H6
C. △H6>△H5
D. △H1+△H2+△H3+△H4+△H5+△H6=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应:2SO3(g) ![]() 2SO2(g)+O2(g)、2NO(g)+O2(g)
2SO2(g)+O2(g)、2NO(g)+O2(g) ![]() 2NO2(g) (不考虑NO2和N2O4之间的相互转化),当加入一定量的SO3使上述系统达到平衡时,n(O2)=0.1 mol、n(NO2)=3.6 mol,则此时SO2气体的物质的量为( )
2NO2(g) (不考虑NO2和N2O4之间的相互转化),当加入一定量的SO3使上述系统达到平衡时,n(O2)=0.1 mol、n(NO2)=3.6 mol,则此时SO2气体的物质的量为( )
A.0.1 molB.3.6 molC.1.8 molD.3.8 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com