
【题目】按如图所示装置进行下列不同的操作,其中不正确的是

A. 铁腐蚀的速度由大到小的顺序:只闭合K3>只闭合K1>都断开>只闭合K2
B. 只闭合K3,正极的电极反应式:2H2O+O2+4e-=4OH-
C. 先只闭合K1,一段时间后,漏斗内液曲上升,然后再只闭合K2,漏斗内液面上升
D. 只闭合K2,U型管左、右两端液面均下降
【答案】A
【解析】A、金属腐蚀速率:电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极,闭合K3,是原电池,铁作负极:闭合K2,是电解池,铁作阴极;闭合K1,铁作阳极,因此腐蚀速率是只闭合K1>只闭合K3>都断开>只闭合K2,故A说法错误;B、B、只闭合K3,构成吸氧腐蚀,正极:O2+2H2O+4e-=4OH-,故B说法正确;C、只闭合K1,铁作阳极,阳极反应式为Fe-2e-=Fe2+,阴极反应式为2H++2e-=H2↑,U型管中气体压强增大,因此漏斗中液面上升,然后闭合K2,铁作阴极,阴极反应式为2H++2e-=H2↑,阳极反应式2Cl-2e-=Cl2↑,U型管中气体压强增大,漏斗中液面上升,故C说法正确;D、根据选项C的分析,铁作阴极,阴极反应式为2H++2e-=H2↑,阳极反应式2Cl-2e-=Cl2↑,故D说法正确。


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】2g碳与水蒸气反应生成CO和H2,需吸收21.88kJ热量,此反应的热化学方程式为
A. C + H2O ==CO + H2ΔH =+131.3kJ·mol—1
B. C(s)+ H2O(g) ==CO(g) + H2(g)ΔH =+10.94kJ·mol—1
C. C(s)+ H2O(g) ==CO(g) + H2(g)ΔH = -131.3kJ·mol—1
D. C(s)+ H2O(g) ==CO(g) + H2(g)ΔH = +131.3kJ·mol—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在稀溶液中:1mol弱酸HX与1molNaOH反应的反应热△H=-12.1kJ/mol;HCl与NaOH反应的中和热△H=-55.6kJ/mol。则HX在稀溶液中的电离热△H等于(单位:kJ/mol)
A. +43.5 B. -43.5 C. -67.7 D. +67.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,甲充有二氧化氮(N2O4![]() 2NO2 △ H > 0);乙充有空气,现分别进行下列两个实验:
2NO2 △ H > 0);乙充有空气,现分别进行下列两个实验:
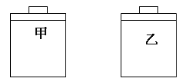
(a)将两容器置于沸水中加热
(b)在活塞上都加2 kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是 ( )
A.(a)甲>乙,(b)甲>乙 B.(a)甲>乙,(b)甲=乙
C.(a)甲<乙,(b)甲>乙 D.(a)甲>乙,(b)甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温条件下将Cl2缓缓通入NH3中,反应生成NH4Cl和N2.下列说法正确的是
A. 反应过程中无明显现象 B. 反应为放热反应
C. 每有3molCl2反应,被氧化NH3为8mol D. NH4Cl是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。
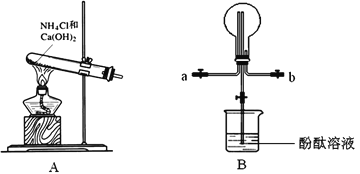
请回答:
(1)实验室制备氨气的化学方程式为 ;干燥氨气常用的干燥剂是 。
(2)收集氨气时,请你选择氨气的进气口 (填“a”或“b”),理由是 。
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是 。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是 ( 填序号)。
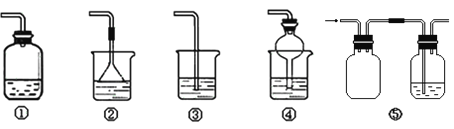
(5)氨气在催化剂并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp (CaC2O4)=4.010-9,若在c(Ca2+)=0.020mol·L-1的溶液生成CaC2O4沉淀,溶液中的c(C2O42-)最小应为( )
A. 4.010-9mol·L-1 B. 2.010-7mol·L-1 C. 2.010-9mol·L-1 D. 8.010-11mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年11月5 日,长征三号乙运载火箭将两颗北斗三号全球导航卫星送入太空轨道。下列有关说法正确的是
A. 火箭燃料中的四氧化二氮属于化石燃料 B. 火箭燃料燃烧时将化学能转化为热能
C. 火箭箭体采用铝合金是为了美观耐用 D. 卫星计算机芯片使用高纯度的二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应aA(s)+bB(g ![]() cC(g)+dD(g)达到平衡时,B%跟压强P和温度T(T2>T1)之间的关系如图所示(填“增大”“减小”“吸”“放”“正”“逆”)
cC(g)+dD(g)达到平衡时,B%跟压强P和温度T(T2>T1)之间的关系如图所示(填“增大”“减小”“吸”“放”“正”“逆”)

①当压强不变时,升高温度,B%变______,其反应为_______热反应。
②当温度不变,增大压强时,B%变_______,平衡向______方向移动,方程式中系数间关系是_____。
③当温度不变,增大压强时,若B%不变,则方程式中系数关系是____ _。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com