
【题目】某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
(1)配制0.50mol/L NaOH溶液
a.若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体 g.
b.从图中选择称量NaOH固体所需要的仪器是(填字母): .
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
(2)测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.
a.写出该反应的热化学方程式(中和热为57.3kJ/mol): .
b.取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如下表.
①请填写下表中的空白:
温度 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2﹣t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3 , 中和后生成溶液的比热容c=4.18J/(g℃).则中和热△H=(取小数点后一位).
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母) .
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
【答案】
(1)5.0;a b e
(2)![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;﹣53.5kJ/mol;acd
Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;﹣53.5kJ/mol;acd
【解析】解:(1)a.需要称量NaOH固体m=nM=cVM=0.5mol/L×0.25L×40g/mol=5.0g,所以答案是:5.0;b.氢氧化钠要在称量瓶或者小烧杯中称量,称量固体氢氧化钠所用的仪器有天平、烧杯和药匙,所以答案是:a b e;(2)a.已知稀强酸、稀强碱反应生成1mol液态水时放出57.3kJ的热量,稀硫酸和氢氧化钡钠稀溶液都是强酸和强碱的稀溶液,则反应的热化学方程式为: ![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol,所以答案是:
Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol,所以答案是: ![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;b.①温度差平均值=
Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;b.①温度差平均值= ![]() ,但是第2组数据明显有误,所以删掉,温度差平均值
,但是第2组数据明显有误,所以删掉,温度差平均值 ![]() =4.0°C,所以答案是:4.0;
=4.0°C,所以答案是:4.0;
②50mL0.50mol/L氢氧化钠与30mL0.50mol/L硫酸溶液进行中和反应生成水的物质的量为0.05L×0.50mol/L=0.025mol,溶液的质量为:80ml×1g/ml=80g,温度变化的值为△T=4℃,则生成0.025mol水放出的热量为Q=mc△T=80g×4.18J/(g℃)×4.0℃=1337.6J,即1.3376KJ,所以实验测得的中和热△H=﹣ ![]() =﹣53.5 kJ/mol,所以答案是:﹣53.5kJ/mol;③a.实验装置保温、隔热效果必须好,否则影响实验结果,故a正确; b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,放出的热量偏高,则大于57.3kJ/mol,故b错误; c.尽量一次快速将NaOH溶液倒入盛有硫酸的小烧杯中,不允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中,故c正确; d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度,故d正确.所以答案是:acd.
=﹣53.5 kJ/mol,所以答案是:﹣53.5kJ/mol;③a.实验装置保温、隔热效果必须好,否则影响实验结果,故a正确; b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,放出的热量偏高,则大于57.3kJ/mol,故b错误; c.尽量一次快速将NaOH溶液倒入盛有硫酸的小烧杯中,不允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中,故c正确; d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度,故d正确.所以答案是:acd.


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
【题目】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入6molL﹣1 H2SO4溶液中,乙同学将电极放入6molL﹣1的NaOH溶液中,如图所示.
请回答:
(1)写出甲池中正极的电极反应式: .
(2)写出乙池中负极的电极反应式和总反应的离子方程式:负极 , 总反应的离子方程式为 .
(3)由此实验,可得到如下哪些正确结论?(填写字母序号).a.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
b.镁的金属性不一定比铝的金属性强
c.该实验说明金属活动性顺序已过时,已没有实用价值
d.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
(4)上述实验也反过来证明了“直接利用金属活动性顺序判断原电池中的正负极”,这种做法(填“可靠”或“不可靠”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是炼钢和炼铜的主要原料,在高温下灼烧生成三氧化二铁和氧化亚铜.三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某学校化学兴趣小组通过实验来探究﹣红色粉末是Fe2O3、Cu2O或两者的混合物,探究过程如下:[查阅资料]Cu2O溶于稀硫酸生成Cu和CuSO4 , 在空气中加热生成CuO.
[提出假设]假设1:红色粉末是Fe2O3 .
假设2:红色粉末是Cu2O.
假设3:红色粉末是Fe2O3和Cu2O的混合物.
[提出探究实验]取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂.
(1)若假设1成立,则实验现象是 .
(2)滴加KSCN试剂后溶液不变红色,某同学认为原固体粉末中一定不含三氧化二铁,你认为这种说法合理吗? . 简述你的理由(不需要写出反应的化学方程式) .
(3)若固体粉末完全溶液无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是 , 写出发生的氧化还原反应的离子方程式: .
(4)[探究延伸]经试验分析,确定红色粉末为Fe2O3和Cu2O的混合物.实验小组称取3.04g该红色粉末,设计如下实验方案进行实验.经查资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
开始沉淀时的pH | 6.0 | 7.5 | 1.4 |
沉淀完全时的pH | 13 | 14 | 3.7 |
步骤Ⅰ:将3.04g红色粉末溶于足量稀硫酸中,再加入足量H2O2溶液,振荡,得澄清透明溶液X.
步骤Ⅱ:在溶液X中加入适量Cu(OH)2粉末,调节溶液pH=4.0,过滤,得红褐色沉淀Y和滤液Z.
步骤Ⅲ:将沉淀Y充分灼烧,得1.6g红色固体M.
步骤Ⅳ:将滤液Z蒸发浓缩,冷却结晶,过滤,得6.0gCuSO45H2O晶体.
①沉淀Y的化学式为 .
②步骤Ⅳ中不需要用到的实验仪器 .
a.烧杯b.玻璃棒c.分液漏斗d.酒精灯e.铁架台(带铁圈)f.托盘天平g.量筒h.蒸发皿i.容量瓶.
③红色粉末样品中Cu2O的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,0.1molL﹣1的HA溶液中 ![]() =1×10﹣8 , 下列叙述中正确的是( )
=1×10﹣8 , 下列叙述中正确的是( )
A.0.01 molL﹣1HA的溶液中 c(H+)=l×l0﹣4molL﹣1
B.pH=3的HA溶液与pH=ll的NaOH溶液等体积混合后所得溶液中:c(Na+)=c(A﹣)>c(OH﹣)=c(H+)
C.浓度均为0.1 molL﹣1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(H+)﹣c(OH﹣)>c(A﹣)﹣c(HA)
D.pH=3的HA溶液与pH=11的NaOH溶液混合后所得溶液显碱性,则 c(Na+)>c(A﹣)>c(OH﹣)><c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表述正确的是( )
A.质量数为16的氧原子: ![]() O
O
B.漂白粉的有效成分:NaClO
C.Mg2+结构示意图: ![]()
D.钠在氧气中燃烧的化学方程式:4Na+O2 ![]() 2Na2O
2Na2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可利用“甲烷蒸气转化法生产氢气”,反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:

图1(水碳比为3) 图2(800℃)
(1)CH4(g)+H2O(g)![]() CO(g)+3H2(g) 的△H_______0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将_____________移动(填“向正应方向”、“向逆反应方向”或“不”)。
CO(g)+3H2(g) 的△H_______0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将_____________移动(填“向正应方向”、“向逆反应方向”或“不”)。
(2)温度对该反应的反应速率和平衡移动的影响是_______________________。
(3)其他条件不变,请在图2中画出压强为2 MPa时,甲烷平衡含量(%)与水碳比之间关系曲线___________。(只要求画出大致的变化曲线)
(4)已知:在700℃,1MPa时,1mol CH4与1mol H2O在2L的密闭容器中反应,6分钟达到平衡,此时CH4的转化率为80%,求这6分钟H2的平均反应速率和该温度下反应的平衡常数是多少________?(写出计算过程,结果保留小数点后一位数字。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下海带提碘的实验方案可以缩短实验时间,避免Cl2和CCl4的毒性.其实验流程如下: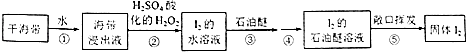
回答下列问题:
(1)步骤①的操作名称是;所需玻璃仪器有玻璃棒、烧杯和 .
(2)步骤②中加入H2O2后发生反应的化学方程式为;选择用H2O2做氧化剂的原因是 .
(3)检验I2的水溶液中含有单质碘的方法是,取样于试管中,加入淀粉,如溶液显色,则可证明含有碘单质.
(4)步骤③的操作名称是;石油醚能用作萃取剂,说明石油醚具有的性质是 .
(5)步骤⑤通过敞口挥发就能得到固体碘,说明石油醚具有良好的 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用软锰矿浆(主费成分是MnO2)吸收工业要气中的SO2,并制备硫酸锰的生产流程如下(浸出液的pH<2,其中除含Mn2+外。还含有少量Fe2+、Al3+、Ca2+等金属离子):
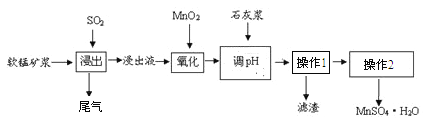
操作1的滤液通过阳离子吸附剂除去Ca2+。金属离子形成氢氧化物沉淀时的pH见下表:
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe2+ | 7.6 | 9.7 |
Fe3+ | 2.7 | 3.7 |
Al3+ | 3.8 | 4.7 |
Mn2+ | 8.3 | 9.8 |
请回答下列问题:
(1)浸出过程中被氧化的物质的化学式为____________________________。
(2)氧化过程中主要反应的离子方程式_________________________________。
(3)在氧化后的液体中加入石灰浆调节pH,pH的范围是_____________________。
(4)操作1的名称是________,操作2包括蒸发浓缩、______过滤、洗涤、干燥等操作。
(5)为测定所得MnSO4·H2O的纯度,准确称取上述样品1.720g加入适量H2SO4和NH4NO3溶液,加热使Mn2+全部氧化成Mn3+后,配成200mL溶液。取20.00mL该溶液,向其中逐滴加入0.0500mol/L的FeSO4溶液,发生如下反应:Fe2++Mn3+=Fe3++Mn2+。当反应恰好完全进行时,共消耗FeSO4溶液19.50mL。通过计算确定MnSO4·H2O的纯度(写出计算过程)_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com