
【题目】实验室制取并收集氯气的装置如图所示,请回答下列问题
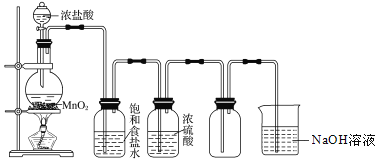
(1)气体发生装置中进行的反应化学方程式是______。
(2)在装置中:①饱和食盐水的作用是______,②浓硫酸的作用是______。
(3)化学实验中检验是否有![]() 产生常用湿润的淀粉
产生常用湿润的淀粉![]() 试纸
试纸![]() 如果有
如果有![]() 产生,可观察到的现象是______。
产生,可观察到的现象是______。
(4)写出尾气吸收装置中进行的反应的离子方程式______。
【答案】4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O 除去氯气中的氯化氢气体,降低氯气的溶解度 吸收水蒸气干燥氯气 淀粉碘化钾试纸变蓝 Cl2+2OH=Cl+ClO+H2O
MnCl2+Cl2↑+2H2O 除去氯气中的氯化氢气体,降低氯气的溶解度 吸收水蒸气干燥氯气 淀粉碘化钾试纸变蓝 Cl2+2OH=Cl+ClO+H2O
【解析】
(1)实验室用浓盐酸和二氧化锰在加热的条件下制取氯气;
(2)制取的氯气中含有水蒸气和挥发出来的氯化氢气体,据此分析;
(3)氯气可置换出碘单质,碘单质遇淀粉变色;
(4)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水。
(1)实验室用浓盐酸和二氧化锰在加热的条件下制取氯气,化学方程式为:4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)制取的氯气中含有水蒸气和挥发出来的氯化氢气体,饱和食盐水是用来除去氯气中的氯化氢气体,降低氯气的溶解度,浓硫酸干燥氯气吸收水蒸气得到干燥的氯气;
(3)氯气具有氧化性,遇到湿润的淀粉碘化钾试纸,会将碘离子氧化为碘单质,遇淀粉变蓝,可观察到湿润的淀粉碘化钾试纸变蓝;
(4)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH=Cl+ClO+H2O。


科目:高中化学 来源: 题型:
【题目】将0.1 mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时都会引起( )
A. CH3COOH电离程度变大 B. 溶液pH减小 C. 溶液的导电能力减弱 D. 溶液中c(H+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg、Al、Fe 三种金属的混合物与足量的稀硫酸反应,生成 2.8L H2(标准状况)则三种金属的物 质的量之和不可能是( )
A.0.12 molB.0.15 molC.0.09 molD.0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G、H、I九种物质,其中A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G、F是单质,其余均为化合物,H是一种淡黄色固体,它们的转化关系如图所示。请回答:

(1)画出G离子结构示意图________;
(2)写出B、I的化学式B________,I________;
(3)写出H的一种用途__________________________________;
(4)写出A受热分解的化学方程式_________________________;
(5)若H与C反应固体增重4.2 g,则参加反应的C气体在标准状况下的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1 mol X气体和0.5 mol Y气体混合于2 L密闭容器中,发生如下反应:3X(g)+Y(g)![]() nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
(1)前2 min内,用X表示的平均反应速率________;
(2)2 min末时Y的转化率________;
(3)化学方程式中Z的化学计量数n________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用钛白工业的副产品FeSO4(含TiO2+、Al3+)可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:

已知:
①过滤1得到的滤渣的主要成分是Al(OH)3、H2TiO3。
②5Fe2++ MnO4-+8H+=5Fe3+ +Mn2++4H2O
5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有_____。
(2)沉淀反应的离子方程式是______________。
(3)实验室测定高纯超微细草酸亚铁组成的步骤依次为:
步骤1:准确称量一定量草酸亚铁样品,加入30 mL 2 mol·L-1的H2SO4溶解。
步骤2:用0.2000 mol·L-1标准KMnO4溶液滴定,消耗其体积31.60 mL。
步骤3:向滴定后的溶液中加入3g Zn粉和8 mL 2 mol·L-1的H2SO4溶液,将Fe3+还原为Fe2+。
步骤4:过滤,滤液用上述标准KMnO4溶液滴定,消耗溶液10.00 mL。
则样品中C2O42-的物质的量为______。(写出计算过程)
(4)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如下图,其变化趋势的原因可能为________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粮食仓储常用磷化铝(AlP)熏蒸杀虫,AlP遇水即产生强还原性的PH3气体。国家标准规定粮食中磷化物(以PH3计)的残留量不超过0.05mg·kg-1时为合格。某小组同学用图所示实验装置和原理测定某粮食样品中磷化物的残留量。C中加入100g原粮,E中加入20.00mL 2.50×10-4mol·L-1KMnO4溶液(H2SO4酸化),C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中的溶液。
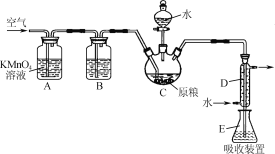
(1)装置A中的KMnO4溶液的作用是________。
(2)装置B中盛装焦性没食子酸的碱性溶液吸收空气中的O2。若去掉该装置,则测得的磷化物的残留量________(填“偏高”“偏低”或“不变”)。
(3)装置E中PH3被氧化成磷酸,MnO4-被还原为Mn2+,写出该反应的离子方程式:________。
(4)收集装置E中的吸收液,加水稀释至250mL,量取其中的25.00mL于锥形瓶中,用4.0×10-5 mol·L-1的Na2SO3标准溶液滴定,消耗Na2SO3标准溶液20.00 mL,反应原理是SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平)。通过计算判断该样品是否合格(写出计算过程)。_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中,发生可逆反应2NO(g)+O2(g)![]() 2NO2(g),不能说明该反应已经达到平衡状态的是
2NO2(g),不能说明该反应已经达到平衡状态的是
A. 正反应生成NO2的速率和逆反应生成NO的速率相等
B. 反应容器中压强不随时间的延长而变化
C. 混合气体颜色深浅保持不变
D. 混合气体的密度不随时间延长而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为了证明、比较SO2和氯水的漂白性,设计了如图所示的实验装置。

(1)实验室常选用KMnO4和浓盐酸制Cl2;选用Cu和浓硫酸反应制取SO2时,其中制SO2应选用如图A、E两发生装置中___装置(填装置序号),反应的化学方程式为___。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:___,D:___。
(3)甲乙两名同学分别利用如图所示装置探究两种气体按不同比例混合后的漂白性。

试
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:___。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是:___(结合反应方程式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com