
【题目】一定条件下,向一带活塞的密闭容器中充入2 mol SO2和1 mol O2,发生下列反应:2SO2(g)+O2(g)![]() 2SO3(g)达到平衡后改变下述条件,SO3气体平衡浓度不改变的是( )
2SO3(g)达到平衡后改变下述条件,SO3气体平衡浓度不改变的是( )
A.保持温度和容器体积不变,充入2 mol SO3(g)
B.保持温度和容器内压强不变,充入2 mol SO2(g)
C.保持温度和容器内压强不变,充入1 mol O2(g)
D.保持温度和容器体积不变,充入1 mol N2 (g)
【答案】D
【解析】
达到平衡后,改变条件,SO3的平衡浓度不改变,说明为等效平衡,恒温恒容按化学计量数转化到左边满足2molSO2,1molO2或恒温恒压按化学计量数转化到左边满足n(SO2):n(O2)=2:1,再结合平衡移动分析。
A、温度和容器的体积不变,充入2molSO3(g),按化学计量数转化到左边,得到n(SO2)=2mol,n(O2)=1mol,原平衡中还存在SO2、O2,故n(SO2)、n(O2)不满足2molSO2,1molO2,与原来的平衡不是等效平衡,所以SO3气体平衡浓度改变,故A不符合;
B、温度和容器内压强不变,充入2 mol SO2(g),平衡将正向移动,所以SO3气体平衡浓度改变,故B不符合;
C、保持温度和容器的压强不变,充入1molO2(g),增大反应物的浓度,平衡向正反应移动,SO3的平衡浓度改变,故C不符合;
D、保持温度和容器体积不变,充入1mol N2 (g),各反应物浓度不变,化学平衡不移动,所以SO3的浓度不变,故D符合;
答案为D。


科目:高中化学 来源: 题型:
【题目】类比pH的定义,对于稀溶液可以定义![]() ,
,![]() 。常温下,某浓度
。常温下,某浓度![]() 溶液在不同pH值下,测得
溶液在不同pH值下,测得![]() 、
、![]() 、
、![]() 变化如图所示。下列说法正确的是
变化如图所示。下列说法正确的是
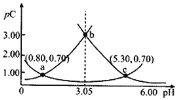
A.![]() 时,
时,![]()
B.常温下,![]() ,
,![]()
C.b点时,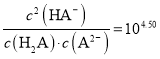
D.![]() 时,
时,![]() 先增大后减小
先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮可形成多种氧化物,如NO、NO2、N2O4等。已知NO2和N2O4的结构式分别是![]() 和
和 。实验测得N-N键键能为167kJ·mol-1, NO2中氮氧键的平均键能为466 kJ·mol-1,N2O4中氮氧键的平均键能为438.5 kJ·mol-1。
。实验测得N-N键键能为167kJ·mol-1, NO2中氮氧键的平均键能为466 kJ·mol-1,N2O4中氮氧键的平均键能为438.5 kJ·mol-1。
(1)写出N2O4转化为NO2的热化学方程式:____________
(2)对反应N2O4(g)![]() 2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是_____
2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是_____

A.A、C两点的反应速率:A>C
B.B、C两点的气体的平均相对分子质量:B<C
C.A、C两点气体的颜色:A深,C浅
D.由状态B到状态A,可以用加热的方法
(3)在100℃时,将0.40mol的NO2气体充入2 L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
时间(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.050 | n2 | 0.080 | 0.080 |
①在上述条件下,从反应开始直至20 s时,二氧化氮的平均反应速率为____________
②n3_____n4(填“>”、“<”或“=”),该反应的平衡常数K的值为_____________,升高温度后,反应2NO2![]() N2O4的衡常数K将______(填“增大”、“减小”或“不变”)。
N2O4的衡常数K将______(填“增大”、“减小”或“不变”)。
③若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度是_____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.可以用灼烧后闻气味区别棉花和羊毛
B.油脂水解一定全部生成甘油和高级脂肪酸
C.向蛋白质溶液中加入重金属盐溶液可使蛋白质产生盐析
D.淀粉和纤维素的组成都是![]() ,但淀粉水解纤维素不能水解
,但淀粉水解纤维素不能水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在一个5L的密闭容器中发生反应![]() ,该反应的平衡常数和温度的关系如下:
,该反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
①该反应的平衡常数表达式K=__________,
②该反应的![]() _________0 (填“>”“<”或“=”)。
_________0 (填“>”“<”或“=”)。
③ 判断该反应是否达到平衡的依据为(_______)
A.压强不随时间改变
B.气体的密度不随时间改变
C.c(A)不随时间改变
D.单位时间里生成C和D的物质的量相等
E. 气体的平均相对分子质量不随时间改变
④1200℃时反应![]() 的平衡常数的值为______________。
的平衡常数的值为______________。
⑤830℃时,充入2.0mol的A和8.0mol的B,如反应初始6s内A的平均反应速率v(A)=0.03mol/(L· s)则6s时c(A)=___________![]() ,C的物质的量为__________mol;若反应经一段时间后,达到平衡时A的转化率为____________,如果这时向该密闭容器中再充入1mol氩气(氩气不参与该反应),平衡时A的转化率将____________(填“增大”“减小” 或“不变”), 如果这时向该密闭容器中再充入1.0mol的A和4.0mol的B, 平衡时A的转化率将____________(填“增大”“减小” 或“不变”)。
,C的物质的量为__________mol;若反应经一段时间后,达到平衡时A的转化率为____________,如果这时向该密闭容器中再充入1mol氩气(氩气不参与该反应),平衡时A的转化率将____________(填“增大”“减小” 或“不变”), 如果这时向该密闭容器中再充入1.0mol的A和4.0mol的B, 平衡时A的转化率将____________(填“增大”“减小” 或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种烃分子的结构如图所示,下列有关说法错误的是( )
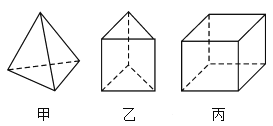
A.1 mol甲分子内含有10 mol共价键
B.由乙分子构成的物质不能发生氧化反应
C.丙分子的二氯取代产物只有三种
D.三者不互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水的电离平衡曲线如图所示:
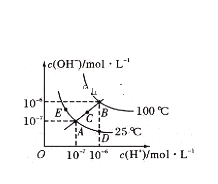
据图回答下列问题:
①图中A、B、C三点处![]() 的大小关系为____________________________________。
的大小关系为____________________________________。
②在A点处,温度不变时,往水中通入适量HCl气体,可以使体系从A点变化到________点。
③在B点处,0.01mol/L的NaOH溶液的pH=_______________。
④在B点处,0.5mol/L ![]() 溶液与1mol/L的KOH溶液等体积混合,充分反应后,所得溶液的pH=__________。
溶液与1mol/L的KOH溶液等体积混合,充分反应后,所得溶液的pH=__________。
⑤在A点处,1g水中含有H+的个数为___________,水的电离平衡常数K与水的离子积![]() 关系为________________。
关系为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关,下列说法不正确的是![]()
A.医用酒精的浓度通常为![]()
B.用食醋可除去热水壶内壁的水垢
C.烹鱼时加适量醋和酒可以增加香味
D.乙烯可作为水果的催熟剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组在给定条件下离子共存判断及反应的离子方程式均正确的是( )
选项 | 条件 | 离子组 | 离子共存判断及反应的离子方程式 |
A | 滴加氨水 | Na+、Al3+、Cl-、NO3- | 不能大量共存,Al3++3OH-=Al(OH)3↓ |
B | AG=lg[ | NH4+、Fe2+、I﹣、NO3- | 一定能大量共存 |
C | pH=1的溶液 | Fe2+、Al3+、 SO42-、MnO4- | 不能大量共存,5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O |
D | 通入少量SO2气体 | K+、Na+、ClO-、SO42- | 不能大量共存,2ClO-+SO2+H2O=2HClO+SO32- |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com