
【题目】【2016·西安一模】某化学兴趣学习小组设计实验探究金属M与浓硫酸反应的气体产物。
[提出假设] 假设1:气体产物只有SO2; 假设2:_______________。
[实验设计]为了探究金属M与浓硫酸反应产物,设计如图实验装置:一定量的浓硫酸与金属M反应。
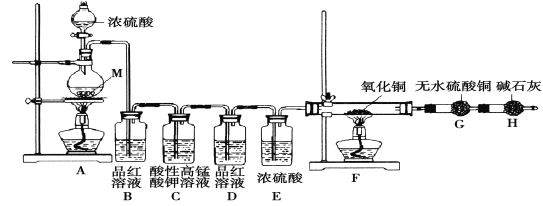
(1) 检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在H装置后面连上一根导管,然后 ,则证明装置的气密性良好。
(2)若B瓶里品红溶液褪色,E、F和G中都无明显现象。反应后硫酸盐中金属显+2价。写A中发生反应的化学方程式: ;
(3)若假设2正确,则可观察到:F管中 ;G干燥管里 。
[实验反思] 为了进一步探究金属M成分和气体组分,进行如下实验:
称取11.2g金属M放入装置A中,加入一定量的浓硫酸,反应结束后,B瓶里品红溶液褪色,金属没有剩余,拆下G并称重,G增重0.9g。
(4)为了观察溶液颜色,实验完毕后,需要稀释烧瓶里溶液。稀释烧瓶里溶液的操作方法: 。
(5)将稀释后的溶液分装甲、乙试管,向甲试管里滴加KSCN溶液,溶液变红色;向乙试管里滴加酸性高锰酸钾溶液,振荡,溶液紫色褪去。如果烧瓶溶液中金属离子浓度相等,则气体成分及物质的量为 。试写出烧瓶里发生反应的总化学方程式 。
【答案】假设2:气体产物有SO2 和H2(2分)
(1) 将导气管插入盛有水的水槽中,微热烧瓶,若导气管冒气泡,停止加热有一段水柱上升;(2分)
(2) M+2H2SO4(浓)![]() MSO4 +SO2↑+2H2O (2分)
MSO4 +SO2↑+2H2O (2分)
(3)黑色粉末变成红色;(1分)白色粉末变为蓝色(1分)
(4) 先将烧瓶中混合溶液冷却,再将混合液慢慢加入盛水的烧杯里,并不断搅拌(2分)
(5) SO2:0.20mol ;H2:0.05mol(2分)
4Fe+9H2SO4(浓) ![]() 2FeSO4+Fe2(SO4)3+4SO2↑+H2↑+8H2O (2分)
2FeSO4+Fe2(SO4)3+4SO2↑+H2↑+8H2O (2分)
【解析】当金属过量时,且金属较活泼则生成的气体中可能含有氢气,所以假设2为:气体产物有SO2和H2 ;
(1)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在H装置后面连上一根导管,然后将导气管插入盛有水的水槽中,微热烧瓶,若导气管冒气泡,停止加热有一段水柱上升,则说明装置的气密性良好;
(2)反应后硫酸盐中金属显+2价,类比铜与浓硫酸的反应,M与浓硫酸反应的化学方程式为:M+2H2SO4(浓)![]() MSO4+SO2↑+2H2O;
MSO4+SO2↑+2H2O;
(3)如果F管中黑色粉末变成红色、G中白色的无水硫酸铜变成蓝色,说明二氧化硫中混有氢气,从而证明假设2正确;
(4)可以类比稀释浓硫酸的方法进行操作,方法为:先将烧瓶中混合溶液冷却,再将混合液慢慢加入盛水的烧杯里,并不断搅拌;
(5)向甲试管里滴加KSCN溶液,溶液变红色,说明金属M为Fe;G增重0.9g,0.9g为水的质量,则氢气的物质的量为:n(H2)=n(H2O)=![]() =0.05mol;1.2g铁的物质的量为:n(Fe)=
=0.05mol;1.2g铁的物质的量为:n(Fe)=![]() =0.2mol;向乙试管里滴加酸性高锰酸钾溶液,振荡,溶液紫色褪去,说明溶液中含有亚铁离子,烧瓶溶液中金属离子浓度相等,则铁离子和亚铁离子的物质的量相等,n(Fe2+)=n(Fe3+)=0.1mol,根据电子守恒,生成二氧化硫的物质的量为:n(SO2)=
=0.2mol;向乙试管里滴加酸性高锰酸钾溶液,振荡,溶液紫色褪去,说明溶液中含有亚铁离子,烧瓶溶液中金属离子浓度相等,则铁离子和亚铁离子的物质的量相等,n(Fe2+)=n(Fe3+)=0.1mol,根据电子守恒,生成二氧化硫的物质的量为:n(SO2)=![]() =0.20mol,铁与硫酸反应的化学方程式为:4Fe+9H2SO4(浓)
=0.20mol,铁与硫酸反应的化学方程式为:4Fe+9H2SO4(浓)![]() 2FeSO4+Fe2(SO4)3+4SO2↑+H2↑+8H2O。
2FeSO4+Fe2(SO4)3+4SO2↑+H2↑+8H2O。


科目:高中化学 来源: 题型:
【题目】【2016宜春校级模拟】在一定温度下,一定体积的密闭容器中有如下平衡:H2(g)+I2(g)2HI(g).已知H2和I2的起始浓度均为0.10molL﹣1时,达平衡时HI的浓度为0.16molL﹣1.若H2和I2的起始浓度均变为0.20molL﹣1,则平衡时H2的浓度(molL﹣1)是( )
A.0.16 B.0.08 C.0.04 D.0.02
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用所学化学知识解答问题:
(1)微粒 ![]() Na+中的质子数是 , 中子数是 , 核外电子数是 .
Na+中的质子数是 , 中子数是 , 核外电子数是 .
(2)用电子式表示形成过程:H2S;MgF2 .
(3)写出化学反应方程式:用四氧化三铁铝热法炼铁;电解法冶炼铝 .
(4)有下列各组微粒或物质:
A. ![]() C和
C和 ![]() C
C
B.CH3CH2CH2CH3和 CH3CH2CH(CH3)CH3
C.  和
和 
D.CH3CH2CH2CH3和 ![]()
①两种微粒互为同位素是;②两种物质属于同系物的是;③两种物质互为同分异构体的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】信息、材料、能源被称为新科技革命的“三大支柱”。下列有关资讯错误的是
A. 在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源
B. 生活中常用的食品袋为聚乙烯产品
C. 随着人类文明逐渐发展,化石燃料将逐步退出历史舞台
D. 太阳能电池的主要材料是高纯度的二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“即食即热型快餐”适合外出时使用,其内层是用铝箔包裹并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线使这两种化学物质发生反应,放出的热量便可对食物进行加热,这两包化学物质最适合的选择是
A.浓硫酸和水 B.生石灰和水 C.氢氧化钠和水 D.氯化钠和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为1L的干燥烧瓶中,用排空气法收集NH3气体,测得烧瓶中气体对氢气的相对密度为9.5,此气体中NH3的体积分数约为( )
A. 83% B. 75% C. 50% D. 25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.烷烃分子中碳原子间以单键结合,碳原子剩余价键全部与氢原子结合
B.分子组成符合CnH2n+2的烃一定是烷烃
C.丙烷分子中三个碳原子在一条直线上
D.同分异构现象是有机物种类繁多的重要原因之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的是
A.已知2H2(g)+O2(g)![]() 2H2O(l) △H=571.6 kJ/mol,则氢气的燃烧热为285.8 kJ/mol
2H2O(l) △H=571.6 kJ/mol,则氢气的燃烧热为285.8 kJ/mol
B.已知C(石墨,s)![]() C(金刚石,s) △H>0 ,则金刚石比石墨稳定
C(金刚石,s) △H>0 ,则金刚石比石墨稳定
C.含20.0 gNaOH稀溶液与稀盐酸完全中和,放出28.7 kJ热量,则稀醋酸和稀NaOH溶液反应热化学方程式为NaOH(aq) + CH3COOH(aq)![]() CH3COONa(aq) + H2O(1) △H=57.4 kJ/mol
CH3COONa(aq) + H2O(1) △H=57.4 kJ/mol
D.已知2C(s)+2O2(g)![]() 2CO2(g) △H1;2C(s)+O2(g)
2CO2(g) △H1;2C(s)+O2(g)![]() 2CO(g) △H2,则△H1>△H2
2CO(g) △H2,则△H1>△H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com