
【题目】下列说法错误的是( )。
A. 硅胶常用于作干燥剂 B. 氢氟酸可以用来刻蚀玻璃
C. 硅的化学性质很稳定,主要以游离态存在于自然界 D. 硅酸钠的水溶液俗称水玻璃,可用于制备木材防火剂
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于丙烷结构、性质的推断中正确的是( )。
A. 丙烷的3个碳原子不在同一直线上 B. 丙烷可与氯水发生取代反应
C. 丙烷能使溴水、酸性KMnO4溶液都褪色 D. 丙烷可与强酸或强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是 ( )
A. 18O原子核内的中子数为8 B. 16O2和18O2的化学性质几乎相同
C. H216O与H218O质子数不同 D. H2和D2 属于同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积固定的密闭容器中,某化学反应2A(g) ![]() B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
实验 序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内,用A表示表示该反应的平均速率
为_______ mol/(L . min)
(2)在实验2,A的初始浓度c2=________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_______________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3_______v1(填>、=、<),c3=________mol/L
(4)比较实验4和实验1,可推测该反应是________反应(选填吸热、放热)。
理由是___________________________________________________________
(5)根据以上实验请指出要加快该反应可采取什么样的方法(列举方法最少2种)
________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
I.取样、氧的固定 .
用溶解氧瓶采集水样,记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
在碘量瓶中将固氧后的水样酸化,MnO(OH)2被I-还原为Mn2+(该反应放热),在暗处静置5min,然后用标准Na2S3O3溶液滴定生成的I2(2S2O32-+I2=2I- +S4O62-)。
回答下列问题:
(1)“氧的固定”中发生反应的化学方程式为___________。
(2)水样酸化后发生反应的离子方程式___________。
(3)在碘量瓶(如图)中进行反应,要盖上塞子且在塞子上倒少量水,这样做的目的是___________。
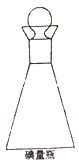
(4)Na2S3O3溶液不稳定,易被氕化,且易受到水中CO2以及微生物的影响而分解,配制该溶液时需要的蒸馏水必须经过煮沸冷却后才能使用,其目的是__________。
(5) Na2S3O3溶液不稳定,使用前需标定,KIO3做基准物标定Na2S3O3溶液的浓度,称取0.214g KIO3与过量的KI作用,析出的碘用Na2S3O3溶液滴定,用去24.00mL,此Na2S3O3溶液的浓度为______(已知M(KIO3) = 214.0g/mol)
(6)取100.00mL水样经固氧、酸化后,用该Na2S3O3溶液滴定,以淀粉溶液作指示剂,终点现象为_____;若消耗Na2S3O3的体积为l0mL,则水样中溶解氧的含量为______mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关AgCl的沉淀溶解平衡说法中正确的是( )
A.AgCl沉淀生成和溶解不断进行,速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.AgCl悬浊液中加入NaCl固体,AgCl溶解度不变
D.升温,AgCl沉淀的溶解度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料.实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)212H2O]的工艺流程如图所示: 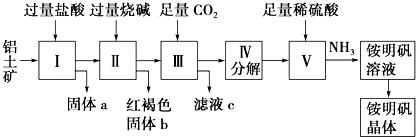 请回答下列问题:
请回答下列问题:
(1)固体a的化学式为 , Ⅲ中通入足量CO2气体发生反应的离子方程式为 .
(2)由Ⅴ 制取铵明矾溶液的化学方程式为 . 从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)、冷却结晶、过滤洗涤.
(3)以1000kg含氧化铝36%的铝土矿为原料制取Al2(SO4)3 , 需消耗质量分数98%的硫酸(密度1.84gcm﹣1)L(计算结果请保留一位小数).
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量.若欲使制得的铵明矾和硫酸铝的物质的量之比为1:1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com