
【题目】水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
I.取样、氧的固定 .
用溶解氧瓶采集水样,记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
在碘量瓶中将固氧后的水样酸化,MnO(OH)2被I-还原为Mn2+(该反应放热),在暗处静置5min,然后用标准Na2S3O3溶液滴定生成的I2(2S2O32-+I2=2I- +S4O62-)。
回答下列问题:
(1)“氧的固定”中发生反应的化学方程式为___________。
(2)水样酸化后发生反应的离子方程式___________。
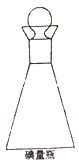
(3)在碘量瓶(如图)中进行反应,要盖上塞子且在塞子上倒少量水,这样做的目的是___________。
(4)Na2S3O3溶液不稳定,易被氕化,且易受到水中CO2以及微生物的影响而分解,配制该溶液时需要的蒸馏水必须经过煮沸冷却后才能使用,其目的是__________。
(5) Na2S3O3溶液不稳定,使用前需标定,KIO3做基准物标定Na2S3O3溶液的浓度,称取0.214g KIO3与过量的KI作用,析出的碘用Na2S3O3溶液滴定,用去24.00mL,此Na2S3O3溶液的浓度为______(已知M(KIO3) = 214.0g/mol)
(6)取100.00mL水样经固氧、酸化后,用该Na2S3O3溶液滴定,以淀粉溶液作指示剂,终点现象为_____;若消耗Na2S3O3的体积为l0mL,则水样中溶解氧的含量为______mg/L。
【答案】 2Mn(OH)2+O2=2MnO(OH)2 MnO(OH)2+2I-+4H+ =I2 + Mn2+ +3H2O 液封、防止碘挥发 杀菌、除氧气及二氧化碳 Na2S2O3浓度= 0.25mol/L 当最后一滴标准液入时,溶液由蓝色变为无色,且半分钟内无变化 200
【解析】本题主要考查对于碘量法测定河水中溶解氧实验方案的评价。
(1)“氧的固定”中发生反应的化学方程式为2Mn(OH)2+O2=2MnO(OH)2。
(2)水样酸化后发生反应的离子方程式为MnO(OH)2+2I-+4H+ =I2 + Mn2+ +3H2O。
(3)在碘量瓶(如图)中进行反应,要盖上塞子且在塞子上倒少量水,这样做的目的是液封、防止碘挥发。
(4)Na2S3O3溶液不稳定,易被氕化,且易受到水中CO2以及微生物的影响而分解,配制该溶液时需要的蒸馏水必须经过煮沸冷却后才能使用,其目的是杀菌、除氧气及二氧化碳。
(5)由![]() + 5I-+6H+
+ 5I-+6H+![]() 3I2+3H2O和I2+2Na2S2O3
3I2+3H2O和I2+2Na2S2O3![]() 2NaI+Na2S4O6可得KIO3~6Na2S2O3,0.214g KIO3的物质的量为0.001000mol,析出的碘用Na2S3O3溶液滴定,用去24.00mL,此Na2S3O3溶液的浓度为0.006000/0.024000mol/L=0.2500mol/L。
2NaI+Na2S4O6可得KIO3~6Na2S2O3,0.214g KIO3的物质的量为0.001000mol,析出的碘用Na2S3O3溶液滴定,用去24.00mL,此Na2S3O3溶液的浓度为0.006000/0.024000mol/L=0.2500mol/L。
(6)取100.00mL水样经固氧、酸化后,用该Na2S3O3溶液滴定,以淀粉溶液作指示剂,终点现象为当最后一滴标准液滴入时,溶液由蓝色变为无色,且半分钟内无变化;
由2Mn(OH)2+O2=2MnO(OH)2、MnO(OH)2+2I-+4H+ =I2 + Mn2+ +3H2O、I2+2Na2S2O3![]() 2NaI+Na2S4O6可得O2~4Na2S2O3,若消耗Na2S3O3的体积为l0mL,则水样中溶解氧的含量为0.2500mol×10mL/4×32g/mol/L/100.00mL=200mg/L。
2NaI+Na2S4O6可得O2~4Na2S2O3,若消耗Na2S3O3的体积为l0mL,则水样中溶解氧的含量为0.2500mol×10mL/4×32g/mol/L/100.00mL=200mg/L。


科目:高中化学 来源: 题型:
【题目】已知短周期元素M的第三电子层上有7个电子,则该元素的说法正确的是 ( )
A. 在周期表中第三周期第VIIA族。
B. 单质为黄绿色气体
C. 该元素为金属元素
D. 最高化合价为+1价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富铁铝土矿(主要含有Al2O3、Fe2O3、FeO和SiO2)可用于制备净水剂明矾KAl(SO4)212H2O和补血剂FeSO47H2O.工艺流程如下(部分操作和产物略去): 
(1)操作1的名称是 .
(2)反应①②③④中是氧化还原反应的是(填写编号).
(3)综合考虑,金属X最好选择的试剂是 , 写出该反应离子方方程式 .
(4)反应①的离子方程式是、 .
(5)溶液D中含有的金属阳离子是 , 检验方法是 .
(6)用含铝元素27%的上述矿石10吨,通过上述流程最多生产明矾吨.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )。
A. 硅胶常用于作干燥剂 B. 氢氟酸可以用来刻蚀玻璃
C. 硅的化学性质很稳定,主要以游离态存在于自然界 D. 硅酸钠的水溶液俗称水玻璃,可用于制备木材防火剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应正向反应过程中能量变化如图所示,下列说法正确的是( )

A. 该反应为吸热反应
B. 当反应达到平衡时,降低温度,A的转化率减小
C. 升高温度平衡常数K增大;压强增大,平衡向正反应方向移动
D. 加入催化剂,反应速率增大,反应热不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于离子检验的说法中正确的是( )
A. 向某溶液中加入AgNO3溶液,生成白色沉淀,该溶液中一定含有Cl-
B. 向某溶液中加入稀盐酸,产生无色气体,则该溶液中一定含有CO![]()
C. 向某溶液中加入NaOH溶液,用蓝色石蕊试纸检验逸出的气体,试纸变红,则该溶液中一定含有NH4+
D. 向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中加几滴新制的氯水,溶液变为红色,则该溶液中一定含有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将X和Y各0.16 mol加入10 L恒容密闭容器中,发生反应X(s)+2Y(g) ![]() 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A. 其他条件不变,再充入0.2 mol Z,Z的体积分数增大
B. 该温度下此反应的平衡常数K=l.44
C. 当容器内气体的平均摩尔质量不变时,即达到化学平衡状态
D. 反应前 2 min 的平均速率 v(Z)=4.0×10-3mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分.
碳 | 氮 | Y | |
X | 硫 | Z |
请判断 X、Y、Z,并用相应的元素符号回答下列问题.
(1)X是 , 它的原子M层电子数是 .
(2)表中元素原子半径最大的是 .
(3)Y在元素周期表中的位置是第周期第族,用电子式表示Y的最简单氢化物的形成过程 .
(4)氮气中氮原子之间的化学键属于键,由氮气与氢气反应生成1mol氨气时转移电子的数目是NA .
(5)硫与Z两种元素相比,非金属性强的是 , 请用化学方程式说明这一结论 .
(6)碳、氮、Y三种元素的最简单气态氢化物的稳定性由强到弱的顺序是 . 由最高价碳元素与最低价氮元素组成化合物的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g) ![]() CH3OCH3(g)
CH3OCH3(g)
+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡。该反应中CO2的平衡转化率随温度的变化曲线如图所示。下列说法正确的是

A.反应2CO2(g)+6H2(g) ![]() CH3OCH3(g) + 3H2O(g)的 △S<0、△H<0
CH3OCH3(g) + 3H2O(g)的 △S<0、△H<0
B.表示乙容器CO2的平衡转化率随温度变化的是曲线B
C.体系中c(CH3OCH3):c(CH3OCH3,状态Ⅱ)<2c(CH3OCH3,状态Ⅲ)
D.逆反应速率v逆:v逆(状态Ⅰ)<v逆(状态Ⅲ)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com