
����Ŀ������һ��������Na2O���ʵ�Na2O2�����������ͼ��ѡ���ʵ���ʵ��װ�ã����һ�����ʵ�飬�ⶨNa2O2�����Ĵ��ȣ��ɹ�ѡ�õķ�Ӧ��ֻ��CaCO3���壬ϡ���������ˮ��������д���пհף�

��1��д����ʵ����Na2O2��Na2O�ֱ�����Ӧ�Ļ�ѧ����ʽ_________________________��_________________
��2��Ӧѡ�õ�װ���ǣ�ֻҪ��д��ͼ��װ�õı�ţ�_______________________
��3����ѡ��װ�õ�����˳��Ӧ�ǣ�����ӿڵ���ĸ�����ӽ���ʡ�ԣ�________________
���𰸡�2Na2O2+2H2O=4NaOH+O2�� Na2O+H2O=2NaOH �ݢڢ٢� G��D��C��A��B��F
��������
�����ƺ������ƾ��ܺ�ˮ��Ӧ����Ӧ������Ϊ���������ƺ�ˮ��Ӧ��������������Һ��ͬʱ������������������˿�������ˮ�������ⶨ���ɵ����������������ȷ���������Ƶ�������ٷֺ������ݴ˷������
(1)�����ƺ������ƾ��ܺ�ˮ��Ӧ������ʽΪ��2Na2O2+2H2O=4NaOH+O2����Na2O+H2O=2NaOH���ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����Na2O+H2O=2NaOH��
(2)ʵ���ԭ���ǣ��������ƺ�ˮ��Ӧ��������������Һ��ͬʱ�����������������������л���ˮ������Ҫ��Ũ������ˮ��Ȼ���������ˮ�������ⶨ�������������������ȷ���������Ƶ�������ٷֺ������ʿ�ѡ���װ��Ϊ�ݢڢ٢ܣ��ʴ�Ϊ���ݢڢ٢ܣ�
(3)����(2)�ķ���������ˮ�������ⶨ��������ʱ������ʢˮ���Լ�ƿ����һ��Ҫ�̽����������ɵ�������ˮ�ų�����Ͳ��ˮ�����������������������������Ӵ���(G)��(D)��(C)��(A)��(B)��(F)���ʴ�Ϊ��G��D��C��A��B��F��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��98gH2SO4��
��1�����Ӹ�����_____
��2��Oԭ�����ʵ�����___mol
��3��HԪ�ص�������______g
��4��Sԭ�Ӹ�����__
��5�����ӵ����ʵ�����_____mol
��6�����ӵĸ�����_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�����������һ����ͬ���ǣ� ��
A. 1gH2��8gO2
B. 0.1mol HCl��22.4LHe
C. 18LH2O��18LCO2
D. 28gCO��1molCO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����:��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺

(1)��ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��_____________��
(2)�����ͼ����ʾ��װ�ý������飬��õ��к�����ֵ_______(����ƫ��ƫС����Ӱ����)��
(3)ʵ���и���60 mL 0.50 mol��L-1�����50 mL 0.55 mol��L-1NaOH��Һ���з�Ӧ����(2)��ʵ����ȣ������к���_________ (��������������������)��
��: (1)�������˻������������ȼ���DZ���(C3H8)������������˻���ȼ���DZ�ϩ(C3H6),��������ɵñ�ϩ����֪��C3H8(g) === CH4(g)��HC��CH(g)��H2(g) ��H1=+156.6 kJ��mol��1
CH3CH��CH2(g)=== CH4(g)�� HC��CH(g ) ��H2=+32.4 kJ��mol��1
��C3H8(g) === CH3CH��CH2(g)��H2(g) ��H =______________ kJ��mol��1��
(2)������ʱ����(N2H4)��ȼ�ϣ����������������������߷�Ӧ���ɵ�������̬ˮ����֪32gN2H4(g)��ȫ����������Ӧ�ų�568kJ���������Ȼ�ѧ����ʽ�ǣ�____________________________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͼʾ���ó��Ľ�����ȷ����(����)
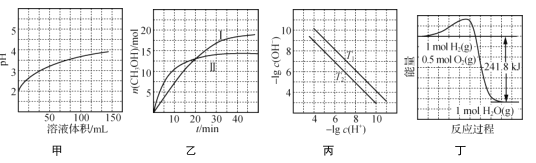
A. ͼ�ױ�ʾ1 mL pH��2ijһԪ����Һ��ˮϡ��ʱ��pH����Һ������ı仯���ߣ�˵��������ǿ��
B. ͼ�ұ�ʾ�����ܱ�����������������ͬʱ�ı��¶ȣ���ӦCO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g)��n(CH3OH)��ʱ��ı仯���ߣ�˵����Ӧƽ�ⳣ��K��>K��
CH3OH(g)��H2O(g)��n(CH3OH)��ʱ��ı仯���ߣ�˵����Ӧƽ�ⳣ��K��>K��
C. ͼ����ʾ��ͬ�¶���ˮ��Һ�У�lg c(H��)����lg c(OH��)�仯���ߣ�˵��T1>T2
D. ͼ����ʾ1 mol H2��0.5 mol O2��Ӧ����1 mol H2O�����е������仯���ߣ�˵��H2��ȼ������241.8 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����VL����MgSO4��K2SO4�Ļ����Һ�ֳ����ȷݣ�һ�ݼ��뺬amolNaOH����Һ��ǡ��ʹþ������ȫ����Ϊ������þ����һ�ݼ��뺬bmolBaCl2����Һ��ǡ��ʹ�����������ȫ����Ϊ���ᱵ����ԭ�����Һ�м����ӵ����ʵ���Ϊ
A. (b-a)molB. (2b-a)molC. 2(b-a)molD. 2(2b-a)mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��״���£�1.92 gij��������Ϊ672 mL������������Է�������Ϊ______��
(2)��25 �桢101 kPa�������£�ͬ������CH4��A��������֮����15��8����A��Ħ������Ϊ________��
(3)������ͬ�ݻ����ܱ�����X��Y����25 ���£�X�г���a g A���壬Y�г���a g CH4���壬X��Y�ڵ�ѹǿ֮����4��11����A��Ħ������Ϊ________��
(4)��ͬ�����£������Ϊa��b��������Ϊa��b��H2��O2�Ļ�����壬��ƽ��Ħ�������ֱ���________��________��
(5)�ڱ�״���£�CO��CO2�Ļ�����干39.2 L������Ϊ61 g����������������ʵ���֮��Ϊ________mol��COռ�������________%��
(6)��ij�¶�ʱ��һ������Ԫ��A���⻯��AH3���ں��º�ѹ���ܱ���������ȫ�ֽ�Ϊ������̬���ʣ���ʱ�����������Ϊԭ����7/4����A���ʵķ���ʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ī˾͡(Bendamustine)��һ�ֿ���ҩ�����Ī˾͡��һ�ֺϳ�·�����£�


(1) D�������������������____(������)��
(2) A��B�ķ�Ӧ����Ϊ____��
(3) E�ķ���ʽΪC12H13N3O4��д��E�Ľṹ��ʽ��__________��
(4) G�� ��ͬ���칹�壬G�ܷ���������Ӧ��������ֻ��2�ֲ�ͬ��ѧ�������⡣д��һ�ַ���������G�Ľṹ��ʽ��__________��
��ͬ���칹�壬G�ܷ���������Ӧ��������ֻ��2�ֲ�ͬ��ѧ�������⡣д��һ�ַ���������G�Ľṹ��ʽ��__________��
(5)��֪��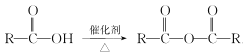 ����д����
����д����![]() �Ҵ�Ϊԭ���Ʊ�
�Ҵ�Ϊԭ���Ʊ� �ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)__________________________��
�ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ЧӦ����ȫ���ע�Ļ�������֮һ��CO2��Ŀǰ�����к�����ߵ�һ���������壬CO2���ۺ������ǽ�����Ҽ���Դ�������Ч;����
��1��CO2�������ܺϳɵ�̼ϩ����2CO2(g)��6H2(g)![]() C2H4(g)��4H2O(g)����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ��ʾ��������b��ʾ������Ϊ________(�ѧʽ)��
C2H4(g)��4H2O(g)����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ��ʾ��������b��ʾ������Ϊ________(�ѧʽ)��

��2��CO2��H2�ڴ���Cu/ZnO�����¿ɷ�������ƽ�з�Ӧ���ֱ�����CH3OH��CO��
��ӦA��CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)
CH3OH(g)��H2O(g)
��ӦB��CO2(g)��H2(g)![]() CO(g)��H2O(g)
CO(g)��H2O(g)
����CO2��H2��ʼͶ�ϱ�Ϊ1��3ʱ���¶ȶ�CO2ƽ��ת���ʼ��״���CO���ʵ�Ӱ����ͼ��ʾ��

����ͼ��֪�¶�����CO�IJ�������������Ҫԭ�������_____��
����ͼ��֪��ȡCH3OH�����˵��¶���________�����д�ʩ���������CO2ת��ΪCH3OH��ƽ��ת���ʵ���________(����ĸ)��
A. ʹ�ô���
B. ������ϵѹǿ
C. ����CO2��H2�ij�ʼͶ�ϱ�
D. Ͷ�ϱȺ�����������䣬���ӷ�Ӧ���Ũ��
��3���ں��º��������£���ӦA�ﵽƽ��ı�־��_____
A. ����������ѹǿ���ٷ����仯
B. �����������ܶȲ��ٷ����仯
C. ������������ɫ���ٷ����仯
D. ����������ƽ��Ħ���������ٷ����仯
��4����CO2��ȡC��̫���ܹ�����ͼ��ʾ�����ȷֽ�ϵͳ�������ķ�ӦΪ2Fe3O4![]() 6FeO��O2����ÿ�ֽ�1 mol Fe3O4ת�Ƶ��ӵ����ʵ���Ϊ_____��������ϵͳ��������Ӧ�Ļ�ѧ����ʽΪ___��
6FeO��O2����ÿ�ֽ�1 mol Fe3O4ת�Ƶ��ӵ����ʵ���Ϊ_____��������ϵͳ��������Ӧ�Ļ�ѧ����ʽΪ___��

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com