
【题目】98gH2SO4中
(1)分子个数是_____
(2)O原子物质的量是___mol
(3)H元素的质量是______g
(4)S原子个数是__
(5)电子的物质的量是_____mol
(6)质子的个数是_____
【答案】6.02×1023或NA 4 2 6.02×1023或NA 50 3.01×1025
【解析】
98gH2SO4的物质的量为![]() =1mol,则
=1mol,则
(1)分子个数是1mol×NA=6.02×1023个,故答案为:6.02×1023或NA;
(2)O原子物质的量为1mol×4=4mol,故答案为:4;
(3)H元素的质量是1mol×2×1g/mol=2g,故答案为:2;
(4)S原子个数是1mol×NA=6.02×1023个,故答案为:6.02×1023或NA;
(5)电子的物质的量是1mol×(1×2+16+8×4)=50mol,故答案为:50;
(6)分子中质子数=电子数,则质子的个数是50mol×NA=3.01×1025个,故答案为:3.01×1025;


科目:高中化学 来源: 题型:
【题目】常温下,0.1mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者所占物质的量分数(分布系数)随pH变化的关系如图所示。下列表述不正确的是

A. HC2O4-![]() H++C2O42- K=1×10-4.3
H++C2O42- K=1×10-4.3
B. 将10mL0.1mol/L的H2C2O4溶液与15mL0.1mol/L的NaOH溶液混合后,所得溶液pH等于4.3
C. 常温下HF的Ka=1×10-3.45,将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为H2C2O4+F-=HF+HC2O4-
D. 在0.1mol/LNaHC2O4溶液中,各离子浓度大小关系为c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某一元弱酸HA的电离常数K=1.6×10-6。 向20.00 mL 浓度约为0.1 mol·L-1 HA溶液中逐滴加入0.1000 mol·L-1 的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:(已知lg4=0.6)
(1)a点溶液中pH约为________,此时溶液中H2O电离出的c(H+)为________。

(2)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用__________作指示剂,滴定终点在________(填“c点以上”或“c点以下”)。
(3)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_________________(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(4)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____mol/L。
实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
1 | 21.01 | 20.00 |
2 | 20.99 | 20.00 |
3 | 21.60 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如下图所示装置进行有关实验。

(1)此装置中,怎样检查除启普发生器之外的装置的气密性?_________________________________。
(2)请完成该实验的有关操作步骤。
①检查装置气密性;
②打开a、b产生氢气,观察试管内物质的颜色变化;
③____________________________________________________;
④加热过氧化钠,观察试管内物质的颜色变化;
⑤反应完全后,__________________________________________;
⑥拆卸装置。
(3)该装置中,碱石灰的作用是_________________________ 。
(4)实验过程中观察到(2)中步骤②无明显变化,步骤④Na2O2熔化后,黄色粉末立即变成白色,干燥管内硫酸铜未变成蓝色。则Na2O2与H2反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
A. 化学反应速率关系是:2v正(NH3) = 3v正(H2O)
B. .若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 达到化学平衡时,4v正(O2) = 5v逆(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液面左边低于右边,恢复到原温度后液面左边与右边基本相平,则烧杯内的物质是( )
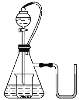
A.过氧化钠B.氧化钠C.钠D.氯化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年11月3日福建泉州港区发生碳九泄露事件。碳九主要含三甲苯、异丙苯、正丙苯、乙基甲苯等有机物。下列关于碳九说法不正确的是![]()
![]()
A. 碳九是多种芳香烃的混合物,可通过石油催化重整得到
B. 进入碳九的泄露区应佩戴含活性炭的口罩,避免吸入有害气体
C. 碳九含上述四种分子的分子式均为C9H12,它们互为同分异构体
D. 碳九含有的有机物均易溶于水,会造成泄露处海域严重污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常采用吸收-电解联合法除去天然气中的H2S气体,并转化为可回收利用的单质硫,其装置如下图所示。通电前,先通入一段时间含H2S的甲烷气,使部分NaOH吸收H2S转化为Na2S,再接通电源,继续通入含杂质的甲烷气,并控制好通气速率即可保证装置中反应的连续性。下列说法正确的是

A. 与电源a端相连的碳棒为阳极,气体A为O2
B. 与电源b端相连的碳棒上电极反应为:2H2O+2e-=2OH-+H2↑
C. 通电过程中,右池溶液中的OH-通过阴离子膜进入左池
D. 在通电前后,右池中的c(NaOH)与c(Na2S)之比基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样。请从下图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体,稀盐酸和蒸馏水)。请填写下列空白:

(1)写出在实验中Na2O2和Na2O分别发生反应的化学方程式_________________________,_________________
(2)应选用的装置是(只要求写出图中装置的标号)_______________________
(3)所选用装置的连接顺序应是(填各接口的字母;连接胶管省略)________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com