
【题目】常温下,0.1mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者所占物质的量分数(分布系数)随pH变化的关系如图所示。下列表述不正确的是

A. HC2O4-![]() H++C2O42- K=1×10-4.3
H++C2O42- K=1×10-4.3
B. 将10mL0.1mol/L的H2C2O4溶液与15mL0.1mol/L的NaOH溶液混合后,所得溶液pH等于4.3
C. 常温下HF的Ka=1×10-3.45,将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为H2C2O4+F-=HF+HC2O4-
D. 在0.1mol/LNaHC2O4溶液中,各离子浓度大小关系为c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)
【答案】B
【解析】
A.由HC2O4-![]() H++C2O42-可知K=
H++C2O42-可知K=![]() ,pH=4.3时,c(C2O42-)=c(HC2O4-)
,pH=4.3时,c(C2O42-)=c(HC2O4-)
B.将等物质的量的NaHC2O4、Na2C2O4溶于水中,HC2O4-电离程度大于C2O42-的水解程度;
C.根据电离常数判断酸性强弱,酸性强的制备酸性弱的;
D.NaHC2O4溶液显酸性,以HC2O4-的电离为主,在溶液中HC2O4-部分电离.
A.由HC2O4-![]() H++C2O42-可知K=
H++C2O42-可知K=![]() ,pH=4.3时,c(C2O42-)=c(HC2O4-),所以K=c(H+)=1×10-4.3,A正确;
,pH=4.3时,c(C2O42-)=c(HC2O4-),所以K=c(H+)=1×10-4.3,A正确;
B.将10mL0.1mol/L的H2C2O4溶液与15mL0.1mol/L的NaOH溶液混合后,两者恰好反应生成等物质的量的NaHC2O4、Na2C2O4。由图像可知,当这两种物质的浓度相同时,溶液的pH=4.3、呈酸性,所以此混合液中HC2O4-电离程度大于C2O42-的水解程度,则溶液中c(C2O42-)>c(HC2O4-),则溶液pH大于4.3,B错误;
C.常温下H2C2O4的K1=10-1.3,K2=10-4.3,HF的KB=1×10-3.45,则酸性:H2C2O4>HF>HC2O4-,所以将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为H2C2O4+F-=HF+HC2O4-,C正确;
D.由图中信息可知,NaHC2O4溶液显酸性,以HC2O4-的电离为主,在溶液中HC2O4-部分电离,则各离子浓度大小关系为:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-),D正确;
故合理选项是B。


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】下列变化中,属于吸热反应的是( )
①液态水汽化②将胆矾加热变为白色粉末③浓H2SO4稀释 ④KClO3分解制O2⑤生石灰跟水反应生成熟石灰⑥石灰石高温分解⑦铝热反应⑧Ba(OH)2·8H2O与固体NH4Cl混合⑨C+H2O=CO+H2 ⑩Al与盐酸反应
A. ②③④⑥⑦⑧⑨ B. ②④⑥⑧⑨ C. ①②④⑥⑧ D. ②③④⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 离子,分别取样,
离子,分别取样,![]() 测得溶液显弱碱性;
测得溶液显弱碱性;![]() 加入足量盐酸,有无色无味气体产生。为确定溶液组成,还需要检测的离子是
加入足量盐酸,有无色无味气体产生。为确定溶液组成,还需要检测的离子是![]()
![]()
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。下列说法错误的是
A.Na3N是由离子键形成的离子化合物
B.Na3N与盐酸反应生成两种盐
C.Na3N与水的反应属于氧化还原反应
D.Na3N中两种粒子的半径:r(Na+)>r(N3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是
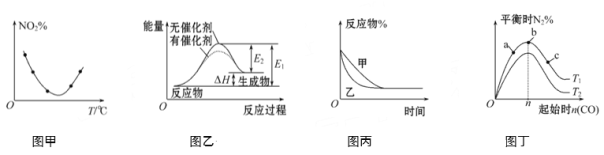
A. 图甲表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)![]() N2O4(g),相同时间后测得NO2含量的曲线,则该反应的ΔH<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的ΔH<0
B. 图乙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变
C. 图丙表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(g)的影响,则P乙>P甲
3C(g)+D(g)的影响,则P乙>P甲
D. 图丁表示反应:4CO(g)+2NO2(g)![]() N2(g)+4CO2(g) ΔH<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,平衡常数K1>K2
N2(g)+4CO2(g) ΔH<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,平衡常数K1>K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡格雷是一种用于预防和治疗因血小板高聚集引起的心、脑及其他动脉循环障碍疾病的药物。以2氯苯甲醛为原料合成该药物的路线如下:

(1)A中官能团名称为___________。
(2)C生成D的反应类型为___________。
(3)X( C6H7BrS)的结构简式为____________________________。
(4)写出C聚合成高分子化合物的化学反应方程式:______________________________。
(5)物质G是物质A的同系物,比A多一个碳原子,符合以下条件的G的同分异构体共有___________种。
①除苯环之外无其他环状结构;②能发生银镜反应。
其中核磁共振氢谱中有5个吸收峰,且峰值比为2︰2︰1︰1︰1的结构简式为___________。
(6)已知: 。写出以乙烯、甲醇为有机原料制备化合物
。写出以乙烯、甲醇为有机原料制备化合物![]() 的合成路线(无机物任选)_____________。
的合成路线(无机物任选)_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】螺环化合物具有抗菌活性,用其制成的药物不易产生抗药性,螺[3,4]辛烷的结构如图,下列有关螺[3,4]辛烷的说法正确的是( )

A. 分子式为C8H16B. 分子中所有碳原子共平面
C. 与2—甲基—3—庚烯互为同分异构体D. 一氯代物有4种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种从废钴锰催化剂[含53.1%(CH3COO)2Co、13.2%(CH3COO)2Mn、23.8%CoCO3、6.5%Mn(OH)2、1.3%SO2及对二甲苯等有机物等]中回收钴和锰的工艺流程如下:
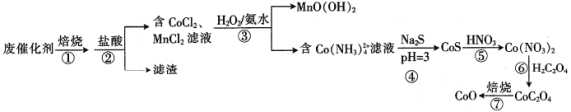
回答下列问题:
(1)步骤①焙烧的目的是_________________________________。
(2)步骤②酸浸时,控制盐酸适当过量、溶液加热并充分搅拌,其目的是___________。
(3)步骤③MnCl2与H2O2和氨水反应的离子方程式为______________________。
(4)步骤④调节pH时采用CH3COOH和CH3 COONa混合溶液,该混合溶液称为缓冲溶液,该溶液中加入少量的酸、碱或稀释时pH变化均不大,其中稀释时pH变化不大的原因是______________________。
(5)步骤⑤硝酸溶解CoS生成Co(NO3)2同时生成NO和S,该反应的化学方程式为______________________。
(6)步骤⑦若在实验室进行,所需的硅酸盐质仪器除酒精灯和玻璃棒外,还有___________(填仪器名称)。
(7)某工厂用mkg废催化剂最终制得 CoO n kg,则CoO的产率为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】98gH2SO4中
(1)分子个数是_____
(2)O原子物质的量是___mol
(3)H元素的质量是______g
(4)S原子个数是__
(5)电子的物质的量是_____mol
(6)质子的个数是_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com