
【题目】把0.8mol X 气体和0.4mol Y 气体混合于2L 密闭容器中,使它们发生如下反应:2X(g)+Y (g)n Z (g)+2W (g).2min 末已生成0.2mol W,若测知以Z的浓度变化表示的反应速率为0.05mol(Lmin)﹣1 , 计算:
(1)前2min内用X的浓度变化表示的平均反应速率;
(2)2min末时Y的浓度.
(3)化学反应方程式中n 值是多少?
【答案】
(1)解:把0.8molX气体和0.4molY气体混合于2L容器中,2min末已生成0.2molW,则:
3X(气)+ | Y(气) | ═ | nZ(气)+ | 2W(气) | |
起始量(mol): | 0.8 | 0.4 | 0 | 0 | |
变化量(mol): | 0.3 | 0.1 | 0.1n | 0.2 | |
2min末(mol): | 0.5 | 0.3 | 0.1n | 0.2 |
根据c= ![]() 计算c(X)=
计算c(X)= ![]() =0.075mol/(Lmin),答:前2min内用X的浓度变化表示的平均反应速率为0.075mol/(Lmin);
=0.075mol/(Lmin),答:前2min内用X的浓度变化表示的平均反应速率为0.075mol/(Lmin);
(2)解:根据三行式确定2min末时Y的浓度为: ![]() =0.15mol/L,
=0.15mol/L,
答:2min末时Y的浓度为0.15mol/L;
(3)解:以Z的浓度变化表示的反应速率为0.05mol(Lmin)﹣1= ![]() ,解得n=2.
,解得n=2.
答:化学反应方程式中n值是2.
【解析】把0.8molX气体和0.4molY气体混合于2L容器中,2min末已生成0.2molW,则:
3X(气)+ | Y(气) | ═ | nZ(气)+ | 2W(气) | |
起始量(mol): | 0.8 | 0.4 | 0 | 0 | |
变化量(mol): | 0.3 | 0.1 | 0.1n | 0.2 | |
2min末(mol): | 0.5 | 0.3 | 0.1n | 0.2 |
·(1)根据c= ![]() 计算c(X);(2)根据三行式确定2min末时Y的浓度;(3)根据速率计算生成Z的物质的量,进而计算n的值.
计算c(X);(2)根据三行式确定2min末时Y的浓度;(3)根据速率计算生成Z的物质的量,进而计算n的值.
【考点精析】根据题目的已知条件,利用化学平衡的计算的相关知识可以得到问题的答案,需要掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】向含有下列4种离子的溶液中加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
A. NO3- B. Ba2+ C. OH- D. Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 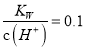 的溶液中:Na+、K+、SiO32—、SO32-
的溶液中:Na+、K+、SiO32—、SO32-
B. pH=1的溶液中:K+、Al3+、SO42-、F—
C. 与镁反应生成氢气的溶液中:Na+、Ba2+、NO3-、Cl-
D. 0.1mol/L的NaHCO3溶液中:NH4+、Mg2+、Br-、AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分, 针对表中的①~⑧种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在这些元素中,化学性质最不活泼的是:______(填具体元素符号,下同)。原子结构示意图为________________ 。元素⑦名称为_______在周期表中的位置________________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的化学式是:_____________。
(3)最高价氧化物是两性氧化物的元素是__________;写出它的氧化物与氢氧化钠反应的离子方程式__________________________________________________。
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是(写元素符号)______________。
(5)元素③的氢化物的化学式为________;该氢化物常温下和元素⑦的单质反应的化学方程式为______________________。
(6)写出⑥的最高价氧化物的水化物和①反应的化学方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常见金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H.其中B是地壳中含量最多的金属.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出). 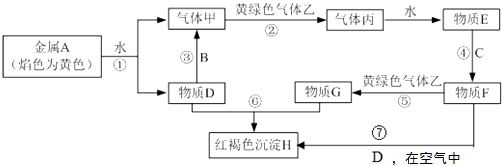
(1)写出化学式:B , G
(2)写出离子反应方程式: ③
⑦ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应,能用离子方程式H++OH-= H2O来表示的是( )
A.盐酸和氢氧化铜B.硫酸和氢氧化钠溶液
C.醋酸和氢氧化钡溶液D.稀硝酸和氨水混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是没有颜色、有刺激性气味的气体,极易溶于水且溶解得快,1体积水大约可溶解700体积氨气。在实验室里,常用氯化铵和氢氧化钙共热制取氨气。某同学用下列装置进行有关氨气制取及喷泉实验的探究,请回答。
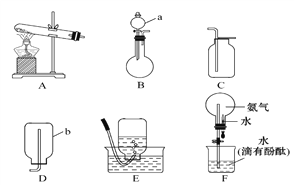
(1)写出图中所示仪器的名称:a____________,b____________。
(2)实验室制取氨气的化学方程式为_____________________________________。从图中选择相应的发生装置是________(填字母,下同),收集装置是________。
(3)某同学用收集有干燥纯净氨气的F装置进行实验观察到了红色喷泉。请描述他的关键操作是_______________________________________________。
(4)0℃、101 kPa的条件下实验结束后,烧瓶中溶液溶质的物质的量浓度为(溶质以NH3计算):____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲图中①、②、③、④表示不同化学元素所组成的化合物,乙图表示由四个单体构成的化合物,以下说法正确的是
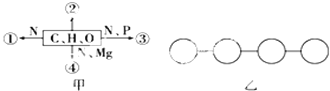
A. 甲图中的②大量存在于皮下和内脏器官周围等部位,则②只在动物细胞中能找到
B. 甲图中③是细胞中的遗传物质,则蓝藻细胞的③为DNA和RNA
C. 乙图中若单体是氨基酸,则该化合物彻底水解后的产物中氢原子数增加3个
D. 乙图中若单体是4种脱氧核苷酸,则该化合物彻底水解后的产物最多有6种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com