
����Ŀ���±���Ԫ�����ڱ���һ����, ��Ա��еĢ١�����Ԫ��,��д���пհ�:
���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� |
��1������ЩԪ����,��ѧ�������������:______(�����Ԫ�ط���,��ͬ)��ԭ�ӽṹʾ��ͼΪ________________ ��Ԫ�آ�����Ϊ_______�����ڱ��е�λ��________________��
��2��������������ˮ�����У�������ǿ�Ļ�����ķ���ʽ��_______��������ǿ�Ļ��������ѧʽ��:_____________��
��3������������������������Ԫ����__________��д���������������������Ʒ�Ӧ�����ӷ���ʽ__________________________________________________��
��4���ۡ��ޡ�������Ԫ���γɵ����ӣ����Ӱ뾶�ɴ�С��˳���ǣ�дԪ�ط��ţ�______________��
��5��Ԫ�آ۵��⻯��Ļ�ѧʽΪ________�����⻯�ﳣ���º�Ԫ�آߵĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪ______________________��
��6��д��������������ˮ����͢ٷ�Ӧ�Ļ�ѧ����ʽ��_______________��
���𰸡� Ar 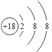 �� �������ڵڢ�A�� HClO4 NaOH Al Al2O3+2OH����2AlO2��+H2O S2����Cl����O2�� H2O Cl2+H2O=HCl+HClO C��2H2SO4(Ũ)
�� �������ڵڢ�A�� HClO4 NaOH Al Al2O3+2OH����2AlO2��+H2O S2����Cl����O2�� H2O Cl2+H2O=HCl+HClO C��2H2SO4(Ũ) ![]() CO2����2SO2����2H2O
CO2����2SO2����2H2O
������������Ԫ�������ڱ��е����λ�ÿ�֪Ԫ�آ١�����C��N��O��Na��Al��S��Cl��Ar����
(1)����ЩԪ���У���ѧ��������õ���ϡ������Ԫ��Ar��ԭ�ӽṹʾ��ͼΪ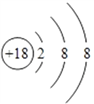 ��Ԫ�آ�����ΪCl�������ڱ��е�λ���ǵ������ڵڢ�A�壻(2)�ǽ�����Խǿ����ۺ����������Խǿ�����������������ˮ�����У�������ǿ�Ļ�����ķ���ʽ��HClO4��������Խǿ������������Ӧˮ����ļ���Խǿ���������ǿ�Ļ�����Ļ�ѧʽ��NaOH��(3)����������������������Ԫ����Al,�������������������Ʒ�Ӧ�����ӷ���ʽΪAl2O3+2OH����2AlO2��+H2O����4�����ӵĺ�����Ӳ���Խ�࣬���Ӱ뾶Խ��������Ų���ͬʱ���Ӱ뾶��ԭ���������������С����ۡ��ޡ�������Ԫ���γɵ����������Ӱ뾶�ɴ�С��˳����S2����Cl����O2������5��Ԫ�آ۵��⻯��Ļ�ѧʽΪH2O�����⻯�ﳣ���º�Ԫ�آߵĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪCl2+H2O=HCl+HClO����6��������������ˮ���������ᣬ�͢ٵĵ���̼��Ӧ�Ļ�ѧ����ʽΪC��2H2SO4(Ũ)
��Ԫ�آ�����ΪCl�������ڱ��е�λ���ǵ������ڵڢ�A�壻(2)�ǽ�����Խǿ����ۺ����������Խǿ�����������������ˮ�����У�������ǿ�Ļ�����ķ���ʽ��HClO4��������Խǿ������������Ӧˮ����ļ���Խǿ���������ǿ�Ļ�����Ļ�ѧʽ��NaOH��(3)����������������������Ԫ����Al,�������������������Ʒ�Ӧ�����ӷ���ʽΪAl2O3+2OH����2AlO2��+H2O����4�����ӵĺ�����Ӳ���Խ�࣬���Ӱ뾶Խ��������Ų���ͬʱ���Ӱ뾶��ԭ���������������С����ۡ��ޡ�������Ԫ���γɵ����������Ӱ뾶�ɴ�С��˳����S2����Cl����O2������5��Ԫ�آ۵��⻯��Ļ�ѧʽΪH2O�����⻯�ﳣ���º�Ԫ�آߵĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪCl2+H2O=HCl+HClO����6��������������ˮ���������ᣬ�͢ٵĵ���̼��Ӧ�Ļ�ѧ����ʽΪC��2H2SO4(Ũ)![]() CO2����2SO2����2H2O��
CO2����2SO2����2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��Ϊ��ѧ��ѧ�ij��������Ҿ�����ͬһ��Ԫ�أ�����֮���ת����ϵ��ͼ��ʾ����Ӧ���������������Ѿ���ȥ���� ![]()
��1����A�ǻ�ɫ���壻BΪ����ij���֮һ���ҿ�ʹƷ����Һ��ɫ����Bͨ��KMnO4��Һ������Ϊ������B����������ԡ�����ԭ�ԡ���Ư���ԡ�������д��D��Ũ��Һ�뵥��ͭ��Ӧ�Ļ�ѧ����ʽ�����˷�Ӧ������������D��μӷ�Ӧ��D�����ʵ���֮��Ϊ��
��2����A�����ʹʪ��ĺ�ɫʯ����ֽ������������D��Ũ��Һ��ʹ����Fe��Al�ۻ�����д��ʵ�����Ʊ�A�Ļ�ѧ����ʽ������д��C��D�����ӷ���ʽ ��
��3����A��һ�ֻ��ý�����C�ǵ���ɫ���壬��C������Ϊ �� ���û�ѧ����ʽ��ʾ�������������̼����ķ�Ӧ����C����¶���ڿ����У���������E��E�Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڵ���ʵ��ж��У���ȷ�Ĺ۵��ǣ� ��
A. ������״̬���ܵ��������
B. ��ˮ��Һ������״̬���ܵ��������
C. ��ˮ��Һ������״̬���ܵ���Ļ�����
D. ��ˮ��Һ������״̬�¶��ܵ���Ļ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D�������ʣ���֪��������ͬ�������ܷ�������������ѧ��Ӧ��
��A2����B===B2����A����B2����C===C2����B ��C2����D===D2����C
�ƶ�A��B��C��D�Ļ�ԭ����ǿ������˳����(����)
A. A��B��C��D B. C��A��B��D
C. B��D��A��C D. D��C��B��A
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڱ����ҵ���3����17���е�Ԫ�أ��ش��������⣺
(1)��Ԫ�صķ�����________����ԭ�ӽṹʾ��ͼΪ________
(2)��Ԫ��λ�ڵ�________���ڣ���________�塣
(3)д�����з�Ӧ�Ļ�ѧ����ʽ��
�ٸ�Ԫ�صĵ��ʣ�ˮ��_______________________________________��
�ڸ�Ԫ�صĵ��ʣ��������ƣ�_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.8mol X �����0.4mol Y ��������2L �ܱ������У�ʹ���Ƿ������·�Ӧ��2X��g��+Y ��g��n Z ��g��+2W ��g����2min ĩ������0.2mol W������֪��Z��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.05mol��Lmin����1 �� ���㣺
��1��ǰ2min����X��Ũ�ȱ仯��ʾ��ƽ����Ӧ���ʣ�
��2��2minĩʱY��Ũ�ȣ�
��3����ѧ��Ӧ����ʽ��n ֵ�Ƕ��٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ![]() ��һ������
��һ������![]() ��һ����ﶼ��4�֣������������칹��
��һ����ﶼ��4�֣������������칹��
B. CH3CH=CHCH3�����е��ĸ�̼ԭ����ͬһֱ����
C. ��ϵͳ�������������� ��������2,3,4-����-2-�һ�����
��������2,3,4-����-2-�һ�����
D. ![]() ��
��![]() ������-�������һ�Ϊͬϵ��
������-�������һ�Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�����ᴿ��ʵ���У���ѡ�õķ�������������ȷ���ǣ� ��
��� | A | B | C | D |
ʵ��Ŀ�� | ��ȡ����ˮ | ����ˮ��ֲ���� | ����ʳ��ˮ����ɳ | ��Ũʳ��ˮ�еõ��Ȼ��ƾ��� |
���뷽�� | ���� | ��Һ | ��ȡ | ���� |
ѡ������ |
|
|
|
|
A.ѡ��A
B.ѡ��B
C.ѡ��C
D.ѡ��D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��Ԫ�����ڱ���һ���֣����еĢ�~����Ԫ�أ���Ԫ�ط��Ż�ѧʽ��ջش�
���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
�� | �� | �� | ||||||
�� | �� | �� | �� | �� | �� | �� | ||
�� | �� |
��1������ЩԪ���У���ѧ��������õ�ԭ�ӵ�ԭ�ӽṹʾ��ͼΪ___________��
��2���ؿ��к������Ľ���Ԫ����____________________________��
��3��������γɵĻ�����ĵ���ʽ______________________________��
��4����ЩԪ���е�����������Ӧ��ˮ�����У�������ǿ����___________��������ǿ����____________�������Ե�����������__________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com