
| 元素 | 性质或原子结构 |
| A | 原子核内只有一个质子 |
| B | 单质是空气中含量最多的气体 |
| X | 原子的最外层电子数是次外层电子数的3倍 |
| Y | 短周期元素中原子半径最大的元素 |
| Z | 最高正化合价与最低负化合价的代数和为6 |
| 实验操作 | 实验现象 | 结论及解释 |
| ①取少量NaBr 溶液于试管中,滴加 ②再加入少量CCl4,振荡,静置. | ①溶液由无色变为橙黄色. ②溶液分层, | 氧化性:Z 单质>Br2 离子方程式 |
| 实验操作 | 实验现象 | 结论及解释 |
| ①氯水 | ②上层液体几乎为无色,下层液体为橙红色 | Cl2+2Br-═2Cl-+Br2 |


科目:高中化学 来源: 题型:
| A、CxHy |
| B、CxHy -x |
| C、CxH2y-2x |
| D、CxHy-2x |
查看答案和解析>>
科目:高中化学 来源: 题型:
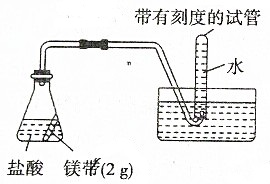 用如图所示的实验装置进行实验X及Y时,每隔半分钟分别测定放出气体的体积.下列选项中可正确表示实验X及Y的结果是( )
用如图所示的实验装置进行实验X及Y时,每隔半分钟分别测定放出气体的体积.下列选项中可正确表示实验X及Y的结果是( )| 实验 | 所用的酸 |
| X | 25mL 0.2mol/L |
| Y | 50mL 0.1mol/L |
A、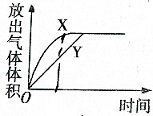 |
B、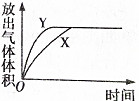 |
C、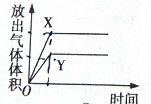 |
D、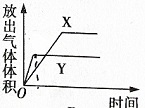 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
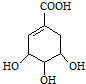
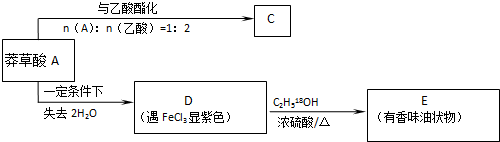
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用氢氧化钠溶液可以鉴别NH4C1和NH4NO3两种物质 |
| B、用焰色反应可以鉴别出NaCl和K2SO4两种无色溶液 |
| C、用盐酸可以鉴别NaHCO3、Na2CO3两种白色固体 |
| D、用丁达尔效应可以鉴别氢氧化铝胶体和氯化铝溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
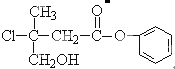
| A、属于芳香烃 |
| B、一定条件下可发生置换、加成反应、取代、酯化、水解、消去反应 |
| C、一定条件下1 mol该中间体最多可与含5 molNaOH的溶液反应 |
| D、一定条件下1 mol该中间体最多可与4 molH2反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com