
【题目】AlCl3是一种催化剂,某校学习小组用下面装置制备少量AlCl3。已知:AlCl3遇到空气中的水蒸气时能剧烈反应生成Al(OH)3和HCl;AlCl3在180℃时升华。根据要求完成下列问题:

(1)a仪器的名称为_______;A装置中反应的化学方程式为_______。
(2)试剂b为_______;C装置的作用为_______。
(3)所用d导管较粗的原因是_______;E装置的作用为_______。
(4)F装置的作用为_______。
(5)若上图中的D、E装置改为下面装置,D装置中的现象为_______;用离子方程式表示E中的现象变化_______。

【答案】 分液漏斗 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 饱和食盐水或水 干燥氯气(或除去氯气中的水蒸气) 防止三氯化铝气体冷凝为固体而堵塞导管 冷凝、收集三氯化铝 吸收氯气防止污染空气,防止空气中的水蒸气进入E装置导致三氯化铝水解 溶液变红色 Cl2+2I- = I2+2Cl-
MnCl2+Cl2↑+2H2O 饱和食盐水或水 干燥氯气(或除去氯气中的水蒸气) 防止三氯化铝气体冷凝为固体而堵塞导管 冷凝、收集三氯化铝 吸收氯气防止污染空气,防止空气中的水蒸气进入E装置导致三氯化铝水解 溶液变红色 Cl2+2I- = I2+2Cl-
【解析】(1)a仪器的名称为分液漏斗;A装置制备氯气,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。(2)生成的氯气中含有氯化氢,可用饱和食盐水除去氯气中的氯化氢,则试剂b为饱和食盐水;参加反应的氯气必须是干燥的,因此C装置的作用为干燥氯气(或除去氯气中的水蒸气)。(3)由于氯化铝的熔沸点较低,因此所用d导管较粗的原因是防止三氯化铝气体冷凝为固体而堵塞导管;E装置的作用为冷凝、收集三氯化铝。(4)氯气有毒,需要尾气处理,另外空气中含有水蒸气,因此F装置的作用为吸收氯气防止污染空气,防止空气中的水蒸气进入E装置导致三氯化铝水解。(5)氯气具有强氧化性,能把氯化亚铁氧化为氯化铁,则D装置中的现象为溶液变红色;氯气还能把碘化钾氧化生成单质碘,碘遇淀粉显蓝色,反应的离子方程式为Cl2+2I-=I2+2Cl-。
MnCl2+Cl2↑+2H2O。(2)生成的氯气中含有氯化氢,可用饱和食盐水除去氯气中的氯化氢,则试剂b为饱和食盐水;参加反应的氯气必须是干燥的,因此C装置的作用为干燥氯气(或除去氯气中的水蒸气)。(3)由于氯化铝的熔沸点较低,因此所用d导管较粗的原因是防止三氯化铝气体冷凝为固体而堵塞导管;E装置的作用为冷凝、收集三氯化铝。(4)氯气有毒,需要尾气处理,另外空气中含有水蒸气,因此F装置的作用为吸收氯气防止污染空气,防止空气中的水蒸气进入E装置导致三氯化铝水解。(5)氯气具有强氧化性,能把氯化亚铁氧化为氯化铁,则D装置中的现象为溶液变红色;氯气还能把碘化钾氧化生成单质碘,碘遇淀粉显蓝色,反应的离子方程式为Cl2+2I-=I2+2Cl-。


科目:高中化学 来源: 题型:
【题目】下列变化发生了氧化反应的是
A.Cl2+2e-=2Cl- B.S2--2e-=S
C.Ag++e-=Ag D.Cr2O72-+14H++6e-=2Cr3++7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下非固态的物质是( )
A.软脂酸(C15H31COOH)
B.油酸(C17H33COOH)
C.草酸(HOOC﹣COOH)
D.氨基酸(H2N﹣CH2COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液遇石蕊试液显红色,下列各组离子中能在该溶液中大量共存的是( )
A.H+、NO3-、Ca2+、Cl-
B.Cu2+、SO42-、HCO3-、Na+
C.Fe2+、NO3-、OH-、Ba2+
D.MnO4-、SO42-、NO3-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计下面流程来探究含铝、铁、铜合金废料的再利用。按要求完成下列问题:

(1)试剂X为_______,试剂Y为_______ 。
(2)反应②的离子反应方程式为_______。
(3)检验滤液C中是否含有Fe3+的操作为_______。
(4)操作III的名称为_______,该操作所用的玻璃仪器为_______。
(5)实验室保存FeSO4溶液时常加入铁粉,加入铁粉的作用是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G七种元素,它们的原子序数依次增大。A在所有元素中原子半径最小;B原子核外电子有6种不同运动状态;D与C、E均相邻;A、D、E三种元素的原子序数之和为25;E2-和F+有相同的核外电子排布;G的质子数是25。请回答下列问题:
(1)写出元素G的基态原子外围电子排布式________;B、C、D三种元素分别形成的最简单氢化物的沸点最高的是________(用化学式表示)。
(2)由上述元素中的两种元素组成的一种阴离子与D的一种同素异形体分子互为等电子体,该阴离子化学式为________。
(3)由上述元素组成的属于非极性分子且VSEPR为直线形的微粒的电子式________(任写一种)。
(4)M是由4个C原子组成的一种不稳定的多原子单质分子,M分子中C原子杂化方式为sp3杂化,M分子的立体构型为________。
(5)某一次性电池的比能量和可储存时间均比普通干电池优良,适用于大电流和连续放电,是民用电池的升级换代产品之一,它的负极材料是Zn,正极材料是G的一种常见氧化物,电解质是KOH。该电池的正极反应式为______________。
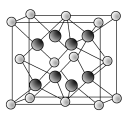
(6)由上述元素中电负性最大的元素和第一电离能最小的元素形成的某化合物N的晶胞如右图所示。化合物N与氧化钙相比,晶格能较小的是______(填化学式)。已知该化合物的晶胞边长为a pm,则该化合物的密度为________g·cm-3(只要求列出算式,不必计算出数值,阿伏加德罗常数的数值为NA,1 pm=10-10cm)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将H2、 N2、O2三种气体分别放入不同容器,使它们温度、密度相同,则其压强(p)大小的关系符合
A.p(H2)>p(O2)>p(N2) B.p(O2)>P(N2)>p(H2)
C.p(H2)>P(N2)>p(O2) D.P(N2)>p(O2)>p(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A. 碳酸氢钠可用于治疗胃酸过多的药物
B. 明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
C. 二氧化硫有漂白性,可以用来漂白食物
D. 常温下,用铁、铝制容器来盛装浓硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com