
【题目】某同学设计下面流程来探究含铝、铁、铜合金废料的再利用。按要求完成下列问题:

(1)试剂X为_______,试剂Y为_______ 。
(2)反应②的离子反应方程式为_______。
(3)检验滤液C中是否含有Fe3+的操作为_______。
(4)操作III的名称为_______,该操作所用的玻璃仪器为_______。
(5)实验室保存FeSO4溶液时常加入铁粉,加入铁粉的作用是_______。
【答案】 氢氧化钠溶液(或NaOH溶液) 稀硫酸(或稀H2SO4) [Al(OH)4]-+CO2===HCO3-+Al(OH)3↓ [或AlO2-+CO2+2H2O===HCO3- +Al(OH)3↓] 取少量滤液C于试管中,滴加KSCN溶液,若溶液不变红则不含Fe3+(若溶液变红色则含Fe3+) 过滤 漏斗、玻璃棒、烧杯 防止Fe2+被氧化
【解析】(1)滤液A中通入CO2生成沉淀B,B最终转化为氧化铝,所以B是氢氧化铝,A中含有偏铝酸根,则试剂X为NaOH溶液。滤渣A是铁和铜,滤液C最终转化为绿矾,则滤液C中含有亚铁离子,则试剂Y为稀硫酸。(2)根据以上分析可知反应②的离子反应方程式为AlO2-+CO2+2H2O=HCO3- +Al(OH)3↓。(3)铁离子和KSCN溶液反应显红色,检验滤液C中是否含有Fe3+的操作为取少量滤液C于试管中,滴加KSCN溶液,若溶液不变红则不含Fe3+。(4)操作III的名称为过滤,该操作所用的玻璃仪器为漏斗、玻璃棒、烧杯。(5)亚铁离子易被氧化,实验室保存FeSO4溶液时常加入铁粉的作用是防止Fe2+被氧化。


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
【题目】下列变化过程中,生成物总能量高于反应物总能量的化学反应是( )
A. 浓硫酸溶于水 B. 干冰气化
C. 镁与盐酸混合 D. 氢氧化钡与氯化铵混合搅拌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】节日期间因燃放鞭炮会引起空气中SO2含量增高,造成大气污染。某实验小组同学欲探究SO2的性质,并测定空气中SO2的含量。
(1)他们设计如下实验装置,请你参与探究,并回答问题:
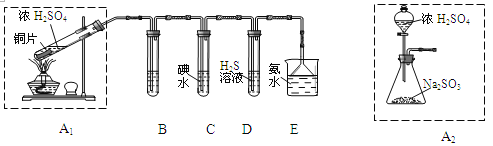
①装置A1中发生反应的化学方程式为 ;
②装置B用于检验SO2的漂白性,其中所盛试剂为 ,装置D用于检验SO2的 性质;
③装置C中反应的离子方程式为 ;
④为了实现绿色环保的目标,甲同学欲用装置A2代替装置A1,你认为装置A2的优点是(写二点) 、 ;
(2)他们拟用以下方法测定空气中SO2含量(假设空气中无其他还原性气体)。
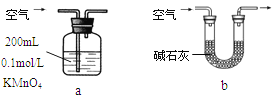
①你认为哪个装置可行(填序号) ,使用你所选用的装置测定SO2含量时,还需要测定的物理量是 ;
②你认为哪个装置不可行(填序号) ,说明理由 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法正确的是( )
A.明矾可用作净水剂
B.甲醛可用作食品防腐剂
C.氢氧化钠可用来治疗胃酸过多
D.铝制容器可长期存放酸性食物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AlCl3是一种催化剂,某校学习小组用下面装置制备少量AlCl3。已知:AlCl3遇到空气中的水蒸气时能剧烈反应生成Al(OH)3和HCl;AlCl3在180℃时升华。根据要求完成下列问题:

(1)a仪器的名称为_______;A装置中反应的化学方程式为_______。
(2)试剂b为_______;C装置的作用为_______。
(3)所用d导管较粗的原因是_______;E装置的作用为_______。
(4)F装置的作用为_______。
(5)若上图中的D、E装置改为下面装置,D装置中的现象为_______;用离子方程式表示E中的现象变化_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国学者成功发现了新一类水分解产氢催化剂:通过调控三氧化钨(WO3)局部原子结构,制备出深蓝色钨氧化物(WO2.9),该种钨的氧化物能高效而快速地催化水分解产生H2。下列有关说法正确的是( )

A. WO3和WO2.9是同分异构体
B. 由WO3制备WO2.9的过程发生了氧化还原反应
C. 18gH2O在WO2.9的高效催化下产生H2体积为22.4L
D. 利用这种新型催化剂分解水的同时可放出热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与11.2L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入2mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A. 2L B. 1 L C. 0.5L D. 3L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com