
����Ŀ��25��ʱ����10mL0.1mol��L��1һԪ����XOH��Һ����εμ�0.1mol��L��1��HCl��Һ����Һ��AG[AG=lg![]() ]�仯��ͼ��ʾ(��Һ���ʱ����仯���Բ���)������˵����ȷ����
]�仯��ͼ��ʾ(��Һ���ʱ����仯���Բ���)������˵����ȷ����
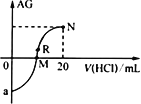
A.��a=-8����25��ʱ��0.1mol��L��1XOH��Һ��pH=8
B.M���ʾ�����XOHǡ����ȫ��Ӧ
C.R����Һ�п��ܴ���c(X��)+c(XOH)=c(Cl��)
D.M�㵽N�㣬ˮ�ĵ���̶���С
���𰸡�C
��������
A��a=��8����lg![]() =-8������Һ��c(H��)��c(OH��)=10-14�����c(H��)=10��11mol/L��pH=11��A����
=-8������Һ��c(H��)��c(OH��)=10-14�����c(H��)=10��11mol/L��pH=11��A����
B��������XOH��ȫ��Ӧ����XCl��Ϊǿ�������Σ���Һ�����ԣ�lg![]() >0����M��AG=0����Һ�����ԣ�B����
>0����M��AG=0����Һ�����ԣ�B����
C����c(X��)+c(XOH)=c(Cl��)��˵��������XOH��ȫ��Ӧ����XCl��Ϊǿ�������Σ���Һ�����ԣ�lg![]() >0��C��ȷ��
>0��C��ȷ��
D��������XOH��ȫ��Ӧ����XCl��Ϊǿ�������Σ���Һ�����ԣ�lg![]() >0����ʱˮ�ĵ���̶����ΪM��N�е�ijһ���㣬���M�㵽N�㣬ˮ�ĵ���̶���������С��D����
>0����ʱˮ�ĵ���̶����ΪM��N�е�ijһ���㣬���M�㵽N�㣬ˮ�ĵ���̶���������С��D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ����Ҫ�Ļ���ԭ�ϡ���ʵ�����Ʊ��������£�

�ش��������⣺
����ϩ���Ʊ����ᴿ
(1)ԭ�ϻ������������������ʣ������Լ�Ϊ____________������Ϊ__________________��
(2)����1![]() װ����ͼ��ʾ�����Ⱥͼг�װ������ȥ����
װ����ͼ��ʾ�����Ⱥͼг�װ������ȥ����

����ƿA�н��еĿ��淴Ӧ��ѧ����ʽΪ________________________
������B������Ϊ____________��
(3)������3�����IJ��貹�룺��װ����װ�ã��������������ʺͷ�ʯ��____________����ȥǰ��֣��ռ�83�����֡�
����ϩ�����IJⶨ
��һ�������£���![]() ����ϩ��Ʒ�м��붨���Ƶõ�
����ϩ��Ʒ�м��붨���Ƶõ�![]() ���뻷��ϩ��ַ�Ӧ��ʣ���
���뻷��ϩ��ַ�Ӧ��ʣ���![]() ������
������![]() ��������
��������![]() �����ɵ�I2��
�����ɵ�I2��![]() ��
��![]() ����Һ���䷴Ӧ��ǡ������
����Һ���䷴Ӧ��ǡ������![]() ����Һ
����Һ![]() ���������ݾ��ѿ۳��������أ���
���������ݾ��ѿ۳��������أ���
�ⶨ�����У������ķ�Ӧ���£���![]()
��![]() I2+2Na2S2O3=2NaI+Na2S4O6
I2+2Na2S2O3=2NaI+Na2S4O6
(4)������Ʒ�л���ϩ����������Ϊ____________������ĸ��ʾ����
(5)��������ᵼ�²ⶨ���ƫ�͵���____________������ţ���
a����Ʒ�к��б������� b���ڲⶨ�����в��ֻ���ϩ�ӷ� c��![]() ����Һ���ֱ�����
����Һ���ֱ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д����ȷ����(����)
A.������Na2SiO3��Һ��ϣ�SiO![]() ��2H��===H2SiO3��
��2H��===H2SiO3��
B.Cl2��NaOH��Һ��Ӧ��Cl2��2OH��===Cl����ClO����H2O
C.��������������Һ�еμ�����������Һ��H����HSO![]() ===SO2����H2O
===SO2����H2O
D.���������Һ�м�������������Һ��Ba2����SO![]() ===BaSO4��
===BaSO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݵ���������Ӧ���Ȼ�ѧ����ʽ
�� I2��g��+ H2��g��![]() 2HI��g�� ��H����9.48 kJ/mol
2HI��g�� ��H����9.48 kJ/mol
�� I2��s��+ H2��g��![]() 2HI��g�� ��H��+26.48 kJ/mol
2HI��g�� ��H��+26.48 kJ/mol
�����ж���ȷ����
A.254g I2��g����ͨ��2gH2��g������Ӧ����9.48 kJ
B.1 mol��̬����1 mol��̬���������������17.00 kJ
C.��Ӧ�ڵķ�Ӧ���������ȷ�Ӧ�ٵķ�Ӧ����������
D.��Ӧ�ٵIJ���ȷ�Ӧ�ڵIJ����ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ���������ֵ������˵����ȷ����
A.28g��ϩ���ϩ������к�C-H������ĿΪ4NA
B.��״���£�22.4L������11.2LH2���е���������ΪNA
C.1mol Cl2������������һ�������³�ַ�Ӧ��ת����3NA����
D.25��ʱ��1LpH=11��NaOH��Һ��1LpH=11��CH3COONa��Һ��������������Ϊ10-11NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ�ֻ���ɫ���д̼�����ζ�����壬����������ˮ�������߱��ʵȷ��档�����ƻ�ԭ����Ŀǰʹ�ý�Ϊ�㷺��ClO2�Ʊ�����������һ������NaClO3��CH3OH�ڴ�����60��ʱ��������Ӧ�õ�ClO2����ͼװ��(�г�װ����)�����Ʊ������ա��ͷŽ������о���
��֪��
��ClO2��Ũ�Ƚϴ�ʱ�ֽ⣬ʵ�������ȶ�������ClO2������NaClO2��ʹ��ʱ����ֻ�ͷų�ClO2һ�����壻
��ClO2��KI��Ӧ�����ӷ���ʽΪ��2ClO2��10I��8H+=2Cl��5I2��4H2O��
��![]()

��ش�
��1���Ƚ�����c��d��ʵ����c���ŵ���___��
��2���Ʊ�װ�ü�����Ľ���һ���ʩ��___��
��3����Ӧ�м״�������Ϊ���ᣬд���Ʊ�ClO2�Ļ�ѧ����ʽ��___�����Ʊ�����ѡ�ò�ͬ�Ļ�ԭ��������Ϊ��ԭ����������ᣬ��ȼ״��������ᷨ���ŵ���___��
��4�������й�˵����ȷ����___��
A������a��NaOH��Һ��Ҫ����ֹͣ��Ӧ�������ն����ClO2
B��װ��e��Ҫ���ڼ����Ƿ���Cl2����
C����ClO2�ͷ�ʵ���У����������ӷ�Ӧ����ʽ�ǣ�4H+��5ClO2-=Cl��4ClO2����2H2O
D��ClO2��Cl2��Ϊǿ������������ͬ�����£������ʵ���ʱ��ClO2������������Cl2��2.5��
��5������ˮ���õ��������ˮ��ClO2��Ũ�ȣ���ʵ��������£�ȡ100.0mL��ˮ�������������ĵ⻯�أ���������������Һ�������ԣ������������Һ������0.1000mol��L1Na2S2O3����Һ�ζ��ⵥ��(I2��2S2O32-=2I��S4O62-)���ﵽ�ζ��յ�ʱ��ȥ20.00mLNa2S2O3����Һ����ø�ˮ����ClO2�ĺ���Ϊ___mg��L1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС���±�ؼ��仯������Ʊ������ʽ�������̽��ʵ�飬����ʵ��ش����⡣
I.̽���Ȼ�������������Ӧ�IJ���
��֪�Ȼ��������۵�Ϊ674�棬�е�Ϊ1023�棻���Ȼ�����100������ʱ����������ˮ�⡣��500���������Ȼ��������������ܷ������з�Ӧ��12FeCl2+3O2![]() 2Fe2O3+8FeCl3��4FeCl2+3O2
2Fe2O3+8FeCl3��4FeCl2+3O2![]() 2Fe2O3+4Cl2���û�ѧС��ѡ����ͼ����װ��(װ�ÿ����ظ�ѡ��)�����Ȼ�������������Ӧ�����̽����
2Fe2O3+4Cl2���û�ѧС��ѡ����ͼ����װ��(װ�ÿ����ظ�ѡ��)�����Ȼ�������������Ӧ�����̽����

(1)ʵ��װ�õĺ�������˳��Ϊ��A��__________��D��װ��E��������___________��
(2)D�з�����Ӧ�����ӷ���ʽ_______��
(3)ij��ѧ��ȤС���ڿ�����500���·�����Ӧ��һ��ʱ���IJ������������ʵ��̽����
�ٶ�B�з�Ӧʣ�����ijɷֿ�չʵ��̽�����������������ּ��裺
����һ������ΪFe2O3��
�����������Ϊ________(�ѧʽ)��
���������������һ��չ��ʵ���о����������������
ʵ����� | Ԥ����������� |
ȡ����������Ʒ��һ֧�ྻ���Թ��У���������������ˮ�� | ______�������һ������������һ�������� |
�ڶԹ������(��״����)�ɷֺ�������������ʵ��̽����B�з�Ӧʣ�������������ⶨΪm1g ��E����������������ⶨΪm2g��B�з�Ӧʣ����尴̽���ٵ�ʵ�鲽����в����������յõ����﴿���Ĺ�������Ϊm3g������������Fe2O3��ռ����������Ϊ______��
��.±�ػ�����֮�䷴Ӧʵ����������̽��
(4)�����£�KClO3�ɽ�KI����ΪI2��KIO3�������Ǹ�С����Ƶ�һ��ʵ�����ݼ�¼����
�Թܱ�� | 1 | 2 | 3 | 4 |
0.20 mol��L-1KI��Һ/ mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0 mol��L-1H2SO4��Һ/ mL | 0 | 3.0 | 6.0 | 9.0 |
����ˮ/mL | 9.0 | 6.0 | 3.0 | 0 |
��Ӧ��ȫ�μ�2�ε�����Һ | ��ɫ | ��ɫ | ��ɫ��2dz | ��ɫ |
�ٸ���ʵ�����ݣ������ѧ��ѧ֪ʶ������˵����ȷ����______
A.��ʵ��Ŀ����̽������������ͬʱ�����Ũ�ȶԷ�Ӧ�����Ӱ��
B.ʵ��1��ʵ��4˵������Ũ��̫�ͻ�̫Ũ��KClO3��KI������Ӧ
C.ʵ��2������˵���ڸ�����Ũ����KClO3��KI����ΪI2
D.ʵ��3��ɫ��2dz��ԭ�����ڸ�����Ũ���µ��۲���ˮ��
��2���Թܷ�Ӧ��ȫ���軹ԭ����ֻ��KC1��д����Ӧ�����ӷ���ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pH=11��X��Y���ּ���Һ��10mL���ֱ�ϡ����1000mL����pH����Һ�����V���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��

A. X��Y���ּ�����ʵ���Ũ��һ�����
B. ϡ�ͺ�X��Һ���Ա�Y��Һ����ǿ
C. ��9��a��11����X��Y��������
D. ��ȫ�к�X��Y����Һʱ������ͬŨ����������VX��VY
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2CO(g)��O2(g)=2CO2(g)����H����566 kJ/mol��Na2O2(s)��CO2(g)=Na2CO3(s)��![]() O2(g)����H����226 kJ/mol�����������Ȼ�ѧ����ʽ�ж�����˵����ȷ����( ��)
O2(g)����H����226 kJ/mol�����������Ȼ�ѧ����ʽ�ж�����˵����ȷ����( ��)

A.CO��ȼ����Ϊ283 kJ
B.��ͼ��ʾΪCO����CO2�ķ�Ӧ���̺������Ĺ�ϵ
C.2Na2O2(s)��2CO2(s) =2Na2CO3(s)��O2(g)��H>��452 kJ/mol
D.CO(g)��Na2O2(s)��Ӧ�ų�509 kJ����ʱ��ת�Ƶ�����Ϊ6.02��1023
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com