
【题目】在下列实验中必须要用到温度计的是 ( )
A. 在实验室中蒸馏石油 B. 由苯制溴苯
C. 由甲苯制TNT D. 由苯制一硝基苯
科目:高中化学 来源: 题型:
【题目】从含铜丰富的自然资源黄铜矿(主要成分为CuFeS2)中冶炼铜的工艺流程如下:

已知: ![]() 。
。
(1)若“过滤1”所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为______。
(2)“除硫”时加入浓盐酸发生反应的离子方程式为_____________________________。
(3)“过滤3”所得滤液中可以循环使用的物质为______________、_____________。
(4)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,发生的反应为![]() 、
、![]() 。此工艺与前一工艺相比主要缺点有______________________(任答一点)。
。此工艺与前一工艺相比主要缺点有______________________(任答一点)。
(5)铜溶解于H2O2和H2SO4的混合溶液中可制备CuSO4。测定溶液中Cu2+浓度的方法:准确量取V1 mL溶液于锥形瓶中,调节pH至3~4,加入过量KI溶液,充分反应后,滴加2滴淀粉溶液,再慢慢滴加c mol/L的Na2S2O3标准溶液至恰好完全反应,消耗Na2S2O3标准溶液V2 mL。上述过程中发生的反应为![]() 、
、![]() 。
。
①“恰好完全反应”时溶液的颜色变化为___________________。
②溶液中Cu2+的物质的量浓度为________________________(用含c、V1、V2的代数式表示)mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)标准状况下有以下四种气体:
①6.72 L CH4 ②3.01×1023个HCl分子 ③2.404×1023个H2S分子 ④0.2 mol NH3
a.物质的量由小到大的顺序_____________________________________
b.质量由小到大的顺序_________________________________________
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为________,R的相对原子质量为________。含R的质量为1.6 g的Na2R,其物质的量为________。
(3)在标准状况下,由CO和CO2组成的混合气体6.72 L,质量为12 g。此混合物中:混合气体的平均相对分子质量是________,对氢气的相对密度是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高纯H2为燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命。
(1)以甲醇为原料制取高纯H2是重要研究方向。甲醇水蒸气重整制氢主要发生以下两个反应:
主反应:CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g) △H=+49 kJmol-1
CO2(g)+3H2(g) △H=+49 kJmol-1
副反应:H2(g)+CO2(g)![]() CO(g)+H2O(g) △H=+41 kJmol-1
CO(g)+H2O(g) △H=+41 kJmol-1
①甲醇在催化剂作用下裂解可得到H2和CO,则该反应的化学方程式为_________________________,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是_________________________。
②分析适当增大水醇比(nH2O∶nCH3OH)对甲醇水蒸气重整制氢的好处_________________________。
③某温度下,将nH2O∶nCH3OH =1∶1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为_________________________。(忽略副反应)
(2)工业常用CH4 与水蒸气在一定条件下来制取H2,其原理为:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+203kJ·mol-1
①该反应的逆反应速率表达式为; V逆=k·c(CO)·c3(H2),k为速率常数,在某温度下,测得实验数据如表:
CO浓度(mol·L-1) | H2浓度(mol·L-1) | 逆反应速率(mol·L-1·min-1) |
0.05 | C1 | 4.8 |
c2 | C1 | 19.2 |
c2 | 0.15 | 8.1 |
由上述数据可得该温度下,上述反应的逆反应速率常数k 为__________L3·mol-3·min-1。
②在体积为3L的密闭容器中通入物质的量均为3mol 的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度及压强的关系如图所示,则压强Pl_____P2(填“大于”或“小于”)温度T3_______T4(填“大于”或“小于”);压强为P1时,在N点; v正_______v逆(填“大于”或“小于”或“等于”)。求N点对应温度下该反应的平衡常数 K=_____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO 易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5; [Cu(NH3)2]Ac 溶液用于除去CO的化学反应方程式:[Cu(NH3)2]Ac+CO+NH3=[Cu(NH3)3] Ac·CO (式中Ac-代表醋酸根)。请回答下列问题:
(1)C、N、O的第一电离能最大的是_____________,原因是___________________________。基态Fe 原子的价电子排布图为___________________________。
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是_____________,羰基铁的结构如图,根据该图可知CO作为配位体是以__________原子为配位原子与Fe原子结合。

(3)离子水化能是气态离子溶于大量水中成为无限稀释溶液时释放的能量。离子在溶液中的稳定性可以从离子的大小、电荷、水化能等因素来解释。Cu2+和Cu+的水化能分别是-2121kJ·mol-1和-582 kJ·mol-1,在水溶液里Cu2+比Cu+稳定的原因是_______________________________。[Cu(NH3)2]+在水溶液中相对稳定,在配合物[Cu(NH3)2]Ac中碳原子的杂化类型是________________________________。
(4)用[Cu(NH3)2]Ac除去CO的反应中,肯定有形成________________。
a.离子键 b.配位键 c.非极性键 d. σ键
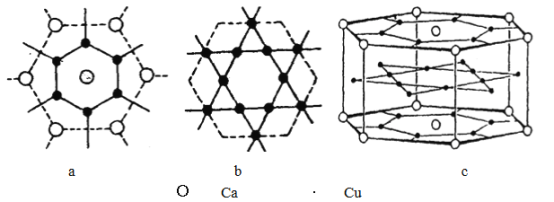
(5)钙铜合金的晶体结构可看成(a) (b) 两种原子层交替堆积排列而成图(c),则该合金六方晶胞(即平行六面体晶胞)中含为Cu________个。已知同层的Ca-Cu的距离为294pm,根据图示求同层相邻Ca-Ca的距离__________pm (已知![]() =1.73 计算结果保留整数)。
=1.73 计算结果保留整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物M 分子的模型如图所示,其中不同颜色的球表示不同的原子,其中原子之间的化学键可以是单键、双键或叁键。关于该有机物M的说法正确的是
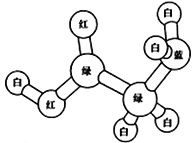
A. 难溶于水,易溶解于烧碱溶液
B. 同一平面上最多有6个原子
C. 含有不饱和键,可以发生加聚反应生成高分子化合物
D. 分子中含有两种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①已知t℃时AgCI的Ksp=2×10-10;②在t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是

A.在t℃时,Ag2CrO4的Ksp为1×10-9
B.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点
C.在t℃时,以0.01 mol/LAgNO3溶液滴定20 mL 0.01 mol/L KCI和0.01 mol/L的K2CrO4的混和溶液,CrO42-先沉淀
D.在t℃时,反应Ag2CrO4(s)+2Cl-(aq)![]() 2AgCl(s)+CrO42-(aq)的平衡常数K=2.5×107
2AgCl(s)+CrO42-(aq)的平衡常数K=2.5×107
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com