
【题目】一定条件下能与C2H6发生反应的物质是
A.溴水B.HClC.Cl2D.NaOH
科目:高中化学 来源: 题型:
【题目】(1)3.01×1023个CO2分子中含______mol氧原子,在标准状况下其体积为______L,它与______gH2O含有相同的氧原子数。
(2)同温同压下,等质量的N2和CO2所含分子数比为______,体积比为______。
(3)某气体在标准状况下的密度为1.25gL-1,则28g该气体所含有的分子数为______。
(4)在标准状况下,22.4L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为___g。
(5)同温同压下,同体积的H2和A气体的质量分别为1.0g和16.0g,则A的相对分子质量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.热水瓶胆中的水垢可以用食醋除去
B.可以用淀粉溶液检验加碘盐中是否含碘元素
C.在蔗糖中加入浓硫酸出现黑色物质, 说明浓硫酸具有脱水性
D.做红烧鱼时,常加一些食醋和酒会更香,是因为生成少量的酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6.4gSO2和8.0gSO3相比较,下列结论中错误的是
A.它们所含氧原子数目之比为2:3
B.它们的体积之比为1:1
C.它们所含原子数目之比为3:4
D.它们的分子数目之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学平衡移动原理同样也适用于其他平衡。已知在氨水中存在下列平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4+ +OH-
NH4+ +OH-
(1)向氨水中加入MgCl2固体时,平衡向____移动,OH-的浓度____(填“增大”“减小”或“不变”,下同), NH4+的浓度____。
(2)向氨水中加入浓盐酸,平衡向____移动。
(3)向浓氨水中加入少量NaOH固体,平衡向____移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图为实验室某浓盐酸试剂瓶上的有关数据,该浓盐酸中HCl的物质的量浓度为________mol/L。某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.3 mol/L稀盐酸:

(2)该学生需要量取_______mL上述浓盐酸进行配制。
(3)配制过程中,除需要使用烧杯、量筒、玻璃棒外,还需要使用的仪器是(填写名称)_______、_______。
(4)配制时,其正确的操作顺序是(要求用字母表示,每个字母只能用一次)_____________________;
A.用30mL蒸馏水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量蒸馏水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加蒸馏水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻线1~2cm处
(5)在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏高的是_____________________
A.摇匀后静置,发现液面低于刻度线,继续加水至与刻度线相切
B.溶液注入容量瓶前没有恢复到室温就进行定容
C.定容时仰视刻度线
D.在配制前用已知浓度的稀盐酸润洗容量瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Co3O4是制备石墨烯电池正极材料LiCoO2的原料。以钴矿石(主要成分为Co3S4,含有少量FeO、Fe2O3、Al2O3等杂质)为原料制取Co3O4的工艺流程如下:
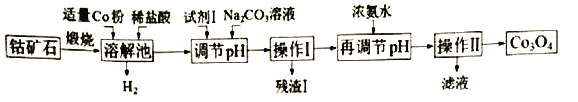
已知:Co与Fe为活泼金属,氧化性由强到弱的顺序为:Co3+>Fe3+>Co2+。
几种氢氧化物的溶度积如下表:
![]()
(l)写出溶解池中生成H2的离子反应方程式是____。
(2)加入试剂1的目的是将Fe2+氧化为Fe3+.试剂l可选用__ 。
A.氯化钠 B.双氧水 C.亚硫酸钠 D.碘水
(3)残渣l的主要成分为____。用浓氨水再调节pH,pH应略大于___ 。(已知:lg2=0.3.当离子浓度小于l.0×l0-5mol/L,可认为沉淀完全)。
(4)操怍Ⅱ包括____、____、干燥,灼烧四个步骤;灼烧中反应的化学方程式 _________。
(5)要得到15.0g质量分数为98%的LiCoO2正极材料,理论上需要Co3O4的质量为 __________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com