
设NA为阿伏加德罗常数的数值,下列说法正确的是 ( )。
A.常温常压下,8 g O2含有4NA个电子
B.1 L 0.1 mol·L-1的氨水中有0.1NA个NH4+
C.标准状况下,22.4 L盐酸含有NA个HCl分子
D.1 mol Na被完全氧化生成Na2O2,失去2NA个电子
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
下列叙述不正确的是
A.水受热不易分解,与水分子之间存在氢键无关
B.有化学键断裂的变化不一定是化学变化
C.熔化状态下能导电的物质不一定是离子化合物
D.易溶于水的物质一定是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应过程中体系的能量变化如图所示,下列说法错误的是
A.反应过程可表示为A+BC—→[A…B…C] —→AB+C
(反应物) (过渡态) (产物)
B.E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能
C.正反应的热效应为△H=E1—E2,且E2>E1,所以正反应为放热反应
D.此图中逆反应的热效应△H=E1—E2,为吸热反应

查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X的最外层电子数是电子层数的3倍,X、M同主族,Y的原子在短周期主族元素中原子半径最大。下列说法正确的是
A.M与X形成的化合物对应的水化物一定是强酸
B.Y2X和Y2X2中化学键类型完全相同
C.X、Y的简单离子半径:r(X2-)>r(Y+)
D.M的气态氢化物比N的气态氢化物稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表是学习物质结构与性质的重要工具。下表是元素周期表的一部分,表中所列字母A、B、D、E、G、H、Q、M、R分别代表某一化学元素。请用所给元素回答下列问题。
| A | |||||||||||||||||
| M | B | D |
| ||||||||||||||
| G | H |
|
| Q | R | ||||||||||||
| E |
| ||||||||||||||||
(1)Q元素在元素周期表中的位置 ,E元素原子结构示意图为
(2)E、Q、R三种元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)_________________________________。
(3)M、D两元素形成的化合物中含有的化学键类型是 ,其MD2分子的结构式:
(4)用电子式表示物质GDA_________________; 用电子式表示G与Q形成化合物的过程 ;
(5)用表中所给元素组成反应物,请各用一个化学方程式说明元素Q和R非金属性的强弱: ;元素G、H的金属性强弱:
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述错误的是 ( )。
A.18 g H2O中含有的质子数为10NA
B.12 g金刚石中含有的共价键数为4NA
C.46 g NO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电
子
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的数值,下列说法正确的是
( )。
A.25 ℃时,pH=2的1.0 L H2SO4溶液中含有H+的数目为0.02 NA
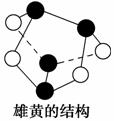
B.0.5 mol雄黄(As4S4,所有原子都满足8电子结构, 结构如图)含有NA个S—S键
结构如图)含有NA个S—S键
C.39 g苯分子中共含6 NA个共价单键
D.向FeI2、NaBr的混合溶液中通入适量氯气,当有1 mol Fe2+被氧化时,该反应转移电子的数目至少为3 NA
mol Fe2+被氧化时,该反应转移电子的数目至少为3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在指定环境中,下列各组离子一定可以大量共存的是 ( )。
A.使pH试纸呈红色的溶液中:Fe2+、ClO-、SO42-、Na+
B.在pH=3的溶液中:Na+、NO3-、Cl-、Al3+
C.由水电离出的c(H+)=10-13 mol·L-1的溶液中:CO32-、SO42-、Cl-、 Na+
D.加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com