
(10分)按要求回答问题:
Ⅰ(1)硫酸酸化的高锰酸钾溶液与草酸反应离子方程式
(2)硫代硫酸钠与硫酸反应的化学方程式
Ⅱ工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2和CO的燃烧热(△H)分别为?890.3kJ?mol?1、?285. 8 kJ?mol?1和?283.0 kJ?mol?1,则生成1m3(标准状况)CO所需热量为
kJ
Ⅲ 请写出下列物质电子式
CO2 H2O2 NH4Cl N2H4
I:(1)5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O (2)S2O32-+2H+=S↓+SO2↑+H2O
Ⅱ 5.52×103kJ III 略
解析试题分析:I:(1)草酸具有还原性,被酸性高锰酸钾氧化成二氧化碳,高锰酸钾还原成Mn2+;(2)硫代硫酸根离子和酸反应生成硫单质和二氧化硫气体;II:写出三者燃烧热的热化学方程式,①-②×2-③×2可得生成2molCO时吸收的热量为247.3KJ,生成1molCO时放出的热量为123.65KJ,用1000L除以22.4L得出CO的物质的量,再乘以123.65得所需的热量;(3)电子式的书写注意先分清是离子化合物还是共价化合物,共价化合物形成共价键,离子化合物有阴阳离子。
考点:离子方程式的书写、反应热的计算、电子式的书写等知识。


科目:高中化学 来源: 题型:单选题
设nA是阿伏加德罗常数的数值,下列说法正确的是
| A.23gNO2和N2O4的混合气体中含有的氮原子数为0.5nA |
| B.4.2 g丙烯中所含的共价键数目为0.6nA |
| C.1 L 0.1 mol/L的Fe2(SO4)3溶液中,Fe3+的数目为0.2 nA |
| D.过氧化氢分解制得标准状况下1.12 L O2,转移电子数目为 0.2 nA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一块表面已被氧化为氧化钠的钠块5.4g,投入50g水中,最多能产生0.10g气体,则原来被氧化的钠是( )
| A.2.3g | B.3.1g | C.4.6g | D.5.3g |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
NA代表阿伏加德罗常数,下列说法正确的是( )
| A.标准状况下,22.4 LSO3中含有的分子数为NA |
| B.100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA |
| C.0.1mol/L稀硫酸中含SO42-的数目为0.1NA |
| D.标准状况下,11.2LNO和5.6LO2混合后,分子总数小于0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(7分)
(1)利用Zn+2FeCl3=ZnCl2+2FeCl2反应,设计一个原电池,写出电极反应式。 正极 ,负极 ,电解质溶液 ,电极反应式 、 。
(2)下列操作中能使所配制的NaOH溶液浓度偏高的是
A 称量的是长期暴露在空气中的NaOH
B 容量瓶不干燥
C 将溶解于烧杯中的NaOH溶液未经冷却就转移到容量瓶中进行配制。
D 混匀容量瓶中溶液后,发现液面低于刻度线,再向容量瓶中加蒸馏水至刻度线
E.定容时,俯视液面使之与刻度线相切
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(4分)孔雀石和石青是自然界存在的两种碳酸盐类铜矿,它们的化学组成可表示为:
x CuCO3 ?y Cu(OH)2(x、y为正整数且x≤2,y≤2)。
(1)孔雀石和石青分别与过量盐酸反应时,孔雀石耗用的盐酸的物质的量与生成的CO2的物质的量之比为4︰1;石青则为3︰1。请推算它们的化学组成(化学式)。
孔雀石: ;石青: 。
(2)现有孔雀石和石青混合样品,取两份等质量的样品,在一份中加入过量盐酸,生成CO2 4.48L(标准状况下);加热另一份样品使其完全分解,得到CuO28g,试通过计算确定该混合物中孔雀石和石青的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下列物质中:
(1)互为同分异构体的有 ;
(2)互为同素异形体的有 ;
(3)属于同位素的有 ;
(4)属于同一种物质的有 。(填序号)
①液氯;②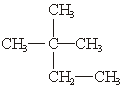 ;③白磷;④氯气;⑤
;③白磷;④氯气;⑤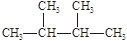 ;⑥
;⑥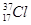 ;⑦
;⑦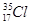 ;⑧红磷
;⑧红磷
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Ⅰ.按要求填空(每空1分)
①KOH的电子式: ②NH4Cl的电子式:
③CO2的结构式: ④HClO的结构式:
Ⅱ.按要求填空(每空2分)
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa(25℃时)时,已知0.5mol液态肼与足量氧气反应,生成氮气和水蒸气,放出312 KJ的热量。N2H4完全燃烧反应的热化学方程式是 ;又已知H2O(l)==H2O(g);△H = +44kJ?mol-1,由64g液态肼与氧气反应生成液态水时放出的热量是 kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
盐泥是氯碱工业中的废渣,主要成分是镁的硅酸盐和碳酸盐(含少量铁、铝、钙的盐)。实验室以盐泥为原料制取MgSO4·7H2O的实验过程如下:
①水,调成泥浆②稀硫酸调pH为1~2③煮沸④过滤―→―→产品
已知:①室温下Ksp[Mg(OH)2]=6.0×10-12。②在溶液中,Fe2+、Fe3+、Al3+从开始沉淀到沉淀完全的pH范围依次为7.1~9.6、2.0~3.7、3.1~4.7。③三种化合物的溶解度(S)随温度变化的曲线如图所示。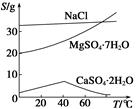
(1)在盐泥中加入稀硫酸调pH为1~2以及煮沸的目的是_____________________。
(2)若室温下的溶液中Mg2+的浓度为6.0 mol·L-1,则溶液pH≥________才可能产生Mg(OH)2沉淀。
(3)由滤液Ⅰ到滤液Ⅱ需先加入NaClO调溶液pH约为5,再趁热过滤,则趁热过滤的目的是__________________,滤渣的主要成分是______________________。
(4)从滤液Ⅱ中获得MgSO4·7H2O晶体的实验步骤依次为①向滤液Ⅱ中加入______________;②过滤,得沉淀;③________________;④蒸发浓缩,降温结晶;⑤过滤、洗涤得产品。
(5)若获得的MgSO4·7H2O的质量为24.6 g,则该盐泥中镁[以Mg(OH)2计]的百分含量约为________(MgSO4·7H2O的相对分子质量为246)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com