
(4分)孔雀石和石青是自然界存在的两种碳酸盐类铜矿,它们的化学组成可表示为:
x CuCO3 ?y Cu(OH)2(x、y为正整数且x≤2,y≤2)。
(1)孔雀石和石青分别与过量盐酸反应时,孔雀石耗用的盐酸的物质的量与生成的CO2的物质的量之比为4︰1;石青则为3︰1。请推算它们的化学组成(化学式)。
孔雀石: ;石青: 。
(2)现有孔雀石和石青混合样品,取两份等质量的样品,在一份中加入过量盐酸,生成CO2 4.48L(标准状况下);加热另一份样品使其完全分解,得到CuO28g,试通过计算确定该混合物中孔雀石和石青的物质的量之比为 。
科目:高中化学 来源: 题型:单选题
镁铝合金6.3 g完全溶于稀硝酸,若反应中硝酸被还原只产生4.48L(标准状况下)NO气体,在反应后的溶液中,加入足量Imol.L-I的NaOH溶液,生成沉淀的质量为
| A.8.7 g | B.7.8 g | C.16.5 g | D.4.0g |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| B.0.5molC3H8分子中所含C-H共价键数为2NA |
| C.标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA |
| D.1mol碳正离子CH5+所含的电子数为11NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
标准状况下有①6.72L甲烷②3.01×1023个氯化氢分子③13.6gH2S气体④0.2mol氨
气。下列对这四种气体的关系从小到大顺序排列(用序号表示)
| A.体积______________________________ | B.密度__________________________ |
| C.质量______________________________ | D.氢原子数______________________ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)按要求回答问题:
Ⅰ(1)硫酸酸化的高锰酸钾溶液与草酸反应离子方程式
(2)硫代硫酸钠与硫酸反应的化学方程式
Ⅱ工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2和CO的燃烧热(△H)分别为?890.3kJ?mol?1、?285. 8 kJ?mol?1和?283.0 kJ?mol?1,则生成1m3(标准状况)CO所需热量为
kJ
Ⅲ 请写出下列物质电子式
CO2 H2O2 NH4Cl N2H4
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
临湘一中食堂以前烧煤,经过改造现在烧天然气,使校园环境有了很大的改善。天然气的主要成分是甲烷,若2克甲烷完全燃烧可放出QKJ的热量,请写出能表示甲烷燃烧热的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(15分)(2012?重庆)氯离子插层镁铝水滑石[Mg2Al(OH)6Cl?xH2O]是一种新型离子交换材料,其在高温下完全分解为MgO、Al2O3、HCl和水蒸气.现用如图装置进行实验确定其化学式(固定装置略去).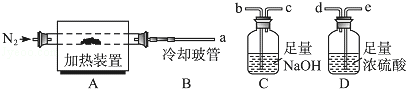
(1)Mg2Al(OH)6Cl?xH2O热分解的化学方程式为 .
(2)若只通过测定装置C、D的增重来确定x,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 .装置连接后,首先要进行的操作的名称是 .
(3)加热前先通N2排尽装置中的空气,称取C、D的初始质量后,再持续通入N2的作用是 、 等.
(4)完全分解后测得C增重3.65g、D增重9.90g,则x= .若取消冷却玻管B后进行实验,测定的x值将 (填“偏高”或“偏低”).
(5)上述水滑石在空气中放置时易发生反应生成[Mg2Al(OH)6Cl1﹣2x(CO3)y?zH2O],该生成物能发生类似的热分解反应.现以此物质为样品,用(2)中连接的装置和试剂进行实验测定z,除测定D的增重外,至少还需测定 .
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比三价铬毒性高,更易被人体吸收且在体内蓄积。
⑴工业上处理酸性含Cr2O72-废水的方法如下:
①向含Cr2O72-的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式: 。
②调节溶液的pH,使Cr3+完全沉淀。实验室粗略测定溶液pH的方法为 ;25℃,若调节溶液的pH=8,则溶液中残余Cr3+的物质的量浓度为 mol/L。(已知25℃时,Ksp[Cr(OH)3]=6.3×10-31)
⑵铬元素总浓度的测定:准确移取25.00mL含Cr2O72-和Cr3+的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成Cr2O72-,煮沸除去过量的(NH4)2S2O8;向上述溶液中加入过量的KI溶液,充分反应后,以淀粉为指示剂,向其中滴加0.015mol/L的Na2S2O3标准溶液,终点时消耗Na2S2O3溶液20.00mL。
计算废水中铬元素总浓度(单位:mg·L-1,写出计算过程)。
已知测定过程中发生的反应如下:
①2Cr3++3S2O82-+7H2O =Cr2O72-+6SO42-+14H+
②Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O
③I2+2S2O32-=2I-+S4O62-
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
把一只表面被氧化成10.2 g氧化铝的铝条A,放入1 L 1.5 mol/L的热氢氧化钠溶液中,过一段时间后取出铝条,溶液质量增加12.6克,此溶液称为甲溶液,体积仍为1 L,再把另一只表面也氧化成一定量的氧化铝的铝条B,放入1 L 0.9 mol/L的硫酸溶液中,,过一段时间取出,其质量减少25.8克,溶液质量增加25.2克,此溶液称为乙溶液,体积仍为1 L,回答下列问题:
(1)甲溶液溶质是 (写化学式),其物质的量是 ;
(2)乙溶液的溶质 (写化学式),其物质的量是 ;
(3)将甲乙两溶液反应,若使滴加的量最小,产生沉淀最多,应将 溶液 (填甲、乙)L 滴加到 溶液中(填甲、乙)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com