
【题目】溶液、胶体和浊液这三种分散系的根本区别是( )
A. 分散质粒子直径的大小B. 光束穿过胶体时形成一条光亮的通路
C. 能否透过滤纸或半透膜D. 是否均一、透明、稳定
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大.X、W同主族,Y、Z为同周期的相邻元素.W原子的质子数等于Y、Z原子最外层电子数之和.Y的氢化物分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍.试推断:
(1)X、Y、Z、W四种元素的符号:X___、Y__、Z___、W_____
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为_____,_____.
(3)由X、Y、Z所形成的离子化合物是_____,它与W的最高氧化物的水化物的浓溶液加热时反应的离子方程式是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钠是一种活泼金属,除了具有金属的一般性质外,还具有自己的特性。关于钠的叙述中,正确的是
A.钠是银白色金属,熔点低,硬度大
B.钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠
C.加热时,金属钠剧烈燃烧,产生黄色火焰
D.金属钠着火可以用泡沫灭火器或用干燥的沙土灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F的原子序数依次增大,它们都具有相同的核外电子层数。已知:A、C、F三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素的符号:A________,B________,E________。
(2)把B的单质(片状)放入滴有酚酞的沸水中,观察到的现象是_________________,反应的化学方程式是_______________________。
(3)A、C两种元素的最高价氧化物的水化物反应的离子方程式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如右图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是 ( )
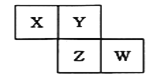
A. Z、X分别与Y形成的化合物均能与NaOH溶液发应生成盐和水
B. 最高价氧化物对应水化物的酸性: Z>W>X
C. 4种元素的单质中,Z单质的熔、沸点最高且易溶于水
D. W单质能与水反应,生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在1400~1450℃的氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g)高 ![]() Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡. 完成下列填空:
Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡. 完成下列填空:
(1)上述反应所涉及的元素,原子半径由大到小的顺序是 . 其中一种元素的原子核外s电子数与p电子数相等,写出它的最外层电子排布的轨道表示式 .
比较碳、硅两种元素的非金属性强弱,可以通过比较(填:化合物性质的差异)来判断.
(2)上述反应混合物中的极性分子是 , 写出非极性分子的电子式 . 从晶体类型的角度分析用氮化硅制造发动机中耐热部件的原因是
(3)下列措施可以提高二氧化硅转化率的是(选填编号).a.增加二氧化硅用量b.升高反应温度
c.增大气体压强 d.向反应容器中多充入氮气
(4)下列描述中能说明反应已达平衡的是(选填编号).a.c(CO)=3c(N2) b.v (CO)=3v(N2)
c. ![]() 保持不变d.气体的压强保持不变
保持不变d.气体的压强保持不变
(5)测得平衡时固体质量减少了11.2g,则用氮气表示的平均反应速率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列有关叙述正确的是
A.大气雾霾污染现象的产生与汽车尾气排放有关
B.玻璃和氮化硅陶瓷都属于新型无机非金属材料
C.空气中的臭氧对人体健康有益无害
D.活性炭与二氧化硫都可用于漂白,其漂白原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于组成细胞的微量元素一组是( )
A.C H N P MgB.Cl Fe S N Mg
C.B Cu Zn Mn MoD.N P K Cu Fe I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期的非金属元素(其单质也可分别用A、B、C、D表示),四种元素的原子序数按B、D、C、A顺序增大,D、C元素在周期表中位置相邻。在一定条件下,B可以分别和A、C、D化合生成甲、乙、丙化合物,C和D化合可得丁。已知乙、丙两个分子中各含有10个电子,并且甲、乙、丙、丁、戊有如下的变化关系:

请回答下列问题:
(1)甲的浓溶液与一种黑色粉末共热可得A。实验室制备A的离子方程式为:__________________;
(2)B元素在周期表中的位置是______________,B在A中燃烧的现象是____________;
(3)写出下列反应的化学方程式:
①C +丙:_____________________________________________;
②丙+丁→D + 乙:___________________________________________;
③A +丙→D + 甲:_____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com