
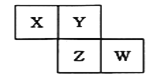
����Ŀ��X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ��е�λ������ͼ��ʾ����Yԭ�ӵ������������Ǵ�����������3��������˵������ȷ���� �� ��
A. Z��X�ֱ���Y�γɵĻ����������NaOH��Һ��Ӧ�����κ�ˮ
B. ����������Ӧˮ���������: Z>W>X
C. 4��Ԫ�صĵ����У�Z���ʵ��ۡ��е������������ˮ
D. W��������ˮ��Ӧ������һ�־���Ư���Ե�����
���𰸡�D
��������Yԭ�ӵ��������������ڲ��������3����������������Ϊ2��6��ӦΪOԪ�أ���������Ԫ�������ڱ��е�λ�ÿ�֪��XΪNԪ�أ�ZΪSԪ�أ�WΪClԪ�أ�A��Z��Y�γɵĻ�������������������������NaOH��Һ��Ӧ�����κ�ˮ������������������Щ�������������Ʒ�Ӧ����NO��ѡ��A����B��ͬ����Ԫ�ش�����Ԫ�صķǽ���������ǿ������Ԫ�صķǽ�����Խǿ����Ӧ����������ˮ���������Խǿ��֪����������Ӧˮ��������ԣ�W>Z��ѡ��B����C������Ԫ�صĵ����У�������Z�ĵ����ǹ��壬����������壬Z��������ۡ��е���ߣ�����������ˮ��ѡ��C����D��������ˮ��Ӧ��������ʹ����ᣬ���������Ư���ԣ���D��ȷ����ѡD��


 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д� Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�NaClO��NaCl�����Һ��������ȷ���ǣ� ��
A.����Һ�У�H+��NH ![]() ��SO
��SO ![]() ��Br�����Դ�������
��Br�����Դ�������
B.����Һ�У�K+��OH����S2����NO3�����ܴ�������
C.�����Һ�е�������FeSO4��Һ�����ӷ���ʽΪ��2Fe2++ClO��+2H+��Cl��+2Fe3++H2O
D.�����Һ�м���Ũ���ᣬÿ����1molCl2 �� ת�Ƶ���ԼΪ6.02��1023��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£��������͵�������1mol����̬��������10L���ܱ������У�������ӦH2��g��+I2��g��=2HI��g����2���Ӻ�ﵽƽ����C��H2��=0.08molL��1 ��
��1����÷�Ӧ��ƽ�ⳣ����
��2����2�����ڵ�H2�ķ�Ӧ���ʣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С��ͬѧΪ��̽��ͭ��Ũ����ķ�Ӧ������������ϵ��ʵ�顣
��ʵ��1��ͭ��Ũ���ᷴӦ��ʵ��װ����ͼ��ʾ��

ʵ�鲽�裺
�������Ӻ�װ�ã����������ԣ������Լ���
�ڼ���A�Թ�ֱ��B��Ʒ����ɫ��Ϩ��ƾ��ƣ�
�۽�Cu˿�����뿪Һ�档
��1��װ�� A �з�����Ӧ�Ļ�ѧ����ʽΪ__________��ʵ���з����� A ������˰�ɫ���壬�����Ϊ________��C��NaOH��Һ������Ϊ______
��2��Ϩ��ƾ��ƺ���Ϊ�е���D�Ĵ��ڣ�B�е�Һ�岻�ᵹ������ԭ����______��
��3��ֹͣ���Ⱥ��ڲ��װ��ǰ������������Ϳ�ʹװ���в���������ȫ�����գ�Ӧ����ȡ�IJ�����__________________��
��ʵ��2��ʵ���з����Թ�A�ڳ��˲�����ɫ�����⣬��ͭ˿���滹������ɫ����ף����п��ܺ�������ͭ����ͭ������ͭ���Լ����ڱε�������ͭ��
�������ϣ�
��������ͭ�����Ի����»ᷢ������������ԭ��Ӧ����Cu2+��ͭ���ʣ��������������գ�����ת��Ϊ����ͭ��
����ͭ������ͭ�����¶�������ϡ���ᣬ�������������գ���ͭ������ͭ��ת��Ϊ����ͭ�Ͷ�������
Ϊ���о��ijɷ֣���С��ͬѧ���ռ����㹻���Ĺ����������ͼ��ʾ��ʵ��
��4�����м��������Ƿ�ϴ�Ӹɾ���ʵ�������___________��
��5�����������չ�����һ�������ķ�Ӧ�Ļ�ѧ����ʽΪ_____________________��
��6�����ж��ڹ���ijɷֵ��ж��У���ȷ���ǣ�����ĸѡ�____________��
A��������У�CuS��Cu2S����ͬʱ����
B��������У�CuO��Cu2O������һ��
C�����������û��Cu2O����һ����Cu2S
D���������������Cu2O��Ҳ������Cu2S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ������ʵ���������ȷ����
A������������Ӧʱ����������O2������������
B�������ڿ��������ȿ����ۻ��һᷢ������ȼ��
C��������ǽ���������Ӧʱ����������һ���ǽ���
D����˿�����ڿ����л����ڴ����ж�����ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Һ���������Һ�����ַ�ɢϵ�ĸ���������( )
A. ��ɢ������ֱ���Ĵ�СB. ������������ʱ�γ�һ��������ͨ·
C. �ܷ�����ֽ���ĤD. �Ƿ��һ�������ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ӷ�Ӧ����H����OH��= H2O��ʾ����(����)
A. ��������������B. ��������������C. �����������ͭD. �������ƺ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ������������:
(1)11H��21H��31H��Ϊ________O2��O3��Ϊ_________
(2)�����й�����: a.CaCl2 b.KOHc.Hed.H2SO4e.NH4Clf.���ʯ
�����в�����ѧ����������________
�ڼȺ������Ӽ��ֺ��й��ۼ���������____________(�����)
(3)��ͼ�Ǽ��ֳ����ĵ��װ�á���ش�:

�ٵ�آ��и�����Ӧʽ��_____,��Һ��H+��_____(�����������)���ƶ�����1mol�����������ߣ���������������ʵ�����______mol��
�ڵ�آ�����________���(�һ�Ρ����Ρ�).
�۵�آ�������ȼ�ϵ�أ�д�������ĵ缫��Ӧʽ��________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г���ʵ�������У�����ֱ�����ڻ����ķ�����ᴿ����(����)
A. ��Һ©��B. ©��C. ������ƿD. ����ƿ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com