
【题目】《科学美国人》评出的2016年十大创新技术之一是碳呼吸电池,电池原理如图所示,则下列有关说法正确的是
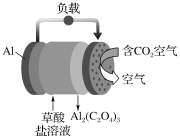
A.以此电池为电源电解精炼铜,当有0.1 mol 电子转移时,有3.2 g铜溶解
B.正极每消耗4.48L的CO2,则生成0.1molC2O42-
C.每生成1 mol Al2(C2O4)3,有6 mol电子流过草酸盐溶液
D.随着反应进行,草酸盐浓度不变
科目:高中化学 来源: 题型:
【题目】美国科学家用某有机分子和球形笼状分子C60制成了“纳米车”(如图所示),每辆“纳米车”是由一个有机分子和4个C60分子构成。“纳米车”可以用来运输单个的有机分子。下列说法正确的是

A. 人们用肉眼可以清晰看到“纳米车”的运动
B. “纳米车”诞生说明人类操纵分子的技术进入了一个新阶段
C. C60是一种新型的化合物
D. C60与12C是同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种新型高分子材料的结构简式为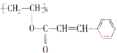 ,对此高聚物叙述不正确的是( )
,对此高聚物叙述不正确的是( )
A.化学式为(C11H10O2)n
B.可以发生水解反应、氧化反应,也能发生卤代反应
C.1 mol 该有机物分子最多能和4 mol H2发生加成反应
D.该高分子材料是经加聚反应而得到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究。
(1)①把含有较高浓度CO2的空气通入饱和K2CO3溶液。②在①的吸收液中通高温水蒸气得到高浓度的CO2气体。请写出②中反应的化学方程式______。
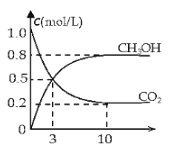
(2)如将CO2与H2以1:3的体积比混合,在适当条件下合成燃料甲醇和水。在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=-49.0kJ/mol。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
从反应开始到平衡,v(H2)=______;氢气的转化率=______;能使平衡体系中n(CH3OH)增大的措施有______。(只写一种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中.△H能正确表示物质的燃烧热的是( )
A.CO(g) +![]() O2(g) ==CO2(g); △H=-283.0 kJ/mol
O2(g) ==CO2(g); △H=-283.0 kJ/mol
B.C(s) +![]() O2 ==CO(g); △H=-110.5 kJ/mol
O2 ==CO(g); △H=-110.5 kJ/mol
C.H2(g) +![]() O2(g)==H2O(g); △H=-241.8 kJ/mol
O2(g)==H2O(g); △H=-241.8 kJ/mol
D.2C8H18(l) +25O2(g)==16 CO2(g)+18 H2O(l); △H=-1136 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为2种无毒气体。T℃时,将0.8 mol NO和0.8 mol CO充入容积为2 L的密闭容器中,模拟尾气转化,容器中NO物质的量随时间变化如图。
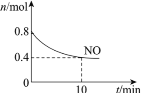
(1)将NO、CO转化为2种无毒气体的化学方程式是__________________。
(2)反应开始至10 min,v(NO)=______mol/(Lmin),NO的转化率为________,此温度下达到平衡常数为________________。
(3)下列说法正确的是______。
a.新型催化剂可以加快NO、CO的转化
b该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/ L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质分类的说法中正确的是( )
A.现有![]() 、
、![]() 、
、![]() 、
、![]() ,可以按某个标准判断
,可以按某个标准判断![]() 与其他三种不同;也可按某个标准判断
与其他三种不同;也可按某个标准判断![]() 与其他三种不同
与其他三种不同
B.在物质分类时,一般是先分类,再定标准,这样就不会有误了
C.树状分类法是唯一能表示物质分类的方法
D.胶体、溶液、浊液分属不同类别的本质是其透过滤纸的性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴镍渣是湿法炼锌净化渣之一,其中含有较多的Zn(II)、Cd(II)和少量Co(II)、Fe(II)、Ni(II)的硫酸盐及氢氧化物。利用以下工艺流程回收金属并制备氧化锌:
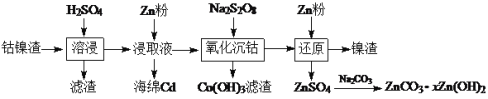
回答下列问题:
(1)“溶浸”时H2SO4的作用是_____________。
(2)向“浸取液”中加入Zn粉后发生反应的离子方程式为__________________。
(3)Na2S2O8中S的化合价为+6,其中过氧键的数目为________。
(4)研究加入Na2S2O8后温度和时间对金属脱除率的影响,所得曲线如下图所示。
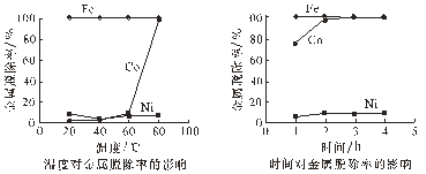
金属脱除是指溶液中的二价金属离子被氧化后形成氢氧化物沉淀而除去。由图可知,Co2+与Ni2+的还原性强弱关系是_________,“氧化沉钴”适宜的条件是________。
(5)在适宜的条件下,加入Na2S2O8并调节溶液pH至5.0~5.2,反应生成Co(OH)3的离子方程式为_______,Co(OH)3滤渣中还含有________。
(6)氧化锌是一种重要而且使用广泛的物理防晒剂,屏蔽紫外线的原理为吸收和散射。由ZnCO3·xZn(OH)2制备氧化锌的方法是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列实验探究亚硝酸钠(NaNO2)的化学性质(AgNO2是淡黄色难溶于水的固体)
实验 | 装置 | 试剂a | 现象 |
① |
| 酚酞 | 无色溶液变红 |
② | AgNO3溶液 | 产生淡黄色沉淀 | |
③ | 淀粉KI 溶液+稀硫酸 | 无色溶液立即变蓝 | |
④ | 酸性K2Cr2O7溶液 | 无色溶液变为绿色 |
由上述实验所得结论不正确的是
A.NaNO2溶液呈碱性:NO2-+H2OHNO2+OH-
B.NaNO2可与某些盐发生复分解反应:NO2-+Ag+=AgNO2↓
C.NaNO2有氧化性:2I-+2H++2NO2-=I2+2NO2↑+H2O
D.NaNO2有还原性:Cr2O72-+3NO2-+8H+=3NO3-+2Cr3++4H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com