
����Ŀ��������ѧ֪ʶ�����Ŀ��
��1���й��Ŵ��Ĵ���֮һ�����ڻ�ҩ�����ı�ը��ӦΪ��2KNO3+3C+S ![]() A+N2��+3CO2��������ƽ�� �ٳ�S�⣬����Ԫ�صĵ縺�ԴӴ�С����Ϊ��
A+N2��+3CO2��������ƽ�� �ٳ�S�⣬����Ԫ�صĵ縺�ԴӴ�С����Ϊ��
�����������У������Թ��ۼ��ķ��ӵ�����ԭ�ӹ���ӻ�����Ϊ �� A�ľ�������Ϊ ��
����֪CN����N2�ṹ���ƣ�����HCN�����ЦҼ���м���Ŀ֮��Ϊ ��
��2��ԭ������С��36��Ԫ��Q��T�������ڱ��мȴ���ͬһ������λ��ͬһ�壬��ԭ������T��Q��2��T�Ļ�̬ԭ����Χ���ӣ��۵��ӣ��Ų�Ϊ �� Q2+��δ�ɶԵ������� ��
��3����CrCl3��ˮ��Һ�У�һ�������´������Ϊ[CrCln��H2O��6��n]x+��n��x��Ϊ���������������ӣ�����ͨ�������ӽ�����֬��R��H�����ɷ������ӽ�����Ӧ��[CrCln��H2O��6��n]x++xR��H��Rx[CrCln��H2O��6��n]+xH+����������H+���к͵ζ����������x��n��ȷ�������ӵ���ɣ�����0.0015mol[CrCln��H2O��6��n]x+����Һ����R��H��ȫ�������к����ɵ�H+��Ũ��Ϊ0.1200molL��1NaOH��Һ25.00mL����֪�������ӵĻ�ѧʽΪ ��
���𰸡�
��1��O��N��C��K��sp�����Ӿ��壻1��1
��2��3d84s2��1��1
��3��[CrCl��H2O��5]2+
���������⣺��1����ͬ����������ҵ縺����������Խǿ�縺��ԽС���ʵ縺��O��N��C��K�����Դ��ǣ�O��N��C��K���ں����Թ��ۼ��ķ���ΪCO2 �� ������Cԭ���γ�2��C=O���������¶Ե��ӣ��ӻ������ĿΪ2��Ϊsp�ӻ���ʽ����ԭ���غ��֪������AΪK2S���������Ӿ��壬���Դ��ǣ�sp�����Ӿ��壻��CN����N2�ṹ���ƣ�Cԭ����Nԭ��֮���γ���������HCN���ӽṹʽΪH��C��N�������к���1���Ҽ���2���м����������ڦҼ�����HCN�����ЦҼ���м���Ŀ֮��Ϊ1��1�����Դ��ǣ�1��1����2��ԭ������С��36��Ԫ��Q��T�������ڱ��мȴ���ͬһ������λ��ͬһ�壬��Q��T���ڵڢ��壬��ԭ������T��Q��2����QΪFeԪ�أ�TΪNiԪ�أ�NiԪ����28��Ԫ�أ�Niԭ�Ӽ۵����Ų�ʽΪ3d84s2 �� Fe2+�ĺ�������Ų�ʽΪ1s24s22p63s23d6 �� 3d�ܼ���4�������ӣ����Դ��ǣ�3d84s2��4����3���к����ɵ�H+��Ũ��Ϊ0.1200mol/L����������Һ25.00mL������Եó�H+�����ʵ���Ϊ0.12mol/L��25.00��10��3L=0.0030mol������x= ![]() =2��Cr�Ļ��ϼ�Ϊ+3�ۣ����[CrCln��H20��6��n]x+ �� ��3��n=2�����Ե�֪n=1�����������ӵĻ�ѧʽΪ[CrCl��H2O��5]2+ �� ���Դ��ǣ�[CrCl��H2O��5]2+ ��
=2��Cr�Ļ��ϼ�Ϊ+3�ۣ����[CrCln��H20��6��n]x+ �� ��3��n=2�����Ե�֪n=1�����������ӵĻ�ѧʽΪ[CrCl��H2O��5]2+ �� ���Դ��ǣ�[CrCl��H2O��5]2+ ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪC��H��0��N��P��Ԫ�ع��ɻ�����ס��ҡ������ṹ����ʾ��ͼ������˵���������
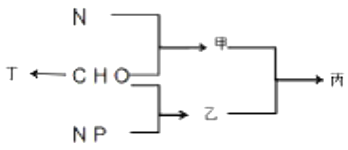
A. �������ڽṹ���ϳ��������У���ĵ�����˫�����Լ�������ɫ
B. ���������ϸ�������õĴ������ʣ�����ϳɳ���Ϊһ�־�Ĥ��ϸ����
C. ������ԭ��ϸ���ڵ����ʺϳɳ��������ҳ���ˮ�������6��
D. ������һ������Ĥ�����书����Ĥ�ϼ�����������й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�ص�����aA2+��bB+��cC3-��dD-��������ͬ�ĵ��Ӳ�ṹ������������ȷ����
A. ���ʵĻ�ԭ��:A>B>D>C B. ���Ӱ뾶:C>D>B>A
C. c-a=5 D. ԭ�Ӱ뾶:A>B>D>C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˻�������ЧӦ����ѧ������˶��ֻ��պ�����CO2�ķ�����
����I:����FeO����CO2���H2
i.6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ��Hl=-76.0kJ/mol
��.C(s)+2H2O(g)==CO2(g)+2H2(g) ��H2=+113.4kJ/mol (1)3FeO(s)+H2O(g)=Fe3O4(s)+H2(g) ��H3=__________��
(2)�ڷ�Ӧi�У�ÿ�ų�38.0kJ��������______gFeO��������
����II:����CO2�Ʊ�CH4
300��ʱ����2L�����ܱ������г���2mol CO2��8molH2��������ӦCO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) ��H4�����������CH4��Ũ���뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ��
CH4(g)+2H2O(g) ��H4�����������CH4��Ũ���뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ��

(3) �ٴӷ�Ӧ��ʼ��ǡ�ôﵽƽ��ʱ��H2��ƽ����Ӧ����v(H2)=________��
��300��ʱ����Ӧ��ƽ�ⳣ��K=________��
�۱����¶Ȳ��䣬��ƽ�����������ٳ���2molCO2��8molH2�����´ﵽƽ��ʱCH4��Ũ��_______(����ĸ)��
A.����0.8mol/L B.����1.6mol/L
C.0.8 mol/L <c(CH4)<1.6 mol/L D.����1.6 mol/L
(4)300��ʱ���������������1.6molCO2��2.0molH2��5.6molCH4��4.0molH2O(g)����v��____v��(����>����<������=��)��
(5)��֪��200��ʱ.�÷�Ӧ��ƽ�ⳣ��K=61.8L2��mol-2������H4___0������>����<������=��)��
������:�ü���Һ����CO2
����100mL3mol/LNaOH��Һ����4.48LCO2(��״��)���õ�����Һ��
(6)������Һ������Ũ�ȵĴ�С����Ϊ____________����������Һ���ɣ����������أ����ù���ijɷ���_______(�ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ����ͼ�õ�ⷨ���ݵ缫���������ʵ���������֤�����ӵ�����ֵ����ʵ�鷽����Ҫ��Ϊ������ֱ�������Ȼ�ͭ��Һ������������ͼ��
���ڵ���ǿ��ΪI A��ͨ��ʱ��Ϊt s��ȷ�����缫��������ͭ������Ϊm g��
�Իش�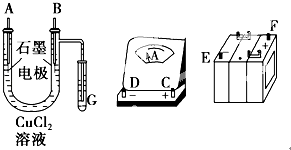
��1��������Щ��������ȷ˳��Ϊ����ͼ�б�ע������������Ӣ����ĸ��ʾ����ͬ����E��D��C�� �� ��F��
��2��д��B���Ϸ�����Ӧ�ĵ缫��Ӧʽ�� �� G�Թ��е���KI��Һ�仯������Ϊ �� ��Ӧ�����ӷ���ʽ�� ��
��3��Ϊ��ȷ�ⶨ�缫������ͭ���������������ʵ�鲽����Ⱥ�˳��Ӧ�� �� �ٳ������ǰ�缫����
�ڹ��µ���缫�ϵ�ͭ����ϴ
��������ˮ��ϴ����缫
�ܵ��º�ɵ缫�����
�ݵ��º�ɹ��µ�ͭ�������
���ٴε��º�ɺ����������
��4����֪���ӵĵ���Ϊ1.6��10��19C�����г������ӵ������ļ������ʽ��NA= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��������ʵ�����������ȷ���ǣ� ��
A.��ͼ�ļ���ʽ��ʾ��������Ϊ��3������4���һ���7�������� 
B.���Ϸ���ʽΪC3H8O�Ĵ������ֲ�ͬ�Ľṹ
C.![]() �У�����ԭ�Ӳ����ܶ���ͬһƽ����
�У�����ԭ�Ӳ����ܶ���ͬһƽ����
D.����ű���������أ���ͼ��  ������ʽ��C15H20O5
������ʽ��C15H20O5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�Na2CO3��Һ�д���ˮ��ƽ�⣺CO32��+H2OHCO3��+OH�� �� ����˵������ȷ���ǣ� ��
A.ͨ��CO2 �� ��ҺpH��С
B.��������NH4Cl���壬ƽ��������Ӧ�����ƶ�
C.���������¶ȣ� ![]() ��С
��С
D.����NaOH �������ȴ�����£���Һ��KW=c��OH����?c��H+������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڳ����£���һ��ʢ��һ����������������ܱղ����������ڹ����ĵط����������巢����Ӧ������������ȷ����
��������ѹǿ���� �������ڷ����������� ��������ԭ���������� �������ڷ����ķ�Ӧ��ȡ����Ӧ��16 g����������Cl2�ڹ��������·�Ӧ���������ȼ���ķ�����ΪNA
A. �٢ڢ� B. �ڢ� C. �ۢܢ� D. �ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�Ũ�Ⱦ�Ϊ0.1mol/L��100mL��Ba��OH��2��Һ�У��ֱ����Ũ�Ⱦ�Ϊ0.1mol/L��H2SO4��NaHSO4��Һ���䵼�������������Һ����仯����������ͼ��ʾ��
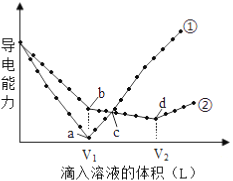
��1�� 0.1mol/L��NaHSO4��ҺpH=_____________��
��2������___________�����μ�H2SO4��Һ�ı仯���ߡ�b����Һ�������Ϊ___________�����Ի���Ի����ԣ���
��3��d����Һ����Ҫ�������ࣺ______________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com