
【题目】A~J是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去)。已知A是一种高熔点物质,D是一种红棕固体,H的焰色呈黄色。

请回答下列问题:
(1)A物质的化学式为________,H物质的名称为______________________。
(2)G![]() J的实验现象是_________________;化学方程式为___________________。
J的实验现象是_________________;化学方程式为___________________。
(3)D与C高温下反应的化学方程式为:________________。
(4)D物质与盐酸恰好反应的离子方程式为__________,所得溶液的颜色为_______________________。
【答案】Al2O3 偏铝酸钠 白色沉淀迅速变为灰绿色,最终变成红褐色沉淀 4Fe(OH)2+O2+2H2O═4Fe(OH)3 Fe2O3+2Al![]() 2Fe+ Al2O3 Fe2O3+6H+═2Fe3++3H2O 浅黄色
2Fe+ Al2O3 Fe2O3+6H+═2Fe3++3H2O 浅黄色
【解析】
D是一种红棕色固体,应为Fe2O3,可与C反应,生成物A既可与盐酸反应,又可与NaOH反应,由转化关系可知C为Al,A为Al2O3,E为Fe,B为O2,H为NaAlO2,I为AlCl3,F为FeCl2,G为Fe(OH)2,J为Fe(OH)3,结合物质的性质以及题目要求可解答该题.
(1)由上述分析可知A为Al2O3,H的名称为偏铝酸钠,
故答案为:Al2O3;偏铝酸钠;
(2)G→J的实验现象是白色沉淀迅速变为灰绿色,最终变成红褐色沉淀,化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:白色沉淀迅速变为灰绿色,最终变成红褐色沉淀;4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(3)D与C高温下反应的化学方程式为Fe2O3+2Al![]() 2Fe+ Al2O3,
2Fe+ Al2O3,
故答案为:Fe2O3+2Al![]() 2Fe+ Al2O3;
2Fe+ Al2O3;
(4)D物质与盐酸恰好反应的离子方程式为Fe2O3+6H+═2Fe3++3H2O,生成铁离子,溶液颜色为浅黄色,
故答案为:Fe2O3+6H+═2Fe3++3H2O;浅黄色。


科目:高中化学 来源: 题型:
【题目】六氟合铝酸钠(Na3AlF6)俗称冰晶石,微溶于水,可用作陶瓷乳白剂、树脂橡胶的耐磨填充剂等。实验室以萤石(CaF2,难溶于水)、石英和纯碱等为原料可制备Na3AlF6,实验步骤如下:
Ⅰ.将萤石(CaF2)、石英和纯碱按一定比例混合后煅烧并释放出CO2;
Ⅱ.……
Ⅲ.在浸取液中加入稀硫酸调节pH,再加入硫酸铝,充分反应后过滤,洗涤烘干后得到六氟合铝酸钠。
回答下列问题:
(1)Na3AlF6中铝元素的化合价为__________。
(2)步骤Ⅰ中煅烧原料混合物时,盛装原料混合物的仪器名称为___________;混合物煅烧后除生成CO2、CaSiO3外还有一种产物(二元化合物),该物质的化学式为______________。
(3)步骤Ⅱ的具体内容是__________________。
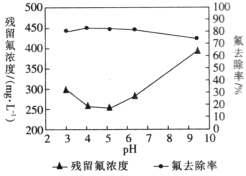
(4)通过实验探究不同pH时氟离子的去除率,即对多份相同量的浸取液调节至不同pH后,再分别加入等量硫酸铝,得到了溶液中残留氟浓度和氟去除率随溶液pH的变化关系如图所示。则步骤Ⅲ中最佳pH为_________;图中当pH增大时,氟去除率下降的原因是_______________________________________。
(5)步骤Ⅲ中检验过滤后的固体已洗涤干净的方法是_______________________________。
(6)写出一种能将含氟废水中氟离子去除的可行方法:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机知识正确的有_____个
①![]() 名称:2,3—二甲基—1,5—戊二烯 ②乙烯的实验式;CH2
名称:2,3—二甲基—1,5—戊二烯 ②乙烯的实验式;CH2
③用质谱仪和红外光谱均可以获得有机物所含化学键或官能团信息
④乙醇的分子式:C2H5OH ⑤苯乙炔共线的原子最多有6个
⑥对甲基苯甲醇的结构简式:![]()
A.2个B.3个C.4个D.5个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业炼铁过程中涉及到的主要反应有:
i.C(s)+O2(g)=CO2(g)△H1=-393kJ/mol
ii.C(s)+CO2(g)=2CO(g)△H2=+172kJ/mol
iii.Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)△H3
2Fe(s)+3CO2(g)△H3
iv.2Fe2O3(s)+3C(s)![]() 4Fe(s)+3CO2(g)△H4=+460kJ/mol
4Fe(s)+3CO2(g)△H4=+460kJ/mol
回答下列问题:
(1)反应iv_________(填“能”或“不能”)在任何温度下自发进行。
(2)△H3=_________kJ/mol。
(3)T1时,向容积为10L的恒容密闭容器中加入3molFe2O3和3molCO发生反应iii,5min时达到平衡,平衡时测得混合气体中CO2的体积分数为80%。
①0~5min内反应的平均速率v(CO2)=_________molL-lmin-l。
②该温度下反应的平衡常数为_________。
③若将平衡后的混合气体通入1L3.6mol/L的NaOH溶液,恰好完全反应,反应的离子方程式为_________,所得溶液中离子浓度由大到小的顺序是_________
④下列选项中能够说明该反应已经达到平衡状态的是_________(填序号)。
a.Fe2O3的物质的量不再变化
b.体系的压强保持不变
c.混合气体的平均摩尔质量保持不变
d.单位时间内消耗CO和生成CO2的物质的量相等
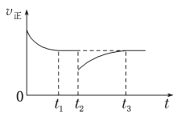
(4)一定条件下进行反应iii,正向反应速率与时间的关系如图所示,t2时刻改变了一个外界条件,可能是_________。
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A.向AgNO3中滴加氨水至过量:Ag++NH3H2O=AgOH↓+![]()
B.向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2=I2+2H2O
C.向Na2S2O3溶液中加入足量稀硫酸:2![]() +4H+=
+4H+=![]() +3S↓+2H2O
+3S↓+2H2O
D.向苯酚钠溶液中通入少量CO2气体:2![]() +CO2+H2O→2
+CO2+H2O→2![]() +
+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饮用水中含有砷会导致砷中毒,金属冶炼过程产生的含砷有毒废弃物需处理与检测。冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2-存在反应:As2S3(s)+3S2-(aq)2![]() (aq);
(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)砷在元素周期表中的位置为_______;AsH3的电子式为______;
(2)下列说法正确的是_________;
a.酸性:H2SO4>H3PO4>H3AsO4
b.原子半径:S>P>As
c.第一电离能:S<P<As
(3)沉淀X为__________(填化学式);
(4)“一级沉砷”中FeSO4的作用是________。
(5)“二级沉砷”中H2O2与含砷物质反应的化学方程式为__________;
(6)关于地下水中砷的来源有多种假设,其中一种认为富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成![]() ,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为______________。
,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的电子气体有BCl3、N2O、SiH4及SiHCl3等。回答下列问题:
(1)气体B2H6与氯气混合可生成气态BCl3,每生成1.0 g BCl3放出5.9 kJ的热量,该反应的热化学方程式为______。
(2)25℃时反应 S(s) +H2(g)H2S(g) Kp1=6.0×105
Si(s)+2H2(g)SiH4(g) Kp2=7.8×106
则反应 Si(s)+2H2S(g)SiH4(g)+2S(s) Kp=_____(Kp为以分压表示的平衡常数,下同)。
(3)多晶硅制中发生一系列反应:
(I)4SiHCl3(g)Si(s)+3SiCl4(g)+2H2(g) △H1=a kJ /mol
(II)SiCl4(g)+H2(g)SiHCl3(g)+HCl(g) △H2=b kJ/mo1
(III)SiCl2(g)+H2(g)Si(s)+2HCl(g) △H3=c kJ/mo1
①反应SiHCl3 (g)SiCl2 (g) +HCl (g) △H=____kJ/mo1 (用含a、b、c的代数式表示)
②反应(I)(II)(III)的Kp与温度的关系如下图

属于吸热反应的是_________(填I、II或III);图中M点分压间满足关系:p(SiCl4)=______(用相关物质的分压p表示)。
(4)一种制取N2O的方法为 O2NNH2(aq)→N2O(g)+H2O(1),该反应的历程如下:
(I)O2NNH2(aq)![]() O2NNH-(aq) +H+(aq) (快速平衡)
O2NNH-(aq) +H+(aq) (快速平衡)
(II)O2NNH-(aq)![]() N2O(g) +OH-(aq) (慢)
N2O(g) +OH-(aq) (慢)
(III)H+(aq)+OH-(aq)![]() H2O(1) (快)
H2O(1) (快)
①活化能最大的反应步骤是_________(填I、II或III)。
②已知反应(I)的速率方程v(正)=k1c(O2NNH2),v(逆)=k -1 c(O2NNH-)c(H+),(k1、k -1分别为正逆反应速率常数,反应(I)达到平衡时,平衡常数K=__________(用k1、k -1表示)。
③已知总反应速率方程为v=K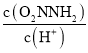 ,反应(II)的v(正)=k2c(O2NNH-),则K=________ (用k1、k -1、k2、k3表示)
,反应(II)的v(正)=k2c(O2NNH-),则K=________ (用k1、k -1、k2、k3表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种如图所示的三室微生物燃料电池用来处理废水(废水中高浓度有机物用C6H12O6表示),下列叙述不正确的是

A.a电极反应式为:C6H12O6+6H2O-24e-=6CO2↑+24H+
B.b电极附近的溶液pH增大
C.温度越高,处理废水的效率越高
D.若反应中转移的电子数为NA,则生成标准状况下N2的体积为2.24L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com