
【题目】某兴趣小组制备氢氧化亚铁沉淀.
实验1 |
| 实验现象 |
液面上方产生白色絮状沉淀,迅速变为灰绿色,振荡,试管壁上有红褐色沉淀生成. |
(1)实验1中产生白色沉淀的离子方程式是 .
(2)为了探究沉淀变灰绿色的原因,该小组同学展开如下探究: ①甲同学推测灰绿色物质为Fe(OH)2和Fe(OH)3混合物.查阅资料后根据调色原理认为白色和红褐色的调和色不可能是灰绿色,并设计实验证实灰绿色物质中不含有Fe(OH)3 , 方案是 .
②乙同学查阅文献:Fe(OH)2在大量SO42﹣存在的情况下形成Fe6(SO4)2(OH)4O3(一种氧基碱式复盐).并设计对比实验证实该假设:向试管中加入 , 再往试管中加入 , 振荡,现象与实验1相同,结论是该假设不成立.
③乙同学继续查阅文献:Fe(OH)2沉淀具有较强的吸附性能,灰绿色可能是由Fe(OH)2表面吸附Fe2+引起.推测所用的硫酸亚铁溶液的浓度应越小越好;氢氧化钠溶液浓度应越大越好.设计了如下实验方案:
试管中10mL | 滴加 | 实验现象 | |
实验2 | 6mol/L | 0.2mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有少量灰绿色),沉淀下沉后,大部分灰绿色变为白色沉淀 |
实验3 | 6mol/L | 0.1mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有极少量灰绿色),沉淀下沉后,底部都为白色沉淀 |
该实验得出的结论是 , 能说明灰绿色是由Fe(OH)2表面吸附Fe2+引起的证据是 . 丙同学认为该实验方案不足以证明灰绿色是由Fe(OH)2表面吸附Fe2+引起的,还需补充的实验是 , 证明该假设成立.
(3)丙同学探究温度对氢氧化亚铁制备实验的影响:取少量灰绿色沉淀,在水浴中加热,颜色由灰绿变白,且有絮状白色沉淀下沉,原因为 .
(4)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件 .
【答案】
(1)Fe2++2OH﹣=Fe(OH)2↓
(2)取一定量的灰绿色沉淀,加入盐酸溶解,再加入KSCN溶液,若溶液不变红色,则证明灰绿色物质中不含有Fe(OH)3;2mL0.1mol/LFeCl2溶液;3滴0.1mol/LNaOH溶液;在氢氧化钠溶液浓度一定的条件下,硫酸亚铁溶液的浓度越小,产生白色沉淀的现象越明显;实验2中沉淀下沉后,大部分灰绿色变为白 色沉淀(或实验3中沉淀下沉后,底部都为白色沉淀);向实验2(或实验3)的白色沉淀中继续加入过量的硫酸亚铁溶液,白色沉淀变成灰绿色
(3)Fe2+在加热时易发生水解,生成Fe(OH)2 , 因此颜色变白,同时沉淀的量增加,导致出现絮状白色沉淀
(4)隔绝氧气、硫酸亚铁少量(或氢氧化钠过量)、硫酸亚铁浓度小(或氢氧化钠浓度大)、将氢氧化钠溶液逐滴加入到硫酸亚铁溶液中、微热等
【解析】解:(1)实验1为氢氧化钠与硫酸亚铁生成氢氧化亚铁白色沉淀,离子方程式为:Fe2++2OH﹣=Fe(OH)2↓;所以答案是:Fe2++2OH﹣=Fe(OH)2↓;(2)①证实灰绿色物质中不含有Fe(OH)3 , 可将沉淀溶解,检验其中是否含有铁离子,方法为:取一定量的灰绿色沉淀,加入盐酸溶解,再加入KSCN溶液,若溶液不变红色,则证明灰绿色物质中不含有Fe(OH)3;所以答案是:取一定量的灰绿色沉淀,加入盐酸溶解,再加入KSCN溶液,若溶液不变红色,则证明灰绿色物质中不含有Fe(OH)3;②用等浓度等体积的氯化亚铁与等浓度等体积的氢氧化钠反应与实验1对比:向试管中加入2mL 0.1mol/LFeCl2溶液,再往试管中加入3滴0.1mol/L NaOH溶液,振荡,现象与实验1对比;所以答案是:2mL 0.1mol/LFeCl2溶液;3滴0.1mol/L NaOH溶液;③由实验可知:在氢氧化钠溶液浓度一定的条件下,硫酸亚铁溶液的浓度越小,产生白色沉淀的现象越明显,实验2中沉淀下沉后,大部分灰绿色变为白色沉淀,实验3中沉淀下沉后,底部都为白色沉淀,说明灰绿色是由Fe(OH)2表面吸附Fe2+引起的,通过亚铁离子的浓度改变补充实验,需要向实验2(或实验3)的白色沉淀中继续加入过量的硫酸亚铁溶液,白色沉淀变成灰绿色;所以答案是:在氢氧化钠溶液浓度一定的条件下,硫酸亚铁溶液的浓度越小,产生白色沉淀的现象越明显;实验2中沉淀下沉后,大部分灰绿色变为白色沉淀(或实验3中沉淀下沉后,底部都为白色沉淀);向实验2(或实验3)的白色沉淀中继续加入过量的硫酸亚铁溶液,白色沉淀变成灰绿色;(3)取少量灰绿色沉淀,Fe2+在加热时易发生水解,生成Fe(OH)2 , 因此颜色变白,同时沉淀的量增加,导致出现絮状白色沉淀;所以答案是:Fe2+在加热时易发生水解,生成Fe(OH)2 , 因此颜色变白,同时沉淀的量增加,导致出现絮状白色沉淀;(4)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制隔绝氧气、硫酸亚铁少量(或氢氧化钠过量)、硫酸亚铁浓度小(或氢氧化钠浓度大)、将氢氧化钠溶液逐滴加入到硫酸亚铁溶液中、微热等;所以答案是:隔绝氧气、硫酸亚铁少量(或氢氧化钠过量)、硫酸亚铁浓度小(或氢氧化钠浓度大)、将氢氧化钠溶液逐滴加入到硫酸亚铁溶液中、微热等.


 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
【题目】氧是地壳中含量最多的元素,据此回答问题。
(1)氧元素基态原子核外未成对电子数为。
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为。 的沸点比
的沸点比  高,原因是 .
高,原因是 .
(3)H+可与H2O形成H3O+ , H3O+中O原子采用杂化。H3O+中H—O—H键角比H2O中H—O—H键角大,原因为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于碱性甲醇燃料电池的正极反应,且电极反应式书写正确的是( )
A. CH3OH-6e-=CO2↑+2H2OB. O2+4e-+2H2O=4OH-
C. CH3OH+6e-=CO32-+4OH-D. O2+4e-=2O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Al2 (SO4 )3 、K2 SO4 和明矾的混合溶液中,如果c(SO4 2- )等于0.2 mol/L,当加入等体积的0.2 mol/L 的KOH溶液时,生成的沉淀恰好溶解,则原混合溶液中K + 的物质的量浓度为( )
A.0.2 mol/L
B.0.25 mol/L
C.0.45 mol/L
D.0.225 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的叙述正确的是( )
A.煤井中的瓦斯气和家庭使用的液化石油气的主要成分都是甲烷
B.苯的结构简式为 ![]() ,分子式可简化为CH
,分子式可简化为CH
C.利用酸性KMnO4溶液可鉴别乙烯和乙烷
D.苯与乙烯均能与溴水发生加成反应,而甲烷只能与溴水发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( ) 
A.反应①为取代反应,有机产物浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并伴有浓烟
C.反应③为取代反应,只生成一种产物
D.反应④中1 mol苯最多与3 mol H2发生加成反应,因为苯分子含有3个碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯推测丙烯(CH2=CH﹣CH3)的结构或性质正确的是( )
A.不能使酸性高锰酸钾溶液褪色
B.不能在空气中燃烧
C.能使溴水褪色
D.与HCl在一定条件下能加成只得到一种产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究金属桥墩腐蚀及防护是跨海建桥的重要课题.下列有关判断中正确的是( ) 
A.用装置①模拟研究时未见a上有气泡,说明铁没有被腐蚀
B.②中桥墩与外加电源正极连接能确保桥墩不被腐蚀
C.③中采用了牺牲阳极的阴极保护法保护桥墩
D.①②③中海水均是实现化学能与电能相互转化的电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制取SO2并验证SO2某些性质的装置图。若观察到装置④中有淡黄色沉淀生成,⑤中的溴水褪色(已知因含有Br2而溴水呈红棕色),请回答: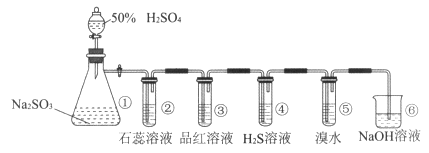
(1)①中发生反应的离子方程式是。
(2)②中的实验现象是。
(3)③的实验现象是 , 证明SO2有性。
(4)④中SO2做剂。
(5)⑤中反应生成两种强酸,该反应的离子方程式是 , 当1 molSO2参与反应时,转移电子的物质的量是。
(6)⑥的作用是。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com