
【题目】有机物A分子式为C2H4,可发生以下系列转化,已知B、D是生活中常见的两种有机物,下列说法不正确的是( )
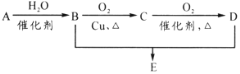
A.75%(体积比)的B溶液常用于医疗消毒
B.D、E都能与NaOH溶液反应
C.由B、D制备E常用浓硫酸作脱水剂
D.B、D、E三种物质可以用饱和Na2CO3溶液鉴别
【答案】C
【解析】
本题考查有机物推断,涉及烯烃、醇、醛、羧酸、酯的性质,比较基础,有利于基础知识的巩固。有机物A分子式为C2H4,则A为CH2═CH2,A与水发生加成反应生成B,B为CH3CH2OH,B发生催化氧化生成C,C为CH3CHO,C进一步氧化生成D,D为CH3COOH,乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3。
A.B为CH3CH2OH,75%的B溶液常用以医疗消毒,选项A正确;
B.D为CH3COOH,与氢氧化钠发生中和反应,E为CH3COOCH2CH3,与氢氧化钠反应生成醋酸钠与乙醇,选项B正确;
C.乙酸乙酯制备中浓H2SO4作催化剂和吸水剂,选项C错误;
D.乙酸与碳酸钠反应生成二氧化碳,有气体生成,乙醇与碳酸钠溶液互溶,而乙酸乙酯与碳酸钠溶液不互溶,溶液分层,现象各不相同,可以进行区别,选项D正确;
答案选C。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
(1)氧化剂______,还原剂________
(2)氧化产物______,还原产物_______
(3)氧化剂与还原剂的物质的量之比:_________________________
(4)用单线桥的方法表示该反应的电子转移情况。________________________
(5)用双线桥的方法表示该反应的电子转移情况。_________________________
(6)当有8mol NH3参加反应时,转移的电子数目为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟基自由基(·OH,电中性,O 为-1 价)是一种活性含氧微粒。常温下,利用·OH 处理含苯酚废水,可将其转化为无毒的氧化物。
(1)·OH 的电子式为________。
(2) pH=3 时 Fe2+催化 H2O2 的分解过程中产生·OH 中间体,催化循环反应如下。将方程式 ii 补充完整。
i.Fe2++ H2O2+H+ = Fe3++ H2O +·OH
ii.___ + ___= ___+ O2↑+2H+
(3)已知:羟基自由基容易发生猝灭 2·OH = H2O2,从而活性降低.用 H2O2 分解产生的·OH 脱除苯酚,当其他条件不变时,不同温度下,苯酚的浓度随时间的变化如图 1 所示.0~20 min 时,温度从40℃上升到 50℃,反应速率基本不变的可能原因是________。
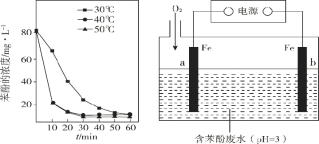
(4)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚废水更加高效,装置如图2所示。已知 a 极主要发生的反应是 O2 生成 H2O2,然后在电解液中产生·OH 并迅速与苯酚反应。
①b 极连接电源的________极(填“正”或“负”)。
②a 极的电极反应式为______。
③除电极反应外,电解液中主要发生的反应方程式有 ________ , _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C,改变0.01 mol·L一1 CH3COONa溶液的pH.溶液中c(CH3COOH)、c(CH3COO-)、c(H +)、c(OH- )的对数值lgc与溶液pH的变化关系如图所示,下列叙述正确的是
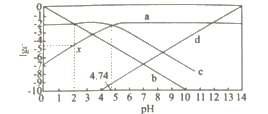
A.图中任意点均满足c(CH3COOH)+c(CH3COO-)=c(Na+)
B.0.01 mol·L-1CH3COOH的pH约等于线a与线c交点处的横坐标值
C.由图中信息可得点x的纵坐标值为4.74
D.25°C时,![]() 的值随 pH的增大而增大
的值随 pH的增大而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海带中提取碘,可经过以下实验步骤完成。下列有关说法正确的是
![]()
A. 灼烧过程中使用的玻璃仪器有酒精灯、烧杯、玻璃棒
B. 氧化过程中发生反应的离子方程式为 2I-+H2O2 =I2+2OH-
C. 检验碘单质时,可选用淀粉碘化钾试纸,若试纸变蓝说明海带中含有碘单质
D. 分液时,先打开活塞放出下层液体,再关闭活塞从上口倒出上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A. 16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA
B. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
C. pH=1的H3PO4溶液中,含有0.1NA个H+
D. 10 g的D2O中含有的质子数与中子数分别为5NA和4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物中间体(G)在有机制药工业中的一种合成方法如下:
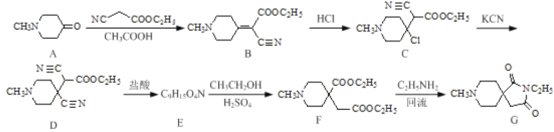
回答下列问题:
(1)化合物D和G中含氧官能团的名称分别为___________、_________。
(2)由B→C的反应类型为_____ ;写出C→ D反应的化学方程式:________。
(3)化合物E的结构简式为________。
(4)反应F→G的另一种生成物是___________。
(5)写出同时满足下列条件的B的同分异构体的结构简式:_______。
①能与新制Cu(OH)2加热条件下反应生成砖红色沉淀,水解产物之一能与FeCl3溶液发生显色反应:
②核磁共振氢谱为四组峰,峰面积比为1:2:4:9;
③分子中含有氨基。
(6)已知:RCN![]() RCH2NH2请设计以HOOCCH2COOH和CH3CH2Cl为原料制备
RCH2NH2请设计以HOOCCH2COOH和CH3CH2Cl为原料制备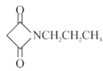 的合成路线:_________(无机试剂任用)。
的合成路线:_________(无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中。
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀。
③在50~60℃下发生反应,直至反应结束。
④除去混合酸后,粗产品依次用H2O和5%NaOH溶液洗涤,最后再用H2O洗涤。
⑤将污水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
(1)配制一定比例浓硫酸与浓硝酸混合酸时,操作注意事项是_____________________________________。
(2)步骤③中,为了使反应在50~60℃下进行,可采用的方法是________________________________。
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是____________________;步骤④中粗产品用5%NaOH溶液洗涤的目的是__________________________________________________。
(4)实验室制备常用改进装置进行苯和溴的取代反应。如实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉。
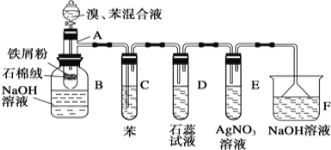
向反应容器A中逐滴加入溴和苯的混合液,几秒中内就发生反应。写出A中所发生反应的化学方程式:_________________________________________________。
(5)试管C中苯的作用是_________________________。反应开始后,观察D和E两试管,看到的现象为___________________________________,________________________________。
(6)反应2~3min后,在B中的NaOH溶液里可观察到的现象是_______________________________。
(7)同学甲认为,在上述整套装置中D和E两试管中的导管应插入液面下,实验现象更明显,请评价同学甲的改进建议:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下两个反应:(A)Cu2++Zn=Cu+Zn2+(B)2FeCl3+Cu=2FeCl2+CuCl2。
(1)分别画出两个实验装置图,注明电解质溶液名称和正负极材料,标出电子流动方向___、___。
(2)写出下列电极反应式:
①(A)中___是负极,负极反应式:___;
②(B)中___是负极,负极反应式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com