
【题目】关于化学键的下列叙述中,正确的是( )
①离子化合物可以含共价键②共价化合物可能含离子键 ③离子化合物中只能含离子键 ④共价化合物中不含离子键 ⑤共价化合物只含共价键⑥共价化合物可能含极性键和非极性键
A. ①④⑤⑥ B. ①③⑥ C. ②③④⑥ D. ②④⑥
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离的c(H+)=1×10-13mol/L,该溶液可能是 ( )
①SO2水溶液 ②NH4Cl溶液 ③NaNO3溶液 ④NaOH溶液
A. ②③ B. ①④ C. ③④ D. ①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(正确的打“√”,错误的打“×”)。
(1)稀豆浆、硅酸、氯化铁溶液均为胶体(_____)
(2)明矾水解时产生具有吸附性的胶体粒子,可作漂白剂(_____)
(3)沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强(______)
(4)“血液透析”利用了胶体的性质(______)
(5)葡萄糖注射液不能产生丁达尔现象,不属于胶体(______)
(6)向污水中投入明矾,生成能凝聚悬浮物的胶体:Al3++3H2O=Al(OH)3(胶体)+3H+(_____)
(7)电泳现象可证明胶体属于电解质溶液(_____)
(8)利用丁达尔效应可以区别溶液与胶体(_____)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为:N2H4+O2═N2+2H2O下列关于该电池工作时说法正确的是( )

A.甲池中负极反应为:N2H4﹣4e﹣═N2+4H+
B.甲池溶液pH不变,乙池溶液pH减小
C.反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度
D.甲池中消耗2.24L O2,此时乙池中理论上最多产生12.8g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
对甲苯丙烯酸甲酯 (E)是一种用于合成抗血栓药的中间体,其合成路线如下:
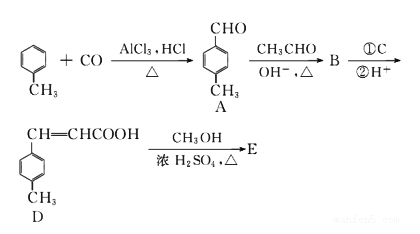
已知:HCHO+CH3CHO![]() CH2=CHCHO+H2O
CH2=CHCHO+H2O
(1)A中官能团的名称为_______,A分子中核磁共振氢谱各峰值比为________。
(2)物质B的结构简式为_______,生成E的反应类型为__________。
(3)试剂C可选用下列中的_________。
a.溴水 b.银氨溶液 c.酸性KMnO4溶液 d.新制Cu(OH)2悬浊液
(4)![]() 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________。
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________。
(5)遇FeCl 3溶液显紫色,且苯环上有两个取代基的A的同分异构体有______种,E在一定条件下可以生成高聚物F,F的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。
(1)提出假设①该反应的气体产物是CO2;②该反应的气体产物是CO。
③该反应的气体产物是 。
(2)设计方案,如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。

(3)查阅资料
氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气。
请写出该反应的离子方程式: 。
(4)实验步骤
①按上图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g。
步骤②、④中都分别通入N2,其作用分别为 。
(5)数据处理
试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式: 。
(6)实验优化 学习小组有同学认为应对实验装置进一步完善。
①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是 。
②从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述正确的是
①CS2为V形的极性分子②ClO3-的立体构型为平面三角形
③SF6中有6对完全相同的成键电子对④SiF4和SO32-的中心原子均采用sp3杂化
A.①③B.②④C.①②D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 金刚石、石墨、C60互为同素异形体,它们都是分子晶体
B. 二氧化碳分子和水分子中所有原子在同一条直线上
C. 正丁烷和异丁烷的分子式都为C4H10,它们互为同分异构体
D. 14C与14N互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取NaOH的化学反应方程式为:2NaCl + H2O![]() 2NaOH + H2↑+ Cl2↑,工艺流程示意图如下:
2NaOH + H2↑+ Cl2↑,工艺流程示意图如下:

下表是NaCl和MaOH在水中的溶解度
温度 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
NaCl | 35.7g | 36g | 36.6g | 37.3g | 38.4g | 39.8g |
NaOH | 42g | 109g | 129g | 174g | 314g | 347g |
依据示意图和表,完成下列填空:
(1)工业食盐中含CaCl2、MgCl2等杂质。除去Ca2+、Mg2+过程发生反应的化学反应方程式为_____。
(2)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过______、冷却、______(填写操作名称)除去NaCl。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是________(填字母序号)。
①Ba(NO3)2 ②BaCl2
(4)为了有效地除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为_______(少选多选都不计分)。
A.先加NaOH,后加Na2CO3,再加钡试剂 B.先加Na2CO3,后加钡试剂,再加NaOH
C.先加钡试剂,后加NaOH,再加Na2CO3 D.先加NaOH,后加钡试剂,再加Na2CO3
(5)用制得的 NaOH固体配制 240 mL0.2mol/L NaOH 溶液。
①配制时,必須使用的玻璃仪器有______________________。
②某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。
烧杯的实际质量为________________g。

③在配制过程中,其他操作都是正确的,下列情对所配制的NaOH珩液的浓度偏高有_____。
A.没有洗涤烧杯和玻璃棒 B.容量瓶不干燥,含有少量蒸馏水
C.定容时俯视刻度线 D.定容时仰视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
④下图是该同学转移溶液的示意图,图中的错误是_____________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com