
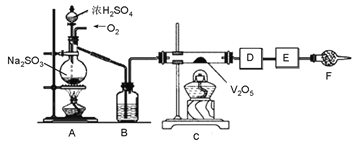
【题目】下图的实验装置可用于研究SO2转化为SO3的转化率。已知:SO3的熔点是16.8℃,沸点是44.8℃。A处为SO2气体发生装置,C处为SO2与O2反应的装置。
完成下列填空:
(1)A处的化学反应方程式为_______________,仪器F的名称为_____。
(2)根据实验需要,应该在D、E处连接合适的装置。请从下图中选择,将所选装置的序号填入相应的空格,D:__________,E:_________。

(3)用amolNa2SO3粉末与足量浓硫酸进行此实验,当A处反应结束时,再继续通入一段时间O2,最后测得E处装置增重bg,则此时SO2的转化率为__________%(用含a、b的代数式表示)。
(4)若Na2SO3变质,会影响到SO2的转化。现欲检验某Na2SO3样品是否变质,你的方法是____________。
(5)实验结束后,如果将收集了SO3的装置敞口露置于空气中,可看到装置出口处产生大量白雾,其原因是________________________。
【答案】 Na2SO3+ H2SO4(浓)→H2O + SO2↑ + Na2SO4 干燥管 ③ ④ ![]() 或
或![]() 取待测样品少许于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液,若有白色沉淀生成,则证明该样品变质。若无白色沉淀生成,则证明该样品未变质 三氧化硫是一种易升华的固体,在空气中三氧化硫气体易吸收水蒸汽而形成酸雾
取待测样品少许于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液,若有白色沉淀生成,则证明该样品变质。若无白色沉淀生成,则证明该样品未变质 三氧化硫是一种易升华的固体,在空气中三氧化硫气体易吸收水蒸汽而形成酸雾
【解析】(1)A处制备SO2,反应的化学反应方程式为Na2SO3+H2SO4(浓)=H2O+SO2↑+Na2SO4,仪器F的名称为干燥管。(2)SO3的熔点是16.8℃,沸点是44.8℃,所以收集三氧化硫时需要利用冰水冷却,即D处是③;又因为SO2是大气污染物,则E处需要吸收多余的SO2,选择碱石灰,即E处是④;(3)用amolNa2SO3粉末与足量浓硫酸进行此实验,根据硫原子守恒可知生成的SO2是amol。当A处反应结束时,再继续通入一段时间O2,最后测得E处装置增重bg,即剩余的SO2是bg,所以此时SO2的转化率为![]() ;(4)Na2SO3变质转化为硫酸钠,所以检验某Na2SO3样品是否变质的方法是取待测样品少许于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液,若有白色沉淀生成,则证明该样品变质。若无白色沉淀生成,则证明该样品未变质;(5)由于三氧化硫是一种易升华的固体,在空气中三氧化硫气体易吸收水蒸汽而形成酸雾,所以实验结束后,如果将收集了SO3的装置敞口露置于空气中,可看到装置出口处产生大量白雾。
;(4)Na2SO3变质转化为硫酸钠,所以检验某Na2SO3样品是否变质的方法是取待测样品少许于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液,若有白色沉淀生成,则证明该样品变质。若无白色沉淀生成,则证明该样品未变质;(5)由于三氧化硫是一种易升华的固体,在空气中三氧化硫气体易吸收水蒸汽而形成酸雾,所以实验结束后,如果将收集了SO3的装置敞口露置于空气中,可看到装置出口处产生大量白雾。


科目:高中化学 来源: 题型:
【题目】下列叙述中,不正确的是
A. 越冬的植物体内自由水与结合水的比值下降,有利于抵抗不利的环境条件
B. 蔗糖、麦芽糖、乳糖、糖原完全水解产物都有葡萄糖
C. 淀粉、糖原、纤维素和核糖都是生物大分子
D. 多糖、蛋白质、核酸等是以碳链为骨架的生物大分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为直流电源电解稀Na2SO4水溶液的装置,通电后在石墨电极a和b附近分别滴加石蕊溶液,下列实验现象正确的是( )

A. 逸出气体的体积:a电极的小于b电极的
B. a电极附近呈蓝色,b电极附近呈红色
C. a电极附近呈红色,b电极附近呈蓝色
D. 一电极逸出无味气体,另一电极逸出刺激性气味气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.丁达尔效应可用于鉴别胶体和溶液
B.胶体粒子的直径在1~100 nm之间
C.胶体一定是混合物
D.将FeCl3稀溶液溶于冷水即可制得Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生社团根据老师的指导进行实验研究:一块下衬白纸的玻璃片上有a、b、c、d四个位置,分别滴加浓度为0.1 mol/L的四种溶液各1滴,每种彼此分开,形成一个个小液滴。在圆心e处放置2粒芝麻粒大小的KMnO4晶体,然后向KMnO4晶体滴加一滴浓盐酸,并将表面皿盖好。可观察到a、b、c、d、e五个位置均有明显反应。
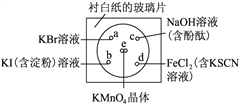
完成下列填空:
(1)e处立即发生反应,化学方程式如下,请配平,并标出电子转移方向和数目______。
![]() KMnO4+
KMnO4+![]() HCl(浓)→
HCl(浓)→![]() KCl+
KCl+![]() MnCl2+
MnCl2+![]() Cl2↑+
Cl2↑+![]() H2O
H2O
(2)在元素周期表中Cl、Br、I位于___________________ 族 ,它们最高价氧化物所对应水化物酸性最强的是__________________(填化学式)。
(3)b处实验现象为_____________________。d处反应的离子方程式为__________________,通过此实验________(填“能”或“不能”)比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱。若能,则其氧化性由强到弱的顺序是___________________________________。
(4)常温下,向饱和氯水中逐滴滴入0.1mol/L的氢氧化钠溶液,pH变化如下图所示,下列有关叙述正确的是__________。
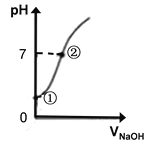
A.①处所示溶液中存在的电离平衡不止一个
B.由①到②的过程中,溶液由酸性逐渐变为碱性
C.由①到②的过程中,水的电离程度逐渐减弱
D.②处所示溶液中:c(Na+)=c(Cl-) + c(ClO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素A原子的L电子层比元素B原子的L电子层少 3个电子,B元素原子核外电子总数比A元素原子核外电子总数多5个,则A、B形成的化合物的化学式可能为( )
A.B2A3B.B3A2
C.A2B3D.BA2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生应用如下图所示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气。回答下列问题:
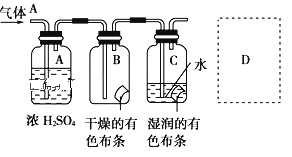
(1)该项研究(实验)的主要目的是__________________________________。
(2)浓H2SO4的作用是 _______________________,与研究目的直接相关的实验现象是___________________。
(3)从物质性质的方面来看,这样的实验设计还存在不妥之处,有隐患,隐患表现为__________________。请在D处以图的形式表明克服隐患的措施__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族, Z、R 、W同周期。下列说法错误的是( )
A. 原子半径:Z>R>W
B. 气态氢化物稳定性:HmW>HnR
C. XW4分子中各原子均满足8电子结构
D. Y、Z、R三种元素组成的化合物水溶液一定显碱性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com