
【题目】某有机物A的结构简式如如图。
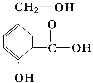
(1)请写出该物质的含氧官能团名称______、______和______。
(2)请写出以下化学反应的方程式:
①A跟NaOH溶液反应:__________
②A跟NaHCO3溶液反应:__________
③A在一定条件下跟Na反应:__________
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1 mol N-N吸收193 kJ热量,生成1 mol N≡N放出941 kJ热量。根据以上信息和数据,下列说法正确的是( )
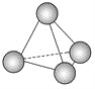
A. N4属于一种新型的化合物
B. N4是N2的同位素
C. N4转变为N2是物理变化
D. 1 mol N4气体转变为N2放出724 kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。A、C、E是常见的金属单质,E为紫红色,反应①可用于焊接铁轨,B是赤铁矿的主要成分,F的溶液中加入KSCN溶液变红。(部分反应物和生成物省略)
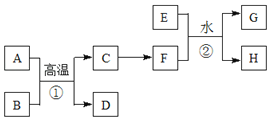
请回答下列问题:
(1)B的化学式是____________D的化学式是_____________
(2)可选用__________(填“字母”)实现反应C→F的转化。
a.稀盐酸 b.氯气/点燃 c.CuSO4溶液
(3)反应①的化学方程式为___________________________。
(4)反应②的离子方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是________。
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1 mol/L,c(Fe3+)=0.3 mol/L,c(SO42-)=0.6 mol/L,则c(K+)为________。
(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为________。
(4)某状况下a L氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成b mL氨水溶液,所得溶液的密度为ρ g/mL,则该氨水的物质的量浓度可表示为________ mol/L;氨水的质量分数为________。
(5)已知1.505×1023个X气体分子的质量是8 g,则X气体的摩尔质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应是化学实验现象的本质,根据描述回答下列问题:
(1)在BaCl2溶液中通入SO2气体,未见沉淀生成,若先通入或加入下列的另一种物质,再通入SO2能看到沉淀的有___(填序号)。
①NO2 ②NH3 ③HCl ④FeCl3溶液 ⑤CO2
(2)A、B、C、D、E五种物质(或离子)均含有同一种元素,它们之间有如图所示的转化关系:
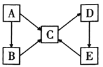
若A为金属单质,B、C均属于盐类,B溶液呈黄色,与硫氰化钾溶液混合后显红色,D是一种白色沉淀,E是一种不溶性碱。B溶液呈酸性的原因是___(用离子方程式表示);选用氢碘酸可与E反应实现E→C的转化,该反应的离子方程式为___。
(3)①通常条件下,未经碾磨的镁粉和未经擦拭的镁条跟冷水不反应,因为表面有一层保护膜。去除这层氧化膜后,镁与冷水就会发生明显的反应,看到有大量细腻的气泡产生。在室温条件下,反应生成的难溶于水的氢氧化镁,沉积在表面形成致密薄膜,几分钟后,反应很快停止。给反应混合液加热,镁跟水的作用又会重新进行,你觉得可能的原因是:___,此时滴加酚酞试液,___(填“会”或“不会”)出现溶液变红的现象。
②取一段擦去表层氧化膜的镁条,卷成螺旋状,插入盛满食盐水的试管中,将试管倒扣在盛有食盐水的烧杯中,可以迅速观察到镁持续不断地跟水反应,你觉得可能的原因是___。
③去除了氧化膜的金属Mg可以与NaHCO3溶液作用析出氢气,溶液中有白色难溶物生成。这是由于镁直接与水反应,转化为H2和Mg(OH)2。溶解在水中的少量Mg(OH)2电离生成的OH-与溶液中的HCO3-反应生成CO32-,促使反应生成的Mg(OH)2更多溶解。溶液中Mg2+、OH-、CO32-,结合析出白色难溶物Mg2(OH)2CO3。请根据以上信息写出Mg与NaHCO3溶液的总反应式:___(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,有关制备途径及性质如下图所示。下列说法错误的是( )

A.途径①所用混酸中H2SO4与HNO3的最佳物质的量之比为3:2
B.与途径①、③相比,途径②更好地体现了绿色化学思想
C.生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量①=②<③
D.利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
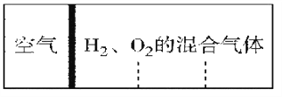
【题目】如图所示,室温下分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2 和O2 的混合气体,若将H2、O2 的混合气体点燃引爆。活塞先左弹,恢复室温后,活塞右滑停留于容器的中央。则原来H2、O2 的物质的量之比可能为①4∶5 ② 2∶5 ③3∶8 ④7∶2
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中,只含有下表中所示的四种离子,则X离子及其个数b可能为( )
离子 | Na+ | Al3+ | Cl- | X |
个数 | 3a | 3a | 2a | b |
A.![]() 、4aB.
、4aB.![]() 、4aC.
、4aC.![]() 、8aD.
、8aD.![]() 、5a
、5a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A. 已知2H2(g)+O2(g)=2H2O(l)△H=﹣483.6 kJmol﹣1,则氢气的燃烧热为483.6 kJmol﹣1
B. 在一定温度和压强下,将0.5mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放出热量19.3 kJ,则其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) △H=﹣19.3kJ/mol
2NH3(g) △H=﹣19.3kJ/mol
C. 已知2C(s)+2O2(g)=2CO2(g)△H1 2C(s)+O2(g)=2CO(g)△H2 则△H1>△H2
D. 已知Ni(CO)4(s)=Ni(s)+4CO(g) △H=Q kJmol﹣1,则Ni(s)+4CO(g)=Ni(CO)4(s) △H=﹣Q kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com