
| A. | Cl- | B. | Ag+ | C. | NO3- | D. | Fe3+ |
分析 混合后溶液中Ag++Cl-=AgCl↓,Ag+和Cl-的浓度减小,计算溶液中铁离子和硝酸根离子再比较.
解答 解:混合后溶液中Ag++Cl-=AgCl↓,Ag+和Cl-的浓度减小,c(Cl-)=$\frac{1mol/L×3×0.2L-0.3mol/L×0.5L}{0.5L+0.2L}$=$\frac{4.5}{7}$mol/L;溶液中c(Fe3+)=$\frac{1mol/L×0.2L}{0.2L+0.5L}$=$\frac{2}{7}$mol/L,c(NO3-)=$\frac{0.3mol/L×0.5L}{0.2L+0.5L}$=$\frac{1.5}{7}$mol/L,所以混合液中所含的离子浓度最大的是Cl-,
故选A.
点评 本题考查了离子反应和物质的量浓度的计算,题目难度不大,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:解答题
 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置:
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中X位于Y的上一周期 | |
| B. | X的含氧酸的酸性强于Y的含氧酸的酸性 | |
| C. | 将H2X、HY分别加热至500℃,只有HY发生分解 | |
| D. | Xn-的还原性强于Ym- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O | |
| B. | 2CH3CH2OH+O2 $→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| D. | 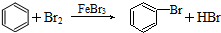 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a、b | B. | b、c | C. | a、d | D. | b、d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | L层上的电子数为奇数的元素一定是主族元素 | |
| B. | 族序数等于周期序数的元素一定是金属元素 | |
| C. | 由不同种元素组成的多原子分子里,一定只存在极性键 | |
| D. | 共价化合物只含有共价键,离子化合物只含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如图所示的装置.
氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如图所示的装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | 只有①②③④ | C. | 只有①②③ | D. | 只有①③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com