
����Ŀ��ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������100mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ������ѻ���ɱ�״̬����
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
���������mL�� | 50 | 120 | 232 | 290 | 310 |
��1����һʱ��Σ�ָ0��1��1��2��2��3��3��4��4��5min����Ӧ�������
��2����һ��ʱ�εķ�Ӧ������С ��
��3����2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ���ʣ�����Һ������䣩 ��
��4�������Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ������������������������зֱ����������������Һ��
A.����ˮ
B.NaCl��Һ
C.Na2CO3��Һ
D.CuSO4��Һ
����Ϊ���е��ǣ����ţ� ��
���𰸡�
��1��2��3 min
��2��4��5 min
��3��0.1mol/��L��min��
��4��AB
���������⣺0��1 min��1��2 min��2��3 min��3��4 min��4��5min����ʱ��ε���������ֱ�Ϊ��50 mL��70mL��112 mL��58 mL��20 mL��
��1.����ͬͨ�����£���Ӧ����Խ����ͬʱ�����ռ�������Խ�ࣻ������ã���Ӧ��������ʱ�����2��3 min��ԭ���ǣ��÷�Ӧ�Ƿ��ȷ�Ӧ���¶�Խ�ߣ���Ӧ����Խ�����Դ��ǣ�2��3 min��
��2.����ͬͨ�����£���Ӧ����ԽС����ͬʱ�����ռ�������Խ�٣�������ã���Ӧ������С��ʱ����ǣ�4��5min��ԭ���ǣ����ŷ�Ӧ�Ľ��У������Ũ���ڼ�С��Ũ��ԽС����Ӧ����Խ�������Դ��ǣ�4��5min��
��3.��2��3 min���������������112 mL������Ҫ��������ʵ���Ϊxmol��
Zn | + | 2HCl | = | ZnCl2 | + | H2 �� | |
2mol | 22.4L | ||||||
xmol | 0.112L |
x=0.01 ����v��HCl ��= ![]() =0.1mol/��L��min�������Դ��ǣ�0.1mol/��L��min����
=0.1mol/��L��min�������Դ��ǣ�0.1mol/��L��min����
��4.���ı仯ѧ��Ӧ���ʵķ����У��ı���Һ��Ũ�ȡ��ı���Һ���¶ȡ��ı����ı�����ȣ�A��������ˮ����Һ���������Ũ�Ƚ��ͣ���Ӧ���ʼ�С�������ɵ�����������䣬��A��ȷ��B����NaCl��Һ����Һ���������Ũ�Ƚ��ͣ���Ӧ���ʼ�С�������ɵ�����������䣬��B��ȷ��C����Na2CO3��Һ����Һ��������������Ũ�Ƚ��ͣ��������̼���Ʒ�Ӧ���ɶ�����̼������������С����C����D����CuSO4��Һ�����γ�ͭпԭ��أ��ӿ췴Ӧ���ʣ���D����ѡ��AB��


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Σ�ջ�ѧҩƷҪ�ڰ�װ��ǩ��ӡ�Ͼ�ʾ�Ա�־�����л�ѧҩƷ�����뾯ʾ��־���ƶ�Ӧ��ȷ����(����)
A. �ƾ������綾Ʒ B. Ũ���ᡪ����ʴƷ
C. ���͡�����ըƷ D. �ռ���綾Ʒ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮԡ���ȵ�ʵ���ǣ� ��
A.����������ӦB.��ȩ��������Ӧ
C.ʵ��������������D.ʵ���������ᶡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�������A�Ľṹ��ʽ���£�

(1)A�ķ���ʽ��________��
(2)A��NaOHˮ��Һ�г�ּ��Ⱥ��ټ�������������ữ�ɵõ�B��C��D��![]() �����л������Է���������С��ϵΪB>C>D����B��C��D�Ľṹ��ʽ�ֱ���B________��C________��D________��
�����л������Է���������С��ϵΪB>C>D����B��C��D�Ľṹ��ʽ�ֱ���B________��C________��D________��
(3)���������У�������B������ѧ��Ӧ����________(������)��
��ŨH2SO4��ŨHNO3�Ļ��Һ����CH3CH2OH(���)����CH3CH2CH2CH3����Na����Ũ��ˮ
(4)��B��ͬ���칹���У�����1,3,5��ȡ�����Ļ�����Ľṹ��ʽΪ_________________��
(5)д��B��̼�����Ʒ�Ӧ�Ļ�ѧ����ʽ��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ҵ���Ũ�����ϼ��ȿɷ������·�Ӧ��CH3CH2OH��CH2-CH2��+H2O���ɿ����Ҵ���������ȥһ����ˮ��������ϩ��
(1)lmol���ΪC3H8O��Һ̬�л���A���������Ʒ�Ӧ����11.2LH2(��״��������A�б���һ��_____�������˻�����̼����һ�ˣ���A�Ľṹ��ʽΪ_____________��
(2)A��Ũ���Ṳ��Ҳ�ɷ�������ȥһ����ˮ������B��д����Ӧ�Ļ�ѧ����________________��
(3)Bͨ����ˮ�пɷ���__________��Ӧ���÷�Ӧ�ķ���ʽΪ��___________________��
(4)A��ͭ˿���£�����ʱ��O2��Ӧ�Ļ�ѧ����ʽΪ��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ϱ�����MnO2��Fe3+��H2O2�Ʊ�O2�����д����á�ij����С��ͬѧ��ʵ���ҽ�������֤���鲢�о���H2O2�������ʡ��ش��������⣺
��1��������֧�ֱ�ʢ��2 mL10% H2O2��Һ���Թܣ���ͬѧ�ڵ�һ���ڶ�֧�Թ��зֱ����MnO2������FeCl3��Һ�����־��д����������ɣ������֧�Թ��м���������������Һ���۲�������Ŀ����________��
��2����ͬѧ����������ϣ���ô���������ͼ��ʾ��
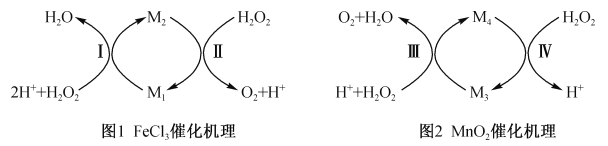
��ͼ1����M1��_______���ѧʽ����
��ͼ2����M4ΪMn2+����Ӧ�������ӷ���ʽΪ_____________��
��3����ͬѧ���Թ��м���2 ml. 3%��H2O2��Һ��0.5mL���ѣ�l mL1 mol/LH2SO4��Һ��3��4��0.5mol/L��K2Cr2O7��Һ�������ϲ��л���Ϊ��ɫ��CrO5��������Һ�����²�ˮ��Ϊ��ɫ��
�����ѳ���ΪCrO5���ȶ����⣬��һ������____________��
��һ��ʱ�����ɫ��ȥ������������������ͬʱˮ������Һ��Ϊ��ɫ����Cr3+������ɫ��Ӧ�����ӷ���ʽΪ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���1 mol��CuSO4��5H2O(s)����ˮ��ʹ��Һ�¶Ƚ��ͣ���ЧӦΪ��H1����1 mol��CuSO4(s)����ˮ��ʹ��Һ�¶����ߣ���ЧӦΪ��H2��CuSO4(s)��5H2O(s)���ȷֽ�Ļ�ѧ����ʽΪCuSO4��5H2O(s)![]() CuSO4(s)��5H2O(l)����ЧӦΪ��H3���������ж���ȷ����(����)
CuSO4(s)��5H2O(l)����ЧӦΪ��H3���������ж���ȷ����(����)
A. ��H2����H3 B. ��H1����H3 C. ��H1����H3����H2 D. ��H1����H2����H3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Һ�м���Ba2+����ְ�ɫ�����������Һ��һ������
A. Fe3+ B. SO42- C. NO3- D. Cl-
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com