
【题目】己知乙醇与浓硫酸混合加热可发生如下反应:CH3CH2OH→CH2-CH2↑+H2O,可看作乙醇分子中脱去一分子水而生成乙烯。
(1)lmol组成为C3H8O的液态有机物A,与足量钠反应生成11.2LH2(标准状况),则A中必有一个_____基,若此基连在碳链的一端,则A的结构简式为_____________。
(2)A与浓硫酸共热也可分子内脱去一分子水而生成B,写出反应的化学方程________________。
(3)B通入溴水中可发生__________反应,该反应的方程式为:___________________。
(4)A在铜丝催化下,加热时与O2反应的化学方程式为:___________________。
【答案】 羟 CH3CH2CH2OH CH3CH2CH2OH→CH3CH=CH2↑+H2O 加成 CH3CH=CH2+Br→CH3CHBrCH2Br 2CH3CH2CH2OH+O2![]() 2CH3CH2CHO+2H2O
2CH3CH2CHO+2H2O
【解析】(1)1mol分子组成为C3H8O的液态有机物A,与足量的金属钠作用,可生成11.2L氢气,n(H2)=11.2L÷22.4L/mol=0.5mol,该有机物为丙醇,含有羟基,若羟基在碳链的一端,应为CH3CH2CH2OH;(2)在浓硫酸作用下发生消去反应可生成CH3CH=CH2,反应的方程式为:CH3CH2CH2OH![]() CH3CH=CH2+H2O;(3)丙烯与溴水发生加成反应可生成CH3CHBrCH2Br,方程式为:CH3CH=CH2+Br2→CH3CHBrCH2Br;(4)CH3CH2CH2OH发生催化氧化可生成CH3CH2CHO,方程式为:2CH3CH2CH2OH+O2
CH3CH=CH2+H2O;(3)丙烯与溴水发生加成反应可生成CH3CHBrCH2Br,方程式为:CH3CH=CH2+Br2→CH3CHBrCH2Br;(4)CH3CH2CH2OH发生催化氧化可生成CH3CH2CHO,方程式为:2CH3CH2CH2OH+O2![]() CH3CH2CHO+2H2O。
CH3CH2CHO+2H2O。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】为了保护自然环境,提高人民的生活质量,必须重视处理“白色污染”。该“白色污染”指的是( )
A. 冶炼厂的白色烟尘B. 石灰窑的白色粉末
C. 聚氯乙烯等塑料垃圾D. 白色建筑材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用 0.100 mol·L-1 的 NaOH 溶液滴定 10.00 mL 浓度均为 0.100 mol·L-1 的盐酸和 CH3COOH 溶液。利用传感器测得滴定过程中溶液的电导 率如图所示。下列说法正确的是( )

A. 曲线①代表滴定 HCl 溶液的曲线
B. A 点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol·L-1
C. 在相同温度下,A、B、C 三点溶液中水的电离程度:C<B=A
D. D 点溶液中:c(Cl-)=2c(OH-)-2c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化氢(PH3)是一种无色剧毒气体,沸点为-89.7℃,易自燃,与空气混合爆炸,微溶于水。其制取原理类似于实验室制氨气,现用下图装置来制取磷化氢并验证其性质。
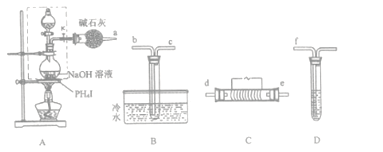
实验开始时,先从分液漏斗向盛有PH4I的圆底烧瓶中加入过量乙醚(无色液体,沸点34.5℃,微溶于水,不与Fe2(SO4)3反应),微热数分钟后再从分液漏斗向圆底烧瓶中加入一定量的浓NaOH溶液继续加热。在装置C处用电热器控制温度在300℃左右,实验过程中可观察到:B装置的试管中有白色蜡状固体生成;D装置的试管中Fe2(SO4)3溶液颜色由棕黄色变成淡绿色,同时也有白色蜡状固体生成。请回答:
(1)按气流方向连接装置,从左到右的顺序为:
a→______→ → → →f
(2)检查A中虚线框内装置的气密性的方法是____
(3)用PH4I和烧碱反应制取PH3的化学方程式是_____________。
(4)实验开始时,先向圆底烧瓶中加入乙醚并微热数分钟,其目的是__________。
(5)装置C中反应的化学方程式是____________;装置D中反应的离子方程式是_____________。
(6)装置B、D中的现象说明PH3具有的化学性质是_________(填字母序号)。
A.碱性 B.不稳定性 C.还原性 D.酸性
(7)实验时处理尾气的方法是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
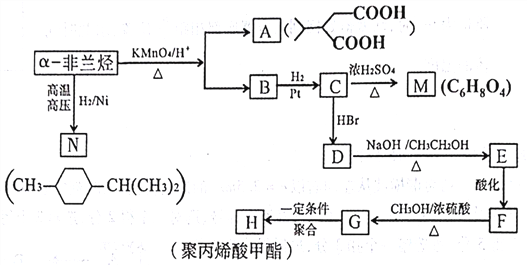
【题目】薄荷油中含有少量的a-非兰烃可以通过下列过程制得聚丙烯酸甲酯(H):
![]()
![]()
![]() +RˊCOOH
+RˊCOOH
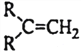
![]()
![]() +CO2
+CO2
(1)写出a-非兰烃的结构简式___________。写出C—M的反应类型___________。
(2)下面是对于A、B、C、D的性质描述,其中正确的是___________(填标号)。
a.lmol A 可与2molNaHCO3反应放出2molCO2
b.lmolB可与2molH2发生加成反应
c.C可以发生缩聚反应
d.检验D的卤素原子种类可与NaOH水溶液共热后再加AgNO3溶液
(3)N的同分异构体中能同时满足下列两个条件的共有___________种(不含立体异构);其中核磁共振氢谱显示4组峰,且峰面积之比为4∶3∶2∶1的是___________(写结构简式)。
①含有一个六元环
②六元环上只有两个取代基,且环上每个碳原子最多只能有一个取代基
(4)E在一定条件下发生聚合反应可得到一种高级吸水树脂,写出生成该树脂反应的
化学方程式___________。
(5)写出F→G反应的化学方程式___________。
(6)BrCH2CH2CH2OH和甲醇也可以用来合成聚丙烯酸甲酯(H),写出合成路线___________(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)。
目标产物)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己醇(![]() )常用来制取增塑剂和作为工业溶剂。下列说法正确的是( )
)常用来制取增塑剂和作为工业溶剂。下列说法正确的是( )
A. 环己醇中至少有12个原子共平面
B. 与环己醇互为同分异构体,且含有醛基(—CHO)的结构有8种(不含立体结构)
C. 标准状况下,1mol环己醇与足量Na反应生成22.4LH2
D. 环己醇的一氯代物有3种(不含立体结构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】伞形酮可用作荧光指示剂和酸碱指示剂。其合成方法为
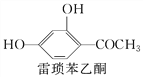

下列说法不正确的是( )
A. 雷琐苯乙酮、苹果酸和伞形酮各1 mol与足量Na反应生成H2体积之比为2∶3∶1
B. 雷琐苯乙酮和伞形酮都能跟FeCl3溶液发生显色反应
C. 1 mol雷琐苯乙酮跟足量H2反应,最多消耗4 mol H2
D. 1 mol伞形酮与足量NaOH溶液反应,最多消耗2 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如右图(夹持仪器略去),主要步骤如下:

步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入适量的液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至室温,过滤,将滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 常温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MsBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性
②MgBr2+3C2H5OC2H5![]() MgBr23C2H5OC2H5
MgBr23C2H5OC2H5
请回答:
(1)仪器A的名称是_______,它在实验中的作用是_________。
(2)步骤2中,可以将B装置中的溴完全导入三颈瓶中的原因是_______;该实验如果将所用的液溴一次性全部加入三颈瓶中,其后果是____________。
(3)步骤3中,第一次过滤得到的固体的物质是_______;根据步骤3、4,总结三乙醚合溴化镁所具有的物理性质:_________________________。
(4)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:
Mg2++Y4-==Mg Y2-
①滴定前润洗滴定管的操作方法是_______________________。
②测定前,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 molL-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液25. 50 mL,则测得无水MgBr2产品的纯度是________(以质量分数表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com