
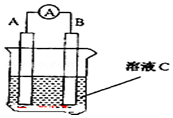
 如图原电池装置图:
如图原电池装置图:分析 根据电池反应式知,Cu失电子发生氧化反应,则作负极,不如Cu活泼的金属或导电的非金属作正极,含有铁离子的可溶性铁盐溶液为电解质溶液,根据转移电子与Cu的关系式计算消耗Cu的质量;根据转移电子与铁离子的关系计算反应速率.
解答 解:2Fe3++Cu═2Fe2++Cu2+,根据方程式可知,铜的化合价升高,失电子,应作为原电池的负极;3价铁离子化合价降低,得到电子,故电解质溶液可选用氯化铁;正极可选用惰性电极石墨(Pt亦可);又负极反应为Cu-2e-=Cu2+,根据电极反应式可知,消耗1mol铜,转移2mol电子,故转移0.1mol电子,消耗的铜为0.05mol,质量为0.05mol×64g/mol=3.2g,同时消耗Fe3+的物质的量为0.1mol,所以Fe3+浓度变化表示的该反应的速率为:$\frac{\frac{0.1mol}{2L}}{10min}$=0.005 mol/(L•min),
故答案为:铜;氯化铁溶液;3.2g;0.005 mol/(L•min).
点评 本题考查了原电池原理的分析判断,原电池原理和电极分析判断是解题关键,注意电极反应生成的离子在电解质溶液中的存在分析,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2FeCO3(s)+O2(g)=Fe2O3(s)+2CO2(g)△H=-130 KJ/mol | |
| B. | 4 FeCO3(s)+O2(g)=2Fe2O3(s)+4CO2(g)△H=+260 KJ/mol | |
| C. | 4 FeCO3(s)+O2(g)=2Fe2O3(s)+4CO2(g)△H=-260 KJ/mol | |
| D. | 4 FeCO3(s)+O2(g)=2Fe2O3(s)+4CO2(g)△H=+130 KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
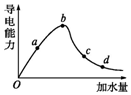 一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图曲线所示,请回答.
一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图曲线所示,请回答.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用物质A表示的平均反应速率为0.3mol/(L•s) | |
| B. | 用物质B表示的平均反应速率为0.6mol/(L•s) | |
| C. | 2 s时物质A的转化率为70% | |
| D. | 2 s时物质B的浓度为0.5mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 氧化镁与稀盐酸混合:MgO+2H+═Mg2++H2O | |
| C. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| D. | 稀盐酸滴在大理石上:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水鉴别甲酸、乙醛、乙酸 | |
| B. | 除去乙烷中少量的乙烯:光照条件下通入氢气 | |
| C. | 除去乙醇中少量的乙酸:加入足量的生石灰,过滤 | |
| D. | 用燃烧的方法鉴别乙醇、苯和四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2和CO2一样能够与NaOH溶液反应 | |
| B. | 硅的导电性能介于金属和绝缘体之间,是良好的半导体材料 | |
| C. | 硅酸是一种比碳酸还弱的酸 | |
| D. | 硅的化学性质不活泼,常温下不与任何物质反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实现无氰电镀 | B. | 研制可降解塑料 | C. | 使用无铅汽油 | D. | 使用无氟冰箱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com