
【题目】今有室温下四种溶液,有关叙述不正确的是( )
① | ② | ③ | ④ | |
浓度c/mol/L | 0.1 | 0.1 | 0.1 | 0.1 |
溶液 | 氨水 | CH3COONa溶液 | 醋酸 | 盐酸 |
A.在20 mL ①溶液中逐滴加入③溶液,溶液导电能力变化如下图
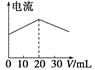
B.②、③两溶液等体积混合,离子浓度:2c(Na+)=c(CH3COO-)+c(CH3COOH)
C.①、④两溶液等体积混合,离子浓度:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.用④滴定①,滴定曲线如下图,可用酚酞作指示剂
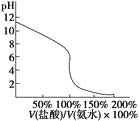
科目:高中化学 来源: 题型:
【题目】下列叙述或书写正确的是
A.![]()
![]() ,则相同条件下,
,则相同条件下,![]() 气体的能量大于1mol氢气和1mol氟气的能量之和
气体的能量大于1mol氢气和1mol氟气的能量之和
B.![]()
![]() ,则反应物的总键能小于生成物的总键能
,则反应物的总键能小于生成物的总键能
C.含![]() 的稀溶液与稀盐酸完全中和,放出
的稀溶液与稀盐酸完全中和,放出![]() 的热量,则表示该中和反应的热化学方程式为
的热量,则表示该中和反应的热化学方程式为![]()
![]()
D.![]() 、30MPa时,发生反应
、30MPa时,发生反应![]()
![]()
![]() 在此条件下将
在此条件下将![]() 和过量
和过量![]() 充分反应,放出热量
充分反应,放出热量![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的表示及说法正确的是
A.已知![]() 石墨,
石墨,![]() 金刚石,
金刚石,![]() ,则金刚石比石墨稳定
,则金刚石比石墨稳定
B.已知![]() ,则2L氟化氢气体分解成1L氢气和1L氟气吸收270kJ热量
,则2L氟化氢气体分解成1L氢气和1L氟气吸收270kJ热量
C.HCl和NaOH反应的中和热为![]() ,则
,则![]() 和
和![]() 反应的中和热
反应的中和热![]()
D.已知I2(g)+H2(g)==2HI(g) △H1;I2(s)+H2(s)==2HI(g) △H2 则![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯和其他无机原料合成化合物E,转化关系如图:
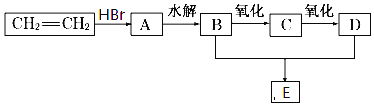
(1)写出下列物质的结构简式:B.______D.______E______
(2)写出有机物C与银氨溶液的反应方程:______
(3)![]() 的化学方程:______
的化学方程:______
(4)若把线路中转化关系中的HBr变成![]() 则E的结构简式______。
则E的结构简式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时0.1molNa2CO3与盐酸混合所得体积为1L的溶液中部分微粒与溶液pH值之间关系如图所示,下列叙述正确的是
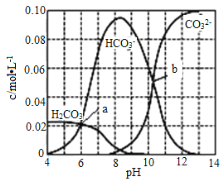
A.混合液随pH增大,![]() 先增大后减小
先增大后减小
B.b点时溶液中离子存在如下关系:2c(![]() )+c(
)+c(![]() )+c(OH-)=c(Na+)+c(H+)
)+c(OH-)=c(Na+)+c(H+)
C.H2CO3的一级电离常数Ka1约为10-6,Ka2的数量级为10-11
D.pH=7时,溶液中离子浓度大小顺序为:c(Na+)=c(Cl-)>c(![]() )>c(H+)=c(OH-)>c(
)>c(H+)=c(OH-)>c(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题小组合成了一种复合材料的基体M的结构简式为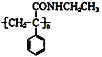 ,合成路线如下
,合成路线如下
![]()
已知:R—CN![]() R—COOH
R—COOH
请回答下列问题:
![]() 有机物C分子结构中含有的官能团有______________。
有机物C分子结构中含有的官能团有______________。
![]() 写出A的结构简式 _________________。
写出A的结构简式 _________________。
![]() 反应①、②的反应类型分别为 _______________、 ________________。
反应①、②的反应类型分别为 _______________、 ________________。
![]() 写出反应③的化学方程式 ________________。
写出反应③的化学方程式 ________________。
![]() 写出符合下列条件:①能使
写出符合下列条件:①能使![]() 溶液显紫色;②只有二个取代基;③与新制的
溶液显紫色;②只有二个取代基;③与新制的![]() 悬浊液混合加热,有砖红色沉淀生成;有机物B的一种同分异构体的结构简式 _____________。
悬浊液混合加热,有砖红色沉淀生成;有机物B的一种同分异构体的结构简式 _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水杨酸己酯分子式为C13H18O3,具有花果香味,用作化妆品香料的定香剂,也用作烟草香精。它的一种同分异构体A具有如下转化关系:
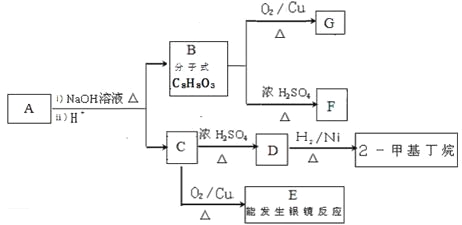
已知:
①C分子中有一个碳原子连接着4个不同的原子或原子团,且1 molC和足量金属Na反应能产生0.5 mol H2
②F中除了含有1个苯环外,还含有1个五元环
(1)写出B的结构简式___________________;写出G含有的官能团的名称_______________
(2)写出A和NaOH溶液反应的化学方程式_________________________________;
写出E发生银镜反应的化学方程式_______________________________________;
(3)B生成F的反应类型是________________;C生成D的反应类型是________________;
(4)化合物B有多种同分异构体,写出两种符合下列条件的同分异构体的结构简式:
_______________________________________________
a.属于芳香族化合物
b.酸性条件下能发生水解反应且其中一种产物的苯环上的一氯代物只有两种
c.1 mol该有机物最多可消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A的密度是相同状况下氢气密度的14倍,有机物A~E能发生如图所示一系列变化,则下列说法错误的是

A. A分子中所有原子均在同一平面内
B. A→B所用试剂为![]()
C. 分子式为![]() 的酯有3种
的酯有3种
D. 等物质的量的B、D分别与足量钠反应生成气体的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废旧电池材料的主要成分为钴酸锂(LiCoO2),还含有一定量的铁、铝、铜等元素的化合物,其回收工艺如图所示,最终可得到Co2O3和锂盐。
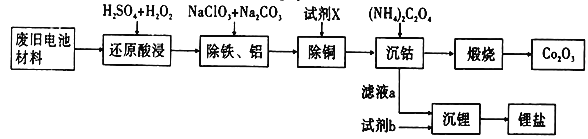
已知:CoC2O4·2H2O微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的C2O42-离子生成Co(C2O4)n2(n-1)-而溶解。
(1)“还原酸浸”过程中钴酸锂反应的离子方程式________________________________________;温度通常控制在40℃以下的原因是_______________________________________________。
(2)“除铝铁”过程的两种试剂的作用分别是____________________,______________________。
(3)“除铜”所用试剂X为H2S,试写出该反应的离子方程式______________________________。
(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如图所示:
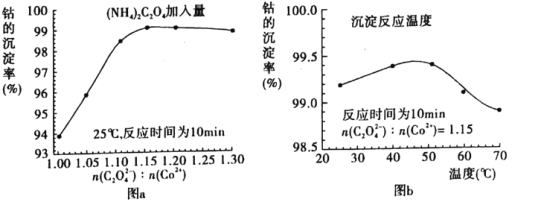
①随n(C2O42-):N(Co2+)比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因________________________________________________________________________。
②沉淀反应时间为10 min,温度在50℃以上时,随温度升高而钴的沉淀率下降的可能原因是_________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com