
【题目】根据表中信息,判断以下叙述正确的是

A. L2+与R2-的核外电子数相等
B. 单质与稀盐酸反应的速率为L<Q
C. M与T形成的化合物具有两性
D. 氢化物的沸点为H2T<H2R
【答案】C
【解析】主族元素中,元素最高正化合价与其族序数相等,元素最低负化合价=族序数-8,原子电子层数越多其原子半径越大,同一周期元素中,原子半径随着原子序数增大而减小,根据表中数据知,L、Q属于第IIA族元素,原子半径L>Q,则L是Mg、Q是Be元素;M为第IIIA族元素,M原子半径略小于Mg,则M是Al元素;R、T属于第VIA族元素,R原子半径大于T,则R是S元素、T为O元素,则:A.L2+是两个电子层,而R2-是三个电子层,所以电子数不相等,A错误;B.金属性越强,单质与稀盐酸反应的速率越快,L>Q,B错误;C.M与T形成的化合物是氧化铝,是两性氧化物,C正确;D.水分子间存在氢键,所以氢化物的沸点为H2T>H2R,D错误,答案选C。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+(aq)+SCN-(aq)![]() Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是
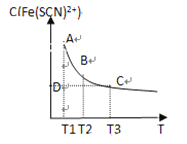
A. FeCl3(aq)与KSCN(aq)反应的热化学反应方程式为Fe3+(aq)+SCN—(aq)![]() Fe(SCN)2+(aq) ΔH >0
Fe(SCN)2+(aq) ΔH >0
B. 温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2
C. 反应处于D点时,一定有υ正>υ逆
D. A点与B点相比,A点的c(Fe3+)大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子核外电子的能量与运动状态的说法正确的是
A.在同一原子中,2p、3p、4p……能级的电子轨道数依次增多
B.在同一能级上运动的电子,其能量一定相同
C.在同一能级上运动的电子,其运动状态有可能相同
D.在同一原子中,1s、2s、3s、4s……能级的原子轨道的平均半径相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱金属钠及其化合物广泛应用于医药、工农业生产和化工领域。回答下列问题:
(1)碱金属的焰色反应及霓虹灯光、激光等现象与原子核外电子发生_________有关。电子排布式为1s22s22p63s23p54s2是_________(填元素符号)原子的_________态原子。
(2)钠形成的化合物均为离子化合物,原因是___________________________。
(3)钠的有机盐是一类重要的钠盐,如丙酸钠(CH3CH2COONa)和氨基乙酸钠(H2NCH2COONa)。
①CH3CH2COO中均为共价键,共价键类型有σ键和π键,σ键与π键的个数比为_________;H2NCH2COO中N原子的杂化轨道类型为_________,C原子的杂化轨道类型为_________。
②丙酸钠和氨基乙酸钠均能水解,水解产物有丙酸和氨基乙酸,二者部分数据如下表:
熔点/℃ | 沸点/℃ | 水溶解性 | |
丙酸 | 21.5 | 141.1 | 能与水混溶 |
氨基乙酸 | 186 | 234 | 易溶于水 |
由熔点数据可知,常温下丙酸为液体,而氨基乙酸为固体,主要原因是__________________,二者均易溶解于水,而相对分子质量与其相差不大的戊烷却难溶于水,原因是__________________。
(4)Na2O晶胞结构如图所示,其中钠为_________(选填“甲”或“乙”),其晶胞参数a=0.566 nm,则Na2O的密度为_________________g·cm3。(列式即可,不必计算出结果,NA =6.02×1023 mol1)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.同一原子中,轨道的能量高低:1s>2s>3s>4s
B.同一原子中,轨道的能量高低:3d<3p<3s
C.不同能级中含有的原子轨道数:s-2;p-6;d-10
D.M 层上所具有的原子轨道数共有 9 个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能大量共存的离子组是
A. NH4+、Mg2+、OH-、Cl- B. Ba2+、K+、SO42-、NO3-
C. Al3+、Cu2+、SO42-、Cl- D. Na+、Al3+、Cl-、AlO2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com