
| A. | 8.3 | B. | 8.7 | C. | 9.3 | D. | 9.7 |
分析 两种碱溶液混合,先计算出混合后溶液的c(OH-),再根据溶液的Kw计算出溶液的c(H+),然后求pH值.
解答 解:pH=8的NaOH溶液中c(OH-)=1×10-6mol/L,pH=10的NaOH溶液中c(OH-)=1×10-4mol/L,
混合后c(OH-)=$\frac{1{0}^{-6}+1{0}^{-4}}{2}$mol/L≈$\frac{1{0}^{-4}}{2}$mol/L,
则溶液中的c(H+)=$\frac{Kw}{c(O{H}^{-})}$=$\frac{1{0}^{-14}}{\frac{1{0}^{-4}}{2}}$mol/L=2.0×10-10mol/L,所以PH=10-lg2=9.7,故选D.
点评 本题考查两种碱溶液混合后的溶液氢离子浓度计算,题目难度不大,注意先计算溶液中c(OH-),再计算c(H+).


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
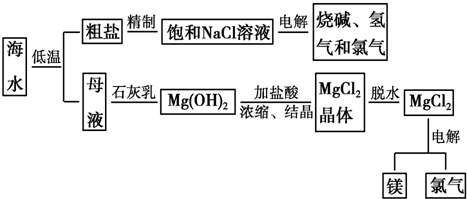
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
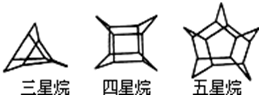
| A. | 三星烷与丙苯互为同分异构体 | B. | 五星烷的二氯取代物有8种 | ||
| C. | 六星烷的化学式为C18H24 | D. | 七星烷的一硝基取代物有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中共有18个纵行,18个族,其中主族数为7个 | |
| B. | 周期表中,元素族序数等于该族元素原子的最外层电子数 | |
| C. | 周期表中,第四周期有32种元素,包括镧系元素 | |
| D. | 周期表中,ⅠA族对应第1纵行,只有一种非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| B. | 1.4g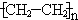 中含有的碳原子数为0.2NA 中含有的碳原子数为0.2NA | |
| C. | 1 mol苯分子中含有C=C双键数为3NA | |
| D. | 乙烷和丙烯的物质的量共1mol,完全燃烧生成水分子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铝属于合金的一种,有着广泛的用途 | |
| B. | 切过肉的菜刀比切过蔬菜的菜刀更耐腐蚀 | |
| C. | 铁是地壳中含量最高的金属,也是世界上年产量最高的金属 | |
| D. | 制作沉重的机床底座时应努力实现用纯铁替代钢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
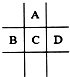 有A、B、C、D四种短周期元素,它们在周期表中的位置如图所示,已知四种元素核外共有56个电子,则以下说法不正确的是( )
有A、B、C、D四种短周期元素,它们在周期表中的位置如图所示,已知四种元素核外共有56个电子,则以下说法不正确的是( )| A. | A的氢化物在常温下通常为液态 | |
| B. | A的单质与C的某种化合物之间可能发生置换反应 | |
| C. | B、C、D的含氧酸酸性依次增强 | |
| D. | D的单质是制备漂白剂的重要原料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com