
【题目】下列对化学用语的理解正确的是( )
A.乙烯的结构简式:CH2CH2
B.电子式![]() 可以表示氢氧根离子,也可以表示羟基
可以表示氢氧根离子,也可以表示羟基
C.比例模型![]() 可以表示甲烷分子,也可以表示四氯化碳分子
可以表示甲烷分子,也可以表示四氯化碳分子
D.结构示意图![]() 可以表示35Cl-,也可以表示37Cl-
可以表示35Cl-,也可以表示37Cl-
科目:高中化学 来源: 题型:
【题目】(1)常温下,向100mL0.01mol/LHA的溶液中逐滴加入0.02mol/LMOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。
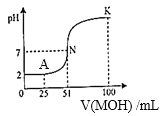
①由图中信息可知HA为______酸(填“强”或“弱”)。
②A点时,溶液中c(H+)、c(M+)、c(A-)由大到小的顺序是_____________;
③K点时,溶液中c(H+)+c(M+)-c(OH-)=_________mol/L。
(2)20℃时,在c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol/L的H2C2O4、NaOH混合溶液中,H2C2O4、HC2O4-、C2O42-的物质的量分数δ随溶液pH变化的关系如图所示。

①Q点:c(H2C2O4)______c(HC2O4-)(填“>”、“<”或“=”)
②该温度下HC2O4-的电离常数K=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A、B、C三个装置中的烧杯分别盛有足量的CuCl2溶液。
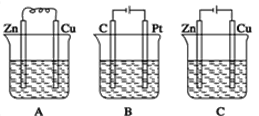
(1)A、B、C三个装置中属于原电池的是___(填标号)。
(2)A池中Zn是___极,电极反应式为___;A中总反应的离子方程式___。
(3)B池中总反应的方程式为___。
(4)C池中Zn是___极,发生___反应,电极反应式为___;反应过程中,CuCl2溶液浓度___(填“变大”“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】平板电视显示屏生产过程中产生大量的废玻璃(含SiO2、Fe2O3、CeO2、FeO等物质)。某小组以此废玻璃为原料,设计如下工艺流程对资源进行回收,得到Ce(OH)4。
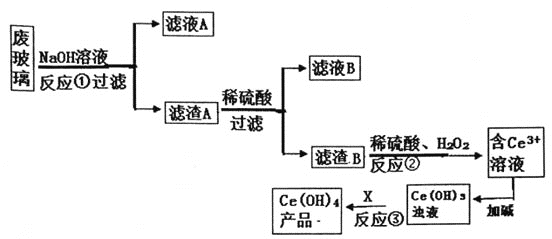
己知:CeO2不溶于强酸或强碱;Ce3+易水解,酸性条件下,Ce4+有强氧化性。
(1)反应①的离子方程式________________________。
(2)反应②的离子方程武是_____________________________。
(3)为了得到较纯的Ce3+溶液,反应②之前要进行的操作是______
(4)反应③需要加入的试剂X可以是______________。
(5)用滴定法测定制得的Ce(OH)4产品纯度。
![]()
用FeSO4溶液滴定用_____做指示剂,滴定终点的现象_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,向20mL0.1mol·L-1MOH溶液中滴加0.1mol·L-1CH3COOH溶液,所得溶液的pH及导电能力变化如图所示。下列叙述正确的是( )
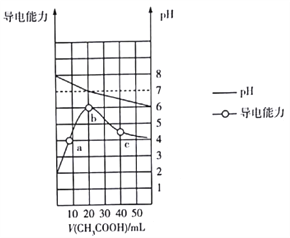
A. MOH是强电解质 B. b点对应的盐不水解
C. 水的离子积Kw:b>c>a D. c点溶液中c(CH3COO-)>c(M+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是
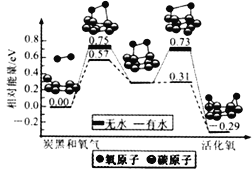
A. 氧分子的活化包括O-O键的断裂与C-O键的生成
B. 每活化一个氧分子放出0.29eV的能量
C. 水可使氧分子活化反应的活化能降低0.42eV
D. 炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有K+、Na+、Fe3+、Fe2+、SO42-、CO32-、I-、Cl-中的一种或多种,进行如图所示的实验,下列说法正确的是 ( )

A. 溶液X中有Fe3+、SO42-
B. 溶液X中有Fe2+、I-可能有SO42-、Cl-
C. 溶液X中有I-、Cl-,无CO32-
D. 溶液X中有I-,Fe2+和Fe3+两种离子中至少有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定法是化学上常用的定量分析的方法,滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等。
Ⅰ.甲化学兴趣小组取20.00 mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用0.200 0 mol·L-1的标准NaOH溶液进行滴定,重复上述滴定操作3次,并记录数据。
(1)滴定时边滴边摇动锥形瓶,眼睛应观察________。(填标号)
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)判断滴定终点的现象是_________________。
(3)根据表中数据,计算待测盐酸溶液的浓度为________ mol·L-1。
滴定次数 | 待测液体积(mL) | 标准NaOH溶液读数记录(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 4.00 | 24.00 |
第三次 | 20.00 | 2.00 | 24.10 |
Ⅱ.乙化学兴趣小组利用氧化还原反应滴定,测定了某工厂废水中游离态氯的含量。实验如下:
①取水样10.0 mL于锥形瓶中,加入10.0 mL的KI溶液(足量),滴入指示剂2~3滴。
②将自己配制的0.01 mol·L-1标准Na2S2O3溶液装入滴定管中,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,试回答下列问题:
(4)步骤①发生的化学反应方程式为__________;加入的指示剂是____________。
(5)步骤②应使用________式滴定管。
(6)氯的所测浓度比实际浓度会偏大,造成误差的原因可能是________。(填标号)
A.配制标准Na2S2O3溶液定容时,加水超过刻度线
B.锥形瓶水洗后直接装待测水样
C.装标准Na2S2O3溶液的滴定管水洗后没有润洗
D.滴定到达终点时,俯视读出滴定管读数
E.滴定前尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备己二酸的原理为:3![]() +8KMnO4═3KOOC(CH2)4COOK+8MnO2↓+2KOH+5H2O
+8KMnO4═3KOOC(CH2)4COOK+8MnO2↓+2KOH+5H2O
主要实验装置和步骤如下:
①在如图装置中加入5mL10%氢氧化钠溶液和50mL水,搅拌使其溶解,然后加入6.3g高锰酸钾,小心预热溶液到40℃。
②从恒压漏斗中缓慢滴加1.4mL环己醇,控制滴速,使反应温度维持在45℃左右,反应20min后,再在沸水浴上加热5min促使反应完全并使MnO2沉淀凝聚。
③加入适量亚硫酸氢钠固体除去多余高锰酸钾。
④通过___操作,得到沉淀和滤液,洗涤沉淀2~3次,将洗涤液合并入滤液。
⑤加热浓缩使溶液体积减少至10mL左右,趁热小心加入浓硫酸,使溶液呈强酸性(调节pH=1~2),冷却结晶、抽滤、洗涤、干燥,得己二酸白色晶体1.5g。

已知:己二酸的电离平衡常数:Ka1=3.8×10﹣5,Ka2=3.9×10-6;相对分子质量为146;其在水中溶解度如下表
温度(℃) | 15 | 34 | 50 | 70 | 87 | 100 |
己二酸溶解度(g) | 1.44 | 3.08 | 8.46 | 34.1 | 94.8 | 100 |
(1)步骤②中缓慢滴加环己醇的原因是___。
(2)步骤④划线部分操作是___、在第④、⑤布中均要求洗涤沉淀,所用洗涤液依次为___、___。
(3)步骤⑤加入浓硫酸调节pH成强酸性的原因是___。
(4)己二酸产品的纯度可用酸碱滴定法测定。取样试样ag(准确至0.0001g),置于250mL锥形瓶中,加入50mL除去CO2的热蒸馏水,摇动使试样完全溶解,冷却至室温,滴加3滴酚酞溶液,用0.1000molL-1的NaOH标准溶液滴定至微红色即为终点,消耗NaOH标准溶液体积bmL
①下列说法正确的是___。
A.称取己二酸样品质量时,先将锥形瓶放在电子天平秤盘的中央,显示数字稳定后按“去皮”键(归零键),再缓慢加样品至所需样品的质量时,记录称取样品的质量
B.摇瓶时,应微动腕关节,使溶液向一个方向做圆周运动,但是勿使瓶口接触滴定管,溶液也不得溅出
C.滴定时左手轻轻挤压玻璃球让液体自行呈线状流下
D.滴定结束后稍停1﹣2分钟,等待滴定管内壁挂有的溶液完全流下时再读取刻度数
E.记录测定结果时,滴定前仰视刻度线,滴定到达终点时又俯视刻度线,将导致滴定结果偏高
②计算己二酸纯度的表达式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com