
【题目】现有A、B、C三种金属单质和甲、乙、丙三种气体,及物质D、E、F、G、H,它们之间能发生如图所示变化(图中有些反应的产物和反应的条件没有全部标出)。请回答下列问题:

(1)写出指定物质的化学式:D____________、G____________、丙____________。
(2)上述反应中既是化合反应,又是氧化还原反应的是____________(填序号)。
(3)写出反应①的离子方程式:____________________________________。
(4)写出反应⑤的离子方程式________________________。用于检验溶液G中金属阳离子的试剂是____________。
【答案】![]()
![]()
![]() ②⑤
②⑤ ![]()
![]()
![]() 溶液
溶液
【解析】
金属单质A的焰色反应为黄色,A为![]() ,
,![]() 与水反应生成
与水反应生成![]() 和
和![]() ,气体甲为
,气体甲为![]() ,溶液D为
,溶液D为![]() ,
,![]() 与金属单质
与金属单质![]() 反应生成
反应生成![]() 和
和![]() ,B为
,B为![]() ,黄绿色气体是
,黄绿色气体是![]() ,
,![]() 与
与![]() 反应生成
反应生成![]() 气体,气体丙为
气体,气体丙为![]() ,
,![]() 加水得到溶液E为盐酸,盐酸与金属单质
加水得到溶液E为盐酸,盐酸与金属单质![]() 反应,生成
反应,生成![]() 和
和![]() ,金属C为
,金属C为![]() ,溶液F为
,溶液F为![]() ,
,![]() 与
与![]() 反应,生成
反应,生成![]() ,溶液G为
,溶液G为![]() ,
,![]() 与
与![]() 反应生成红褐色沉淀
反应生成红褐色沉淀![]() 和
和![]() ,H为
,H为![]() 。
。
(1)根据分析可知,D为![]() 、G为
、G为![]() 、丙为
、丙为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;![]() ;
;
(2)化合反应是两种或两种以上的物质反应生成一种新物质的反应,氧化还原反应是反应前后有元素化合价改变的反应,所以②⑤是既是化合反应,又是氧化还原反应,故答案为:②⑤;
(3)反应①是![]() 与水反应生成
与水反应生成![]() 和
和![]() ,其离子反应方程式:
,其离子反应方程式:![]() ↑,故答案为:
↑,故答案为:![]() ↑;
↑;
(4)反应⑤是![]() 与
与![]() 应生成
应生成![]() ,其离子反应方程式:
,其离子反应方程式:![]() ,溶液G为
,溶液G为![]() ,阳离子是
,阳离子是![]() ,滴加
,滴加![]() 溶液,溶液变为血红色,说明有
溶液,溶液变为血红色,说明有![]() ,故答案为:
,故答案为:![]() ;
;![]() 溶液。
溶液。


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池可长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时负极反应为Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为Fe(OH)3-3e-+5OH-=FeO![]() +4H2O
+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.一定条件下,反应室(容积恒定为2L)中有反应:A(g)+2B(g)![]() C(g)。
C(g)。
(1)能说明上述反应达到平衡状态的是________(填字母,下同)。
A.反应中A与B的物质的量浓度之比为1∶2 B.混合气体总物质的量不再变化
C.混合气体的密度不随时间的变化而变化 D.2v正(A)=v逆(B)
(2)1molA(g)与2molB(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:

①p1________p2(填“<”、“>”或“=”,下同),正反应的ΔH________0。
②下列措施中一定能使![]() 增大的是________。
增大的是________。
A.升高温度B.恒温恒容再充入A
C.恒温恒容再充入BD.恒温恒容再充入1molC
(3)100℃时将1molA和2molB通入反应室,保持温度不变,10min末C(g)的浓度为0.05mol·L-1,则10min末B的转化率为_____,此时v正_____v逆(填“<”、“>”或“=”)。
II.一定温度下,在容积为VL的密闭容器中进行反应:aN(g)![]() bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
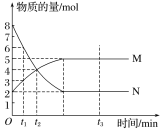
(1)此反应的化学方程式中![]() =____________。
=____________。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为____________。
(3)下列叙述能说明上述反应达到平衡状态的是____________(填字母)。
A.反应中M与N的物质的量之比为1∶1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗amolN,同时生成bmolM
E.混合气体的压强不随时间的变化而变化
F.混合气体的平均相对分子质量不随时间的变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。
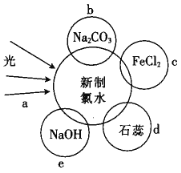
(1)氯水中含有的粒子有![]() 、
、![]() 、______、
、______、![]() 、
、![]() 、______、
、______、![]() 七种。
七种。
(2)久置的氯水变为_____________,原因是___________________________(用化学反应方程式表示)。
(3)b过程中的离子方程式是_______________________。
(4)e过程中所发生的主要反应的化学方程式为____________________________。
(5)能证明氯水具有漂白性的是______________________(填“a”“b”“c”或“d”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH4-CO2催化重整反应为:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)ΔH。
2CO(g)+2H2(g)ΔH。
已知:C(s)+2H2(g)=CH4(g)ΔH=-75kJ·mol1
C(s)+O2(g)=CO2(g)ΔH=-394kJ·mol1
C(s)+![]() O2(g)=CO(g)ΔH=-111kJ·mol1
O2(g)=CO(g)ΔH=-111kJ·mol1
该催化重整反应的ΔH=________kJ·mol1。有利于提高CH4平衡转化率的条件是____(填标号)。
A.高温低压B.低温高压C.高温高压D.低温低压
某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为___________________________。
素材1:研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。总反应为:2Li+2H2O===2LiOH+H2↑。根据以上素材回答下列问题:
(2)该电池的负极是________,负极反应式是_____________________________。
(3)正极现象是_______________________________________________。
(4)放电时OH-向_____________(填“正极”或“负极”)移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是![]() ,含
,含![]() 、
、![]() 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下:
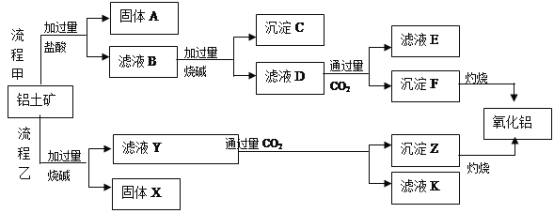
请回答下列问题:
(1)流程乙加入烧碱后的离子方程式为_________________________________________.
(2)固体A的应用_________________________________________.(两点)
(3)滤液D与少量CO2反应的离子方程式为__________________________________,
向该滤液K中加入足量石灰水的离子方程式是________
(4)流程乙制氧化铝的优点是所用的试剂较经济,缺点是__________________________
(5)已知298K时,![]() 的溶度积常数
的溶度积常数![]() =10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的pH最小为_______.
=10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的pH最小为_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家开发出了多种太阳能电池,除晶体硅太阳能电池外,还有GaAs太阳能电池、铜铟镓硒薄膜太阳能电池等。
(1)基态Ga原子的电子排布式为___。
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因___。
(3)与SeO3互为等电子体的两种阴离子___(写化学式)。
(4)AsF3是极性分子,理由是___。
(5)金刚砂(SiC)晶胞如图所示:
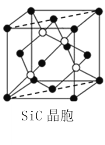
①金刚砂中硅原子的杂化轨道类型为___,沿晶胞图中虚线方向的切面图为___(填标号)。
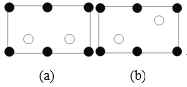
②若晶胞参数为apm,阿伏加德罗常数为NA,则金刚砂的密度为___g·cm-3(列出表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O。下列说法正确的是
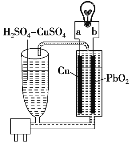
A.b为负极,a为正极
B.该电池工作时,内电路中电子由电极a流向电极b
C.b极的电极反应为PbO2 + 4H++4e-= Pb2++2H2O
D.调节电解质溶液的方法是补充H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在体积均为20mL、浓度均为0.1mol/L的HX溶液、HY溶液中分别滴加0.1mol/L的NaOH溶液,反应后溶液中水电离的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加NaOH溶液体积的关系如图所示。下列推断正确的是
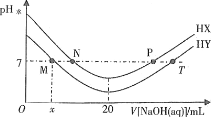
A.HX的电离方程式为HX=H++X-
B.T点时c(Na+)=c(Y-)>c(H+)=c(OH-)
C.常温下用蒸馏水分别稀释N、P点溶液,pH都一定降低
D.常温下,HY的电离常数![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com