
����Ŀ��ֱ���ŷź�SO2���������γ����꣬Σ��������ij��ѧʵ��С����������й�SO2���ʵ�̽����� 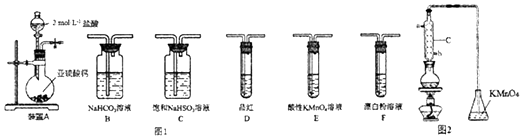
��1��װ��A�з�Ӧ�����ӷ���ʽΪ ��
��2��ѡ��ͼ1����װ�ú�ҩƷ̽��������������������ǿ����
�ټ�ͬѧ��Ϊ����A��C��F��β������˳������װ�ÿ���֤��������ʹη��������ǿ������ͬѧ��Ϊ�÷������������������� ��
�ڱ�ͬѧ��Ƶĺ���ʵ������Ϊ������A��C��β������������ĸ��˳������װ�ã�����װ��C�������� �� ֤�������������ǿ�ڴ���������Ե�ʵ�������� ��
��3��������ͼ2 ��װ��A���Һ��SO2�ĺ�������ȡ10.00mL��Һ��Բ����ƿ�У�����ʹSO2ȫ����������20.00mL 0.1000mol/L��KMnO4����Һ���գ���ַ�Ӧ������0.200Omol/L��KI��Һ�ζ�������KMnO4 �� ����KI��Һ25.00mL��
����֪��5SO2+2MnO4��+2H2O=2Mn2++5SO42��+4H+ �� 10I��+2MnO4��+16H+=2Mn2++5I2+8H2O��
�ٸ�װ��������C������Ϊ �� ˮͨ��C�Ľ���Ϊ ��
�ڲ�Һ��SO2�ĺ���Ϊmol/L��
���𰸡�
��1��2H++CaSO3=Ca2++H2O+SO2��
��2����������ͨ����������Һ������������ԭ��Ӧ����֤��ǿ���Ʊ������ԭ����B��E��D��F����ȥHCl��������Ӱ������ʵ���ã�װ��D��Ʒ�첻��ɫ��F�г��ְ�ɫ����
��3�����������ܣ�b��0.25
���������⣺��1��װ��A��������������Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ����������ӷ���ʽΪ��2H++CaSO3=Ca2++H2O+SO2�������Դ��ǣ�2H++CaSO3=Ca2++H2O+SO2������2���ٰ���A��C��F˳������װ�ã����б��͵����������Ƴ�ȥHCl����������ͨ����������Һ������������ԭ��Ӧ������֤��ǿ���Ʊ������ԭ��������֤��������ʹ����������ǿ����
���Դ��ǣ���������ͨ����������Һ������������ԭ��Ӧ����֤��ǿ���Ʊ������ԭ�����ڴ��������ǿ�����ԡ�����������л�ԭ�ԣ��������ö���������������ֱ�ӷ�Ӧ�ж�������������������ǿ��������֤���������Ա�̼��ǿ���ٽ��̼�����Ա�HClOǿ�����жϣ�Aװ���Ʊ������������������ӷ����Ʊ��Ķ��������л���HCl���ñ��͵����������Ƴ�ȥHCl����ͨ��̼��������Һ��������֤���������Ա�̼��ǿ�������Ը��������Һ������ȥ������̼�еĶ���������Ʒ����Һ���������̼�ж��������Ƿ��������ͨ��F�У���װ������˳��ΪA��C��B��E��D��F������װ��C�������dz�ȥHCl���壬D��Ʒ�첻��ɫ��F�г��ְ�ɫ��������֤�������������ǿ�ڴ����ᣬ
���Դ��ǣ�B��E��D��F����ȥHCl��������Ӱ������ʵ���ã�װ��D��Ʒ�첻��ɫ��F�г��ְ�ɫ��������3���ٸ�װ��������C������Ϊ���������ܣ���ȡ����ԭ��ͨ������ˮ�������������ܽ�ˮ��Ϊb��
���Դ��ǣ����������ܣ�b������10I��+2MnO4��+16H+=2Mn2++5I2+8H2O���������KMnO4���ʵ���Ϊ ![]() ��0.200Omol/L��0.025L=0.001mol��
��0.200Omol/L��0.025L=0.001mol��
�������Һ��SO2��Ӧ��KMnO4���ʵ���Ϊ0.02L��0.1000mol/L��0.001mol=0.001mol��
��5SO2+2MnO4��+2H2O=2Mn2++5SO42��+4H+ �� ���Һ��SO2����Ϊ0.001mol�� ![]() =0.0025mol�����Բ�Һ��SO2�ĺ���Ϊ=
=0.0025mol�����Բ�Һ��SO2�ĺ���Ϊ= ![]() =0.25mol/L��
=0.25mol/L��
���Դ��ǣ�0.25��


 �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��˫�������ṹ��ʽ��ͼ��ʾ ![]() �������ڽ���ѪҺ�еĵ��̴��������ʺϳ���·��ͼ��ʾ��
�������ڽ���ѪҺ�еĵ��̴��������ʺϳ���·��ͼ��ʾ��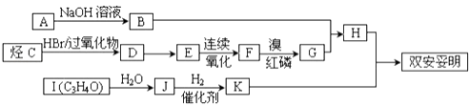
��֪���� ![]()
��RCH�TCH2 ![]() RCH2CH2Br
RCH2CH2Br
����֪��C���ܶ���ͬ��ͬѹ��H2�ܶȵ�28������֧����һ������I�ܷ���������Ӧ��1mol I��C3H4O������2mol H2�����ӳɷ�Ӧ��K�Ľṹ���жԳ��ԣ��Իش��������⣺
��1��д��˫�������ķ���ʽ ��
��2��C�Ľṹ��ʽΪ��H�Ľṹ��ʽΪ ��
��3����ӦD��E�ķ�Ӧ������ �� ��ӦI��J�������� ��
��4����Ӧ��H+K��˫���������Ļ�ѧ����ʽΪ ��
��5����������3��������H��ͬ���칹�����֣�����FeCl3��Һ��ɫ���ڱ�����ֻ������ȡ��������1mol�������������3mol NaOH��������ԭ�ӹ������ֲ�ͬ����������д�ṹ��ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A. ������Ԫ�صĻ�����һ����������
B. ������һ����ͬ�ַ��ӹ���
C. ��һ��Ԫ�ص�����һ���ǵ���
D. ��ͬ�ַ��ӹ��ɵ�����һ���Ǵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��O2��g��+2H2��g��=2H2O��g����H=��483.6kJmol��1
C��s��ʯī��+O2��g��=CO2��g����H=��393.5kJmol��1
CO2��g��+C��s��ʯī��=2CO��g����H=+172.5kJmol��1
��1����д��CO��ˮ������Ӧ���Ȼ�ѧ����ʽ
��2����һ���Ϊ10L���ܱ������У�ͨ��һ������CO��ˮ��������850��ʱ������Ӧ��������CO��ˮ����Ũ�ȱ仯��ͼ����0��4min��ƽ����Ӧ����v��CO��= �� ������ʱ��ƽ�ⳣ��K= �� 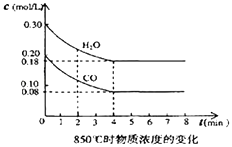
ʱ��/min | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
��3��t�棨����850�棩ʱ������ͬ�����з���������Ӧ�������ڸ����ʵ�Ũ�ȱ仯���ұ���
�ٱ���3min��4min֮�䷴Ӧ����״̬��c1��ֵ0.08mol/L ������ڡ�С�ڻ���ڣ���
�ڷ�Ӧ��4min��5min�䣬ƽ�����淽���ƶ������������µ�ԭ��������ĸ��������5min��6min֮����ֵ�����仯�����ܵ�ԭ���� �� ������ĸ��
a������ˮ���� b�������¶� c��ʹ�ô��� d����������Ũ�ȣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ṹΪ����CH��CH��CH��CH��CH��CH��CH��CH�����ĸ߷��ӻ������õ������������䵼�����������ߡ������߷��ӻ�����ĵ�����
A.��ȲB.��ϩC.��ϩD.1,3������ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϵIJ������ݡ����ø�Ũ��������480 mL�� 1 mol/L��ϡ���ᡣ�ɹ�ѡ�õ������У�����ƿ���ձ��۲�������ҩ�ע���Ͳ

��ش��������⣺
��1����Ũ��������ʵ���Ũ��Ϊ____________ mol/L��
��2������ϡ����ʱ�����������в���Ҫ��������____________������ţ�����ȱ�ٵ�������______________________________ (��д��������)��
��3�������㣬����480mL��1mol/L��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ______ mL����ȡŨ�������õ���Ͳ�Ĺ����________��
(�����й����ѡ�ã� 10 mL���� 25 mL���� 50 mL����100 mL)
��4���������Ƶ�ϡ������вⶨ��������Ũ�ȴ���1mol/L�����ƹ��������и�������������������ԭ����____________��
A������ʱ����������ƿ�̶��߽��ж���
B�����ձ��н�Ũ�������ϡ�ͺ�����ת������ƿ��
C��ת����Һʱ��������������Һ��������ƿ����
D������ƿ������ˮϴ�Ӻ�δ���������������ˮ
E������ҡ�Ⱥ���Һ����ڿ̶��ߣ��ټ�����ˮ���̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ�
A. Ԫ�صĵ��ʿ���������ԭ����Ԫ�صĻ��������Ƶ�
B. �õ���Խ������������������Ծ�Խǿ
C. ������ֻ�ܵõ����ӱ���ԭ��ֻ����������
D. ���и�Ԫ�صĻ����һ������ǿ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�CH4��H2O��g��������Ӧ��CH4��g��+H2O��g��CO��g��+3H2��g������ʼ ![]() =Z���ں�ѹ�£�ƽ��ʱCH4����������գ�CH4����Z��T���¶ȣ��Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
=Z���ں�ѹ�£�ƽ��ʱCH4����������գ�CH4����Z��T���¶ȣ��Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� �� 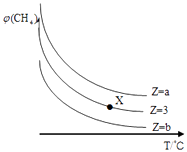
A.�÷�Ӧ���ʱ��H��0
B.ͼ��Z�Ĵ�СΪb��3��a
C.ͼ��X���Ӧ��ƽ�������� ![]() =3
=3
D.�¶Ȳ���ʱ��ͼ��X���Ӧ��ƽ���ڼ�ѹ��գ�CH4������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ù���NaOH�������ʵ���Ũ����Һʱ�����в����ᵼ����ҺŨ��ƫ�͵��ǣ�
A. ���ձ����ܽ�ʱ��������Һ�彦��
B. ��Ʒ�к�������Na2O����
C. ����ƿʹ��ǰ��NaOH��Һ��ϴ
D. ����ʱ��������ƿ�̶���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com