
����Ŀ����������һ�������ĩ�����п��ܺ��������������ʣ�![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ����֪
����֪![]() ������ˮ��
������ˮ��![]() ��Һ����ɫ���ֽ�������ʵ�飺
��Һ����ɫ���ֽ�������ʵ�飺
������ˮ����ɫ��Һ��������Һ�м���![]() ��Һ���ɰ�ɫ�������ټ�����ʱ������ʧ��
��Һ���ɰ�ɫ�������ټ�����ʱ������ʧ��
��������ʵ�������ƶϣ�
��1��һ�������ڵ������ǣ���д��ѧʽ��_________________________��
��2��һ�����ڵ������ǣ���д��ѧʽ��_________________________��
��3�����ܴ��ڵ������ǣ���д��ѧʽ��_________________________��
��4��������ܴ��ڵ����������Լ�����Ϊ��_________________________��
����5�����ǻ��õļ����Ԫ�أ��Ƽ��仯�������������������й㷺��Ӧ�á��ƼغϽ���ں˷�Ӧ���������Ƚ���Һ��![]() �ƼغϽ�����
�ƼغϽ�����![]() ˮ����
ˮ����![]() ������ȷ������-�غϽ����ɣ���
������ȷ������-�غϽ����ɣ���![]() ����ʽ��ʾ����__________�����������Һ�������Ϊ
����ʽ��ʾ����__________�����������Һ�������Ϊ![]() ����
����![]() ��Һ�����ʵ���Ũ��Ϊ___________________��
��Һ�����ʵ���Ũ��Ϊ___________________��
���𰸡�CaCO3��Na2SO4��CuSO4 Na2CO3 NaCl ϡ���ᡢ��������Һ NaK2 0.2mol/L
��������
�����ɢ�����ˮ����ɫ��Һ����֪һ������CuSO4��CaCO3���ɢ�����Һ�м���BaCl2��Һ���ɰ�ɫ�������ټ�����ʱ������ʧ����֪��ɫ����Ϊ̼�ᱵ����һ����Na2CO3������Na2SO4������ȷ���Ƿ�NaCl���Դ�����𣻣�II�����ݷ�����Ӧ��2Na+2H2O=2NaOH+H2����2K+2H2O=2KOH+H2��������������������������з��̼���Na��K���ʵ���������![]() ����ɵá�
����ɵá�
�ɢ�����ˮ����ɫ��Һ����֪һ������CuSO4��CaCO3���ɢ�����Һ�м���BaCl2��Һ���ɰ�ɫ�������ټ�����ʱ������ʧ����֪��ɫ����Ϊ̼�ᱵ����һ����Na2CO3������Na2SO4������ȷ���Ƿ�NaCl��
��1��һ�������ڵ�������CaCO3��Na2SO4��CuSO4���ʴ�Ϊ��CaCO3��Na2SO4��CuSO4��
��2��һ�����ڵ�������Na2CO3���ʴ�Ϊ��Na2CO3��
��3�����ܴ��ڵ�������NaCl���ʴ�Ϊ��NaCl��
��4���������ӵļ��鷽����֪��������ܴ��ڵ����������Լ�Ϊϡ���ᡢ��������Һ���ʴ�Ϊ��ϡ���ᡢ��������Һ��
��5�����ơ��ص����ʵ����ֱ�Ϊamol��bmol����

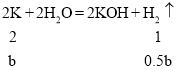
0.5a+0.5b=0.15��23a+39b=10.1������ɵã�a=0.10��b=0.20��n��Na����n��K��=1��2������-�غϽ�ѧʽΪNaK2��c(NaOH)=![]() ���ʴ�Ϊ��NaK2��0.2mol/L��
���ʴ�Ϊ��NaK2��0.2mol/L��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£����ܱ������г�������ʵ�����NO��CO��������Ӧ��2NO(g)+2CO(g)![]() N2(g)+2CO2(g)����������ѧ��Ӧ�ﵽƽ��ʱ������������ȷ���ǣ� ��
N2(g)+2CO2(g)����������ѧ��Ӧ�ﵽƽ��ʱ������������ȷ���ǣ� ��
A.CO2��CO�����ʵ���һ�����
B.NO��CO2�����ʵ���һ�����
C.��Ӧ���ת���ʴﵽ�˸������µ������
D.ƽ��ʱ�����������ʵ���һ�����ڷ�Ӧ��ʼǰ�����������ʵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β���е��к�������Ҫ��NO��̼�⻯���PCO��ijУͬѧ���ʵ�齫ģ������β��ת��Ϊ�����塣�ش��������⣻
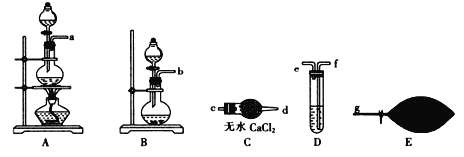
(1) Ϊ������ģ��β��������ͬѧ����ͼ��ʾװ�÷ֱ��Ʊ�NO����ϩ��CO�������塣
�� ��ʵ��������װ��A��ȡNO����Һ©����ʢ�ŵ���_______(���Լ�����)��
�� ��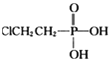 (��ϩ��)��NaOH��Һ����װ��B��ȡ��ϩ����Ӧ������ϩ�Ļ�ѧ����ʽΪ(��֪��ת��ΪNa3 PO4)_______________________��
(��ϩ��)��NaOH��Һ����װ��B��ȡ��ϩ����Ӧ������ϩ�Ļ�ѧ����ʽΪ(��֪��ת��ΪNa3 PO4)_______________________��
�� ��H2C2O4��Ũ������ȡCO�Ļ�ѧ����ʽ��H2C2O4 ![]() CO�� + CO2 ��+ H2O����Ȼ������ᴿ��ѡ����ͼװ��Ԥ��һ�����﴿����CO�����ӿ����ӵ�˳��Ϊ(������������)___________��g������װ��C����Ҫ������������________��װ��D��ʢ�ŵ�ҩƷ��_______��
CO�� + CO2 ��+ H2O����Ȼ������ᴿ��ѡ����ͼװ��Ԥ��һ�����﴿����CO�����ӿ����ӵ�˳��Ϊ(������������)___________��g������װ��C����Ҫ������������________��װ��D��ʢ�ŵ�ҩƷ��_______��
(2) ����ͬѧ�������Ƶõ�������������ʵ���������γ�ģ��β��(NO��CO��C2 H4������)������ͼ��ʾװ�ý���β��ת�������顣
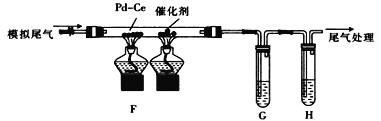
�� Ϊ�������Ӧ����������Ƿ���CO2���ɺ���ϩ�IJ�����G��H��ʢ�ŵ��Լ�������_______(����)��
a. NaOH��Һ�� b. ����KMnO4��Һ c. ����ʯ��ˮ�� d. Br2��CCl4��Һ
�� ͨ��ģ��β����ǰ�����Ƚ��������ȵ���Ӧ������¶ȣ���Ŀ����__________________��д������CO��NO��ȫת��Ϊ������Ļ�ѧ����ʽ��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ѧ��Ӧ����Fe(s)��CO2(g)![]() FeO(s)��CO(g)����ƽ�ⳣ��ΪK1����ѧ��Ӧ����Fe(s)��H2O(g)
FeO(s)��CO(g)����ƽ�ⳣ��ΪK1����ѧ��Ӧ����Fe(s)��H2O(g)![]() FeO(s)��H2(g)����ƽ�ⳣ��ΪK2�����¶�973 K��
FeO(s)��H2(g)����ƽ�ⳣ��ΪK2�����¶�973 K��
1173 K����£�K1��K2��ֵ�ֱ����£�
�¶� | K1 | K2 |
973 K | 1.47 | 2.38 |
1173 K | 2.15 | 1.67 |
(1)ͨ�������е���ֵ�����ƶϣ���Ӧ����________(��������������������)��Ӧ��
(2)���з�Ӧ����CO2(g)��H2(g)![]() CO(g)��H2O(g)������д���÷�Ӧ��ƽ�ⳣ��K3����ѧ����ʽ��K3��_________��
CO(g)��H2O(g)������д���÷�Ӧ��ƽ�ⳣ��K3����ѧ����ʽ��K3��_________��
(3)���жϷ�Ӧ���Ѵ�ƽ��״̬����_________��
A��������ѹǿ����
B�����������c(CO)����
C��v��(H2)��v��(H2O)
D��c(CO2)��c(CO)
(4)���ݷ�Ӧ���������Ƶ���K1��K2��K3֮��Ĺ�ϵʽ_________���ݴ˹�ϵʽ���ϱ����ݣ�Ҳ���ƶϳ���Ӧ����____________(��������������������)��Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��_______(��д���)��
A����С��Ӧ�����ݻ� B������Ӧ�����ݻ�
C�������¶� D�������¶�
E��ʹ�ú��ʵĴ��� F���跨����CO����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A��B��F�Ǽ�ͥ�г������л��F������ʳƷ��װ��E��ʯ�ͻ�����չˮƽ�ı�־����������ת����ϵ�ش����⡣

��1���ֱ�д��A��E�й����ŵ����ƣ�A��_________��E��_________��
��2��������������Ϊ________________��
��3��д����Ӧ���ͣ���_________��
��4����д�����з�Ӧ�Ļ�ѧ����ʽ��
��д��A��B��Ũ�����м��ȷ�Ӧ�ķ���ʽ_________________��
��B�ڽ���ͭ�������ڿ����м��ȷ�Ӧ________________��
��5��F��һ�ֳ����ĸ߷��Ӳ��ϣ��������Ǵ����˾�ķ��㡣Ȼ�������ֲ�����ɵĵ����ijһ����������__________________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼��Ԫ�صĵ��ʼ��仯�����ڻ���ҽҩ�����ϵ��������Ź㷺��Ӧ�á��ش��������⣺
��1��Fe(H2NCONH2)6](NO3)3�������������������غ���(��)����һ����Ҫ�������û�������Fe3+�ĺ�������Ų�ʽΪ___�������ǽ���Ԫ�صĵ縺���ɴ�С��˳��Ϊ___��̼ԭ��Ϊ____�ӻ���NO3-�Ŀռ乹��Ϊ____��
��2��Ŀǰ���ֵ���ԭ�Ӵ�Al13��������±�����ƣ���ԭ�Ӵ�Al13����____���塣Na[Al(OH)4]���ڵĻ�ѧ���� ___������ĸ����
A ���Ӽ� B ���Լ� C �Ǽ��Լ� D ��λ�� E ��� F ������
��3����֪��

��Ӧ���Ҽ�������1 molʱ���м�___������ӡ����١�����____����
��4����ԭ�ӷ����и�ԭ������ͬһƽ�棬�����ƽ�е�p�������p���ӿ��ڶ��ԭ�Ӽ��˶����γɡ�����м�������SO2�����д��ڡ�����м������ɱ�ʾ�ɦ�34����![]() �������еġ�����أ�����ɱ�ʾΪ_______
�������еġ�����أ�����ɱ�ʾΪ_______
��5����������̼�ܽ���r-Fe���γɵ�һ�ּ�϶�����壬����Ϊ���������ṹ����ͼ��ʾ���������ܶ�Ϊd g��cm-3���������������̼ԭ��֮��ľ���Ϊ_____ pm�������ӵ�������ֵ��NA��ʾ��д����ļ���ʽ���ɣ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̿��ԭ��Ҳ���Դ������������ij�ܱ������м��������Ļ���̿��һ����NO��������ӦC(s) + 2NO(g)![]() N2(g) + CO2(g) + Q��Q��0������T1��ʱ����Ӧ���е���ͬʱ�䣬��������ڸ����ʵ����ʵ���Ũ�����£�
N2(g) + CO2(g) + Q��Q��0������T1��ʱ����Ӧ���е���ͬʱ�䣬��������ڸ����ʵ����ʵ���Ũ�����£�
ʱ�� /min | 0 | 10 | 20 | 30 | 40 | 50 | |
Ũ�� /mol��L-1 | NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 | |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 | |
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ________��0-10 min��NO��ƽ����Ӧ����Ϊ____________��
��30 min��ֻ�ı�ijһ���������ݱ��������жϸı������������__________����Ӧ�أ�ƽ��__��ѡ���ţ���
a��������Ӧ�����ƶ� b�����淴Ӧ�����ƶ� c���������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ס�����Ԫ���ڿ�����������Ҳ��������Ҫ����;����ش��������⣺
��1����ԭ���ڳɼ�ʱ���ܽ�һ��3s���Ӽ�������3d�ܼ����μӳɼ���д���ü���̬ԭ�ӵĺ�������Ų�ʽ________ ��
��2��N��P����+5�ۣ�PCl5���γ������;��壬�����к���[PCl4]+��[PCl6]������[PCl4]+�ռ乹��Ϊ___________����NCl5�����ڣ���ԭ����___________________��
��3��N��P����Ԫ�ض����γɶ�����̬�⻯�������N2H4)Ϊ��Ԫ�����ˮ�еĵ����백���ƣ�д��������ˮ�е�һ�����뷽��ʽ_______________________��
��4�������Ʋ��HC1O4����H5IO6[��д��(HO)5IO]����HIO4�������ʵ�������ǿ������˳��Ϊ_________(�����)��
����֪һ�������·�����Ӧ��Na2O+NaCl=Na3OCl���÷�Ӧ�������ƻ����γɵĻ�ѧ����_________��
��5��������������ֱ���������Σ���ͼb���ͻ�״ƫ�����Σ���ͼc��������������Ӷ��������������壨ͼa��ͨ��������ԭ�����Ӷ��ɡ�ֱ���������ε�������ӣ�ͼb���У���ԭ�Ӻ���ԭ�ӵ�ԭ�Ӹ�����Ϊn��____����3����ԭ�ӵĻ�״ƫ�����ε�������ӣ�ͼc���Ļ�ѧʽΪ_____��

��6����ԭ�ӷ����и�ԭ������ͬһƽ�棬���л���ƽ�е�p�������p���ӿ��ڶ��ԭ�Ӽ��˶����γ�����м��������еĦм����÷��Ŧ�![]() ��ʾ������m���������γɴ�м���ԭ������n���������γɴ�м��ĵ��������籽�����еĴ�м��ɱ�ʾΪ������SO2�еĴ�м�Ӧ��ʾΪ___________��
��ʾ������m���������γɴ�м���ԭ������n���������γɴ�м��ĵ��������籽�����еĴ�м��ɱ�ʾΪ������SO2�еĴ�м�Ӧ��ʾΪ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��������һ����Ҫ��Ӧ�ǣ�CO(g)+H2O(g)=CO2(g)+H2(g)��
��֪��25��ʱ����C(s)+![]() O2(g)
O2(g)![]() CO(g) H4=-111kJ/mol
CO(g) H4=-111kJ/mol
��H2(g)+![]() O2(g)=H2(g) H2=-242kJ/mol
O2(g)=H2(g) H2=-242kJ/mol
��C(s)+O2(g)=CO2(g) H2=-394kJ/mol
����˵������ȷ���ǣ� ��
A.25��ʱ��![]()
B.����ѹǿ����Ӧ�ٵ�ƽ�����淴Ӧ�����ƣ�ƽ�ⳣ��K��С
C.��Ӧ�ٴﵽƽ��ʱ��ÿ����![]() ��ͬʱ����0.5molO2
��ͬʱ����0.5molO2
D.��Ӧ�ڶϿ�2molH2��1molO2�еĻ�ѧ�������յ��������γ�4molO-H�����ų���������484kJ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com