
【题目】氮、磷、硫、氯元素在科研与生产中也有许多重要的用途。请回答下列问题:
(1)磷原子在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态原子的核外电子排布式________ 。
(2)N和P都有+5价,PCl5能形成离子型晶体,晶格中含有[PCl4]+和[PCl6]-,则[PCl4]+空间构型为___________。但NCl5不存在,其原因是___________________。
(3)N、P两种元素都能形成多种气态氢化物。联氨(N2H4)为二元弱碱,在水中的电离与氨相似,写出联氨在水中第一步电离方程式_______________________。
(4)①请推测①HC1O4、②H5IO6[可写成(HO)5IO]、③HIO4三种物质的酸性由强到弱的顺序为_________(填序号)。
②已知一定条件下发生反应:Na2O+NaCl=Na3OCl,该反应过程中破坏和形成的化学键有_________。
(5)复杂磷酸盐有直链多磷酸盐(如图b)和环状偏磷酸盐(如图c)。其酸根阴离子都是由磷氧四面体(图a)通过共用氧原子连接而成。直链多磷酸盐的酸根离子(图b)中,磷原子和氧原子的原子个数比为n:____;含3个磷原子的环状偏磷酸盐的酸根离子(图c)的化学式为_____。

(6)多原子分子中各原子若在同一平面,且有互相平行的p轨道,则p电子可在多个原子间运动,形成离域π键。分子中的π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为Π,则SO2中的大π键应表示为___________。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为Π,则SO2中的大π键应表示为___________。
【答案】1s22s22p63s13p33d1(或[Ne] 3s13p33d1) 正四面体 N原子最外层没有d轨道 N2H4·H2O ≒ N2H5++OH—(或N2H4+H2O ≒ N2H5++OH—) ①③② 离子键 3n+1 P3O93- ![]()
【解析】
本题考查了核外电子排布式,最高价含氧酸酸性大小,大Π键以及确定化学式等物质结构与性质的相关知识,难度适中。
(1)P原子基态电子排布式为[Ne]3s23p3,磷原子在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态原子的核外电子排布式[Ne]3s13p33d1。
(2)[PCl4]+中P原子的价层电子对数=4+1/2(5-1-4×1)=4,采取sp3杂化,因而其空间构型为正四面体;P原子半径比N原子大且有可以利用的3d空轨道采取sp3d杂化,P原子周围可容纳较多的配位体形成较高配位数的化合物;N原子半径小没有可以利用的3d空轨道,配位数只能达到4,因此PCl5存在但NCl5不存在。
(3)氨在水中的电离方程式为NH3+H2ONH4++OH-,而联氨(N2H4)为二元弱碱,在水中的电离与氨相似,故联氨在水中第一步电离方程式为N2H4+H2ON2H5++OH-。
(4)①由于非金属性Cl>Br>I,非金属性越强,则对应的最高价氧化物的酸性越强,则①的酸性最强。在②③中都是碘元素的含氧酸,非羟基氧个数越多,酸性越强,则酸性为③>②,故三种物质的酸性由强到弱的顺序为①③②。
②反应物和生成物均是离子化合物,且只含离子键,因而该反应过程中破坏和形成的化学键为离子键。
(5)由图可知,直链多磷酸盐的酸根离子(图b)中,每个P原子占有两个O原子,另有两个氧原子与另一个磷原子共用占一半,最后首尾两个氧原子各一半为整个分子的,故磷原子和氧原子的原子个数比为n:3n+1;图c中,有3个P原子,和9个O原子,P的化合价为+5,O的化合价为-2,该离子所带电荷为(+5)×3+(-2)×9=-3,因而该化学式为P3O93-。
(6)SO2是sp2杂化,有一个未参与杂化的p轨道(假设为pz),其中有一对孤电子对。而氧的三个p轨道中有2个单电子,其中一个参与成键,另外一个未参与成键的p轨道,因为有2个氧,所以一共有相互平行的3个p轨道(包含pz),其中有4个电子(S提供2个,氧各1个),因此形成![]() 键。
键。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为HOOC![]() CH2—COOH,下列说法正确的是
CH2—COOH,下列说法正确的是
A. 苹果酸中能发生酯化反应的官能团有2种
B. 1mol苹果酸可与3mol NaOH发生中和反应
C. 1mol苹果酸与足量金属Na反应生成生成1mol H2
D. HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请分析下图装置。

⑴Fe电极是_____(填“正”或“负”)极,其电极反应为________;
⑵Cu电极是_____电极,其电极反应为________________。
⑶若用浓硝酸做电解质溶液____做负极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白黎芦醇具有抗氧化和预防心血管疾病的作用,下列有关白黎芦醇的说法正确的是
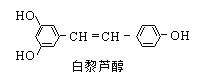
A.白黎芦醇能与NaHCO3溶液反应
B.分子中共含有8种化学环境不同的氢原子
C.1 mol白黎芦醇最多能与7 mol氢气加成
D.1 mol白黎芦醇最多能反应溴水中的3.5 molBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双氧水是常见的氧化剂、消毒剂,一种制取双氧水的流程如下:
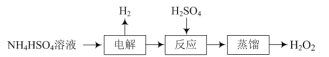
(1)“电解”后生成(NH4)2S2O8,该反应的化学方程式为______。
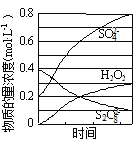
(2)“反应”中部分物质的浓度变化如图所示,该反应的离子方程式为______。
(3)双氧水中H2O2的含量可以用酸性KMnO4溶液来测定,测定时MnO![]() 被还原成Mn2+,测定反应的离子方程式为______。
被还原成Mn2+,测定反应的离子方程式为______。
(4)pH=6时,(NH4)2S2O8溶液与足量MnSO4反应有MnO2沉淀生成,过滤后所得滤液中含硫微粒均为SO42-,该反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解AgNO3溶液,说法不正确的是( )
A.电解过程中阴极质量不断增加
B.电解过程中溶液的pH不断降低
C.此时向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况
D.电解后两极产生的气体体积比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4-溴环己烯主要用于有机合成,它可发生如图所示的转化,下列叙述错误的是( )

A. 反应①为氧化反应,产物含有溴原子和羧基两种官能团
B. 反应②为取代反应,产物含有羟基和碳碳双键两种官能团
C. 反应③为消去反应,产物含碳碳双键和溴原子两种官能团
D. 反应④为加成反应,产物只含溴原子一种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水星大气中含有一种被称为硫化羰(化学式为COS)的物质。已知硫化羰与CO2的结构相似,但能在O2中完全燃烧,下列有关硫化羰的说法正确的是
A. OCS的电子式为![]()
B. OCS分子中三个原子位于同一直线上
C. OCS的沸点比CO2的低
D. OCS分子中含有1个σ键和1个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下结构简式表示一种有机物的结构,关于其性质的叙述不正确的是( )
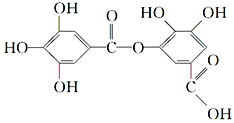
A. 它有酸性,能与纯碱溶液反应
B. 可以水解,其水解产物只有一种
C. 1mol该有机物最多能与7 mol NaOH反应
D. 该有机物能发生取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com